【病例7-10】以急性播散性脑脊髓炎为首发表现的SLE
患者,女,25岁,因“四肢无力20余天”于2015年7月22日来诊。
主要病史:患者于入院3周前(2015年6月30日)夜间无明显诱因出现嘴唇闭合不全,渐左侧肢体乏力,左上肢抬举困难,左下肢行走困难,于当地医院就诊。6月30日,行头部CT扫描提示右额叶可疑稍低密度影,对症治疗(具体不详)后,症状进行性加重。7月1日出现双侧肢体功能完全丧失,并抬头困难,反应迟钝,并发热、头痛、恶心呕吐,舌强不能言语,大小便失禁,偶有四肢抽搐,查体示四肢腱反射消失,左侧巴宾斯基征(+),遂于7月5日转到武汉某三甲医院神经内科。诊断为急性播散性脑脊髓炎,给予甲泼尼龙、头孢哌酮钠他唑巴坦钠,依诺肝素钠注射治疗,上述症状稍缓解,但仍双侧肢体无力,伸舌困难,言语困难症状稍缓解,并于7月15日出现左前胸部带状疱疹,给予更昔洛韦针治疗,入院时疱疹处已结痂。既往体健,无特殊病史。
入院查体:查体欠合作,颈项软,意识清楚,眼睛闭合仅持续1秒,应答切题,言语模糊,伸舌困难,鼻唇沟尚对称,口腔黏膜可见弥漫的白斑,左侧肢体肌力0级,右侧肢体肌力Ⅱ~Ⅲ级;左侧肢体腱反射消失,右侧肢体腱反射减弱,小便引流,大便不自主。左侧巴宾斯基征(+),右侧巴宾斯基征(±)。
辅助检查:血常规示外周血白细胞2.2×109/L,无贫血及血小板计数减少。尿常规:尿蛋白(+);肾功能(2015年7月9日):尿素氮15.32 mmol/L,肌酐 177.8 µmol/L;艾滋病毒抗体(-),梅毒特异性抗体(-),血沉115 mm/h,ANA 1∶3 200,抗SSA抗体(+),抗Sm抗体(+),红斑狼疮细胞(+)。
MRI扫描+增强+MRS(2015年7月13日)显示:双侧半卵圆中心、右侧基底节区及颞叶见大片常T1高Flair信号;右侧侧脑室受压,中线左偏约5.8 mm,增强扫描上述异常信号区未见明显强化,右侧额顶部柔脑膜强化稍明显。
颈椎、胸椎平扫+增强(2015年7月13日)显示:颈椎以C5未中心曲度稍反弓,C3/4~5/6椎间盘轻度退行性改变;胸椎、颈髓、胸髓未见明显异常。
2015年7月23日,入院后复查头部MRI(图7-36)显示:双侧额顶叶脑白质区片状长T1、长T2及T2 FLAIR高信号影,邻近脑沟变浅,图7-36分别为轴位T1WI、T2WI、T2-FLAIR。
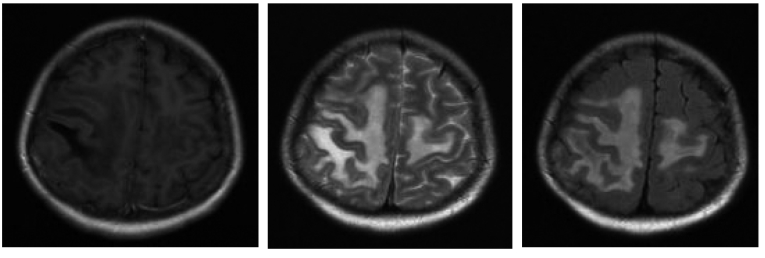
图7-36 头部MRI影像(一)
诊治经过:入院诊断为SLE,急性播散性脑脊髓炎。通过影像学诊断,因颅内压一直很高,腰椎穿刺及颅内活检均风险很大,患者及家属均拒绝。治疗予甲泼尼龙、羟氯喹、白芍总苷、环磷酰胺及丙种球蛋白治疗。1个月后患者症状逐渐好转。2015年8月24日,复查头部MRI(图7-37)提示病灶明显缩小,右侧额叶示片状脑软化灶,呈长T1、长T2及T2FLAIR低信号影。
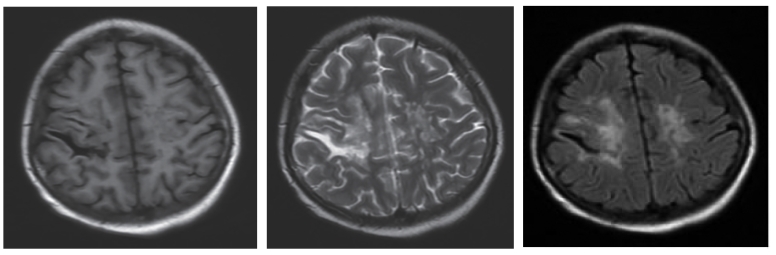
图7-37 头部MRI影像(二)
总结:本例患者在急性期使用大剂量甲泼尼龙联合环磷酰胺治疗,并同时使用丙种球蛋白免疫支持治疗。患者颅内炎性病变吸收明显。2个月后,患者因出现停经,换用霉芬酸酯继续治疗。随访3个月后患者生活基本可以自理,目前对该病例密切随访中。
病例提供者:吴志红(武汉市中西医结合医院风湿免疫科)
【病例7-11】SLE颅内出血并发静脉窦血栓[1]
患者,女,15岁,因“发热伴头晕半月,言语不清一周”入院。
2015年12月13日颅脑MRI扫描(图7-38)提示顶枕部头皮下异常信号影(红色箭头);2015年12月30日头颅MRI扫描(图7-39)提示左侧颞叶、右侧顶叶、颞叶、枕叶及右侧小脑半球异常信号影,考虑出血灶亚急性期,部分偏慢性;右侧横窦信号异常,可疑亚急性血栓(白色箭头)。入院后,明确诊断为SLE、神经精神性狼疮。予甲泼尼龙冲击后序贯减量,联合环磷酰胺丙种免疫球蛋白、低分子肝素及阿司匹林抗凝等治疗,低分子肝素抗凝2周后改为华法林,症状明显改善,监测INR维持在2.0~2.5后出院。2016年1月6日复查头颅MRI扫描(图7-40)提示右侧顶叶、颞叶、枕叶出血灶(亚急性晚期);横窦信号异常,可疑亚急性血栓,均较2015年12月30日时有所吸收。2016年2月25日复查头颅MRI扫描(图7-41)提示病灶基本吸收。现半年随访病情稳定。现近1年随访,病情稳定。
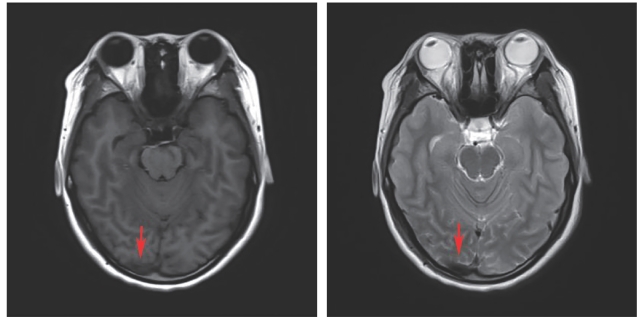
图7-38 2015年12月13日头颅MRI影像
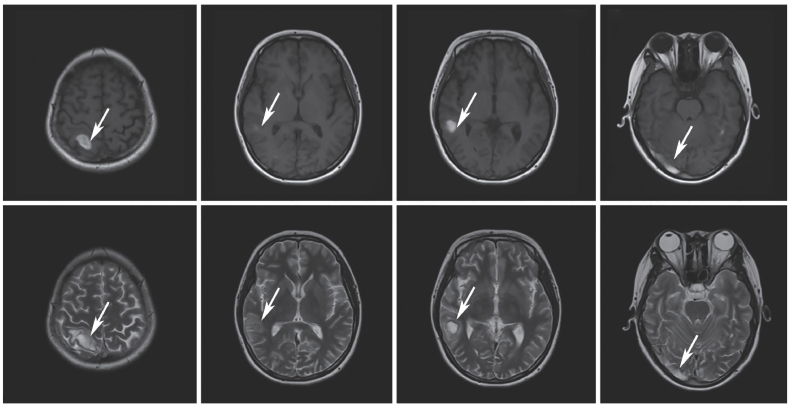
图7-39 2015年12月30日头颅MRI影像
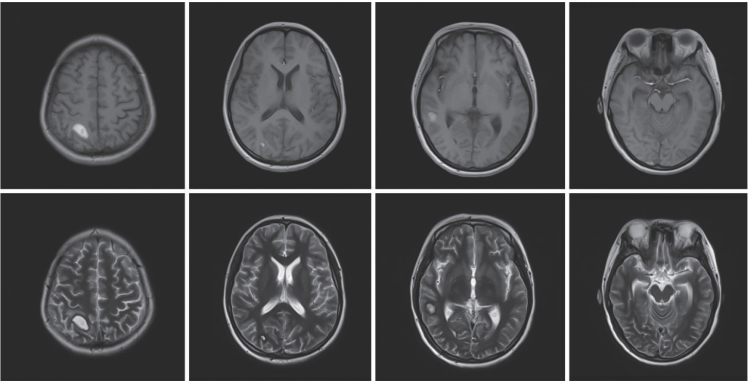
图7-40 2016年1月6日(抗凝治疗后1周)复查头颅MRI影像
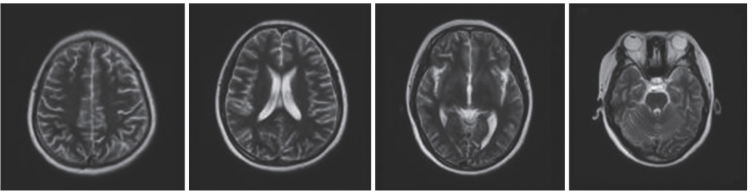
图7-41 2016年2月25日(抗凝治疗6周)头颅CT影像
病例提供者:吴锐、孙虎、李慧(南昌大学第一附属医院风湿免疫科)
【病例7-12】SLE可逆性后部脑病综合征
患者,女,23岁,6个月前因发热、面部红斑、水肿,完善检查后明确诊断为SLE、狼疮肾炎,经糖皮质激素联合免疫抑制剂环磷酰胺及利妥昔单抗治疗后好转。
2016年10月8日头晕,伴恶心、呕吐,呕吐物为胃内容物,随后出现抽搐伴意识不清,视力受损,应用降颅压利尿脱水、降压等治疗后症状改善。脑脊液培养及常规未见明显异常。头颅MRI扫描示双侧额、顶、枕叶白质异常信号,考虑SLE脑病,不除外后部白质脑病。
2016年10月12日,头颅MRI+MRA影像学检查(图7-42)显示:双侧额、顶、枕叶白质内见对称性斑片状长T1、长T2、T2Flair高信号影;脑沟、裂未见增宽,脑室系统未见扩张,中线结构居中。
2016年10月13日,患者突然出现排尿困难及腹痛症状,2016年10月15日全腹CT影像学检查(图7-43)显示:腹腔、盆腔积液。扫描区双侧胸腔积液并双下肺膨胀不全。双侧胸腹壁皮下软组织肿。心包少量积液。
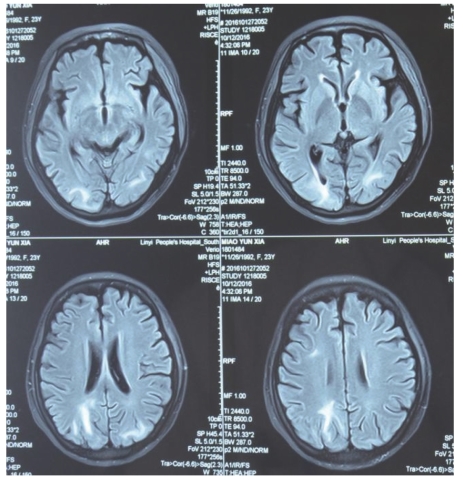
图7-42 2016年10月12日头颅MRI+MRA显示狼疮性脑病
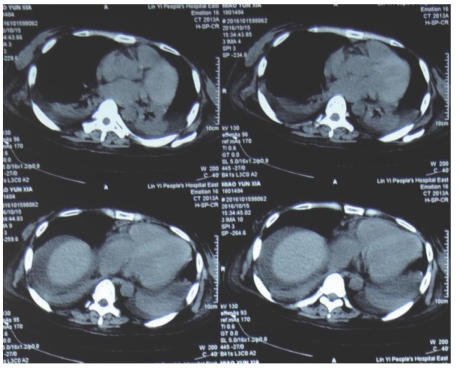
图7-43 2016年10月15日全腹CT显示腹腔、盆腔积液
总结:可逆性后部脑病综合征(posterior reversible encephalopathy sybdrome,PRES)是一组以头痛、视觉障碍、痫性发作、意识障碍和精神异常四联征为主要症状,病灶以对称性累及后部脑白质为主,积极治疗后临床表现及影像学可逆的临床神经影像综合征。1996年,PRES被Hinchey等首次报道。女性多见,急性或亚急性起病。PRES病因包括恶性高血压、严重肾脏疾病、妊娠期子痫(子痫前期)、自身免疫性疾病、恶性肿瘤治疗(顺铂、干扰素)、器官、干细胞移植后、免疫抑制剂使用(环孢素、他克莫司等)。本例患者有SLE、狼疮肾炎病史6月,患者出现头晕、恶心、呕吐、肢体抽搐伴意识不清、视力受损,入院后测血压偏高,全身水肿明显,给予脱水、降压等治疗后意识恢复。符合PRES的诊断。本病需与神经精神狼疮(NPSLE)鉴别。NPSLE可出现多种神经、精神症状,两者鉴别主要通过典型症状、头颅MRI、脑脊液化验等鉴别。NPSLE常需激素冲击联合免疫抑制剂治疗,而PRES治疗以中止诱发因素,积极控制高血压,终止癫痫发作,减轻脑水肿为主,过度应用大剂量激素及强化免疫抑制剂治疗反而加重病情。
病例提供者:张振春(山东省临沂市人民医院风湿免疫科)
【病例7-13】SLE并发硬脑膜炎硬脊膜炎
患者,男,56岁,因“颈背痛2年,头痛、发热10天”于2016年6月2日入院。
主要病史:患者2年前无明显诱因出现颈背部疼痛,夜间为主,伴晨僵,抗炎止痛药可改善。10天前出现阵发性头痛,持续1~2小时,口服氟桂利嗪可缓解;反复发热,体温最高38.5℃,无畏寒、寒战,无咳嗽、咳痰,无腹泻,无尿频、尿急。
入院查体:颈前屈时后颈部、头部疼痛,活动受限,软组织轻度压痛,布氏征阳性。余未查见明显异常。
辅助检查:血常规正常;尿蛋白(±);ANA 1∶1 000均质型;抗核小体抗体(++)、抗组蛋白抗体(++)、核糖体P蛋白(+++)、抗dsDNA抗体(+++);补体C3下降(0.47 g/L)、C4正常;RF、抗CCP抗体、CRP、ESR、肝肾功均正常。Coomb's试验(直接抗人球蛋白试验)(+),IgG4正常,布氏杆菌(-),结核感染T细胞斑点检测(T-Spot)阴性。2016年5月31日头颅普通MRI扫描(图7-44)显示硬脑膜略增厚(红色箭头);2016年6月3日颈椎MRI扫描显示C5/6椎间盘突出(轻度),颈椎退行性变。2016年6月3日腰椎穿刺,脑脊液压力145 cmH2 O,无色透明、细胞数正常,蛋白升高(1 001 mg/L)、糖及氯化物正常,IgM升高(2.73 mg/L)、IgG升高(>103.00 mg/L)、IgA升高(15.2 mg/L)、白蛋白升高(>319.00 mg/L),脑脊液病原学检查阴性。
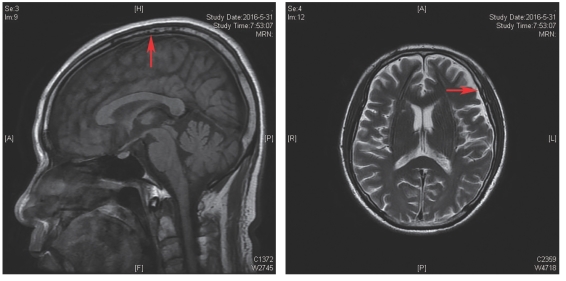
图7-44 2016年5月31日头颅MRI影像
入院诊治经过:明确诊断为SLE,完善腰穿无感染证据,考虑狼疮脑病所致头痛、发热,予甲泼尼龙、环磷酰胺治疗。治疗1周,头痛略有好转。之后再次头痛加重,剧烈难忍,止痛药无效。2016年6月12日复查腰椎穿刺提示脑脊液压力30 mmH2O,蛋白较前明显减低,2016年6月12日复查头颅增强MRI(图7-45)显示:颅内硬脑膜、颈部硬脊膜弥漫性强化、略增厚(红色箭头),符合狼疮性硬脑脊膜炎、低颅压性头痛,给静脉+口服补液每天约3 000 ml、维持原治疗方案。此后1周,患者症状逐渐缓解,于2016年6月27日出院。
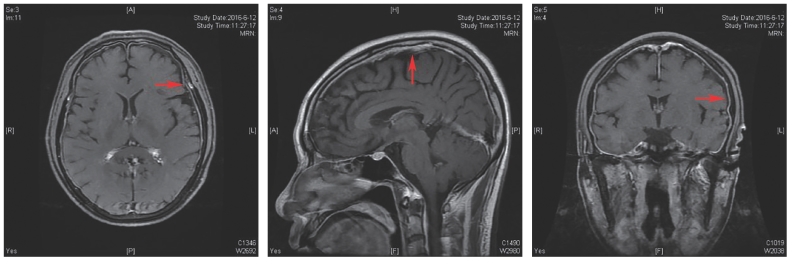
图7-45 2016年6月12日复查头颅增强MRI影像
总结:SLE累及中枢神经系统可出现弥漫性肥厚性硬脑膜炎,有时合并硬脊膜炎,起病隐匿。临床常见表现为头痛、颅神经麻痹、颈肩腰背痛,疼痛具有炎性疼痛的特点;查体可有脑膜刺激征;脑脊液蛋白升高,压力正常。病理常为纤维组织增生伴慢性炎症细胞浸润。本组MRI图像较为典型,平扫MRI显示:T1WI硬脑膜呈等信号弥漫性轻度均匀增厚,T2WI低信号(图7-44);增强MRI扫描显示:硬脑膜、硬脊膜弥漫性均匀强化、略增厚(图7-45)。本例出现脑脊液不足和低颅压性头痛,原因不清,猜测与慢性炎症造成脑脊液生成障碍,或硬膜损伤、脑脊液外渗有关。其他引起硬脊膜炎的疾病包括结核性脑膜炎、真菌病、莱姆病、梅毒、癌性脑膜炎、类风湿关节炎、IgG4相关疾病、ANCA相关血管炎、结节病等,常引起硬膜局灶性或非均匀性增厚、强化。(https://www.xing528.com)
病例提供者:孙明姝(青岛大学附属医院风湿免疫科)
【病例7-14】SLE大脑后部脑病综合征
SLE初发患者,女,28岁。多系统受累,糖皮质激素、免疫抑制剂治疗过程中出现深昏迷,后行头颅MRI扫描显示:双侧额、顶、颞、枕叶、小脑半球及基底节区异常信号影,考虑大脑后部脑病综合征(部分可逆,部分不可逆)。经甲泼尼龙、鞘内注射地塞米松、降颅压等治疗,病灶逐渐吸收。
头颅MRI扫描显示:额叶、基底节区、顶叶多发病灶,在T1相为低信号(图7-46),T2相(图7-47)及FLAIR相(图7-48)为高信号,DWI(图7-49)相额叶、基底节区、部分顶叶为低信号,相应病变在ADC(图7-50)呈现高信号(红色箭头),而顶叶小部分病灶在DWI相为高信号,相应病变在ADC相为低信号(黄色箭头),可逆性后部脑病的诊断主要靠DWI及ADC相病变信号的不同(DWI低信号,ADC高信号),而该患者顶叶小部分病变并不符合后部脑病的MRI改变(黄色箭头),考虑为疾病病变的不同时期。
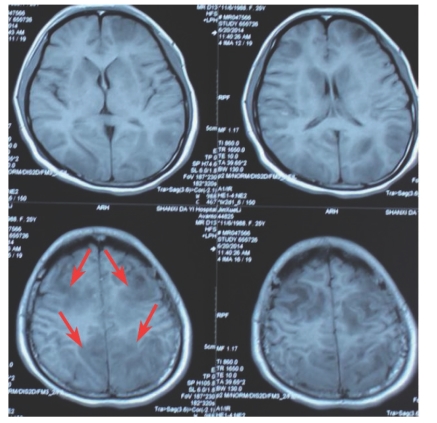
图7-46 头颅MRI影像(一)
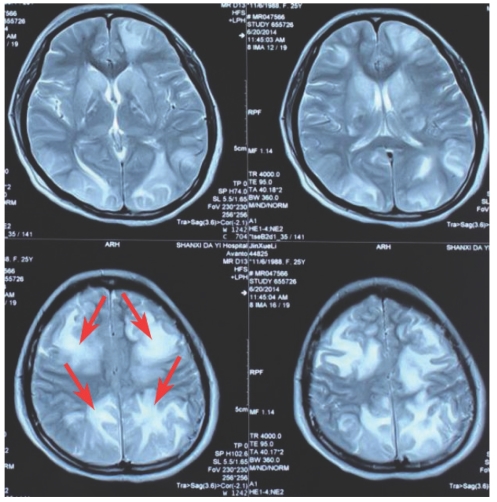
图7-47 头颅MRI影像(二)
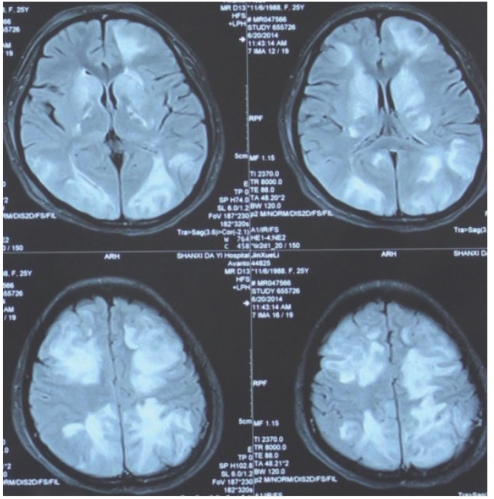
图7-48 头颅MRI影像(三)
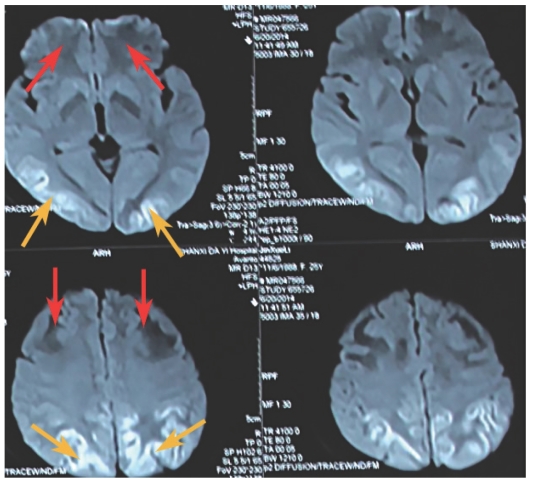
图7-49 头颅MRI影像(四)
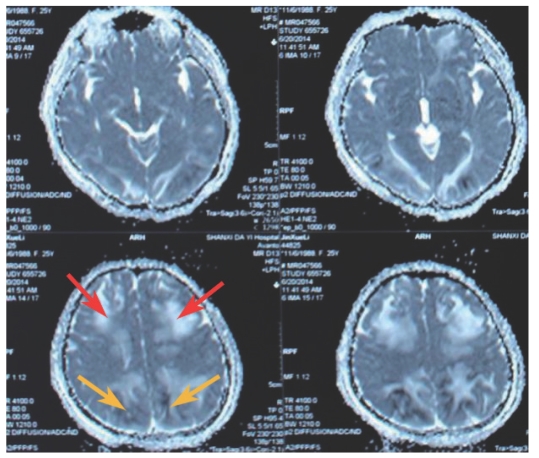
图7-50 头颅MRI影像(五)
治疗前后FLAIR相对比,见图7-51~7-53。

图7-51 2014年6月20日头颅MRI影像
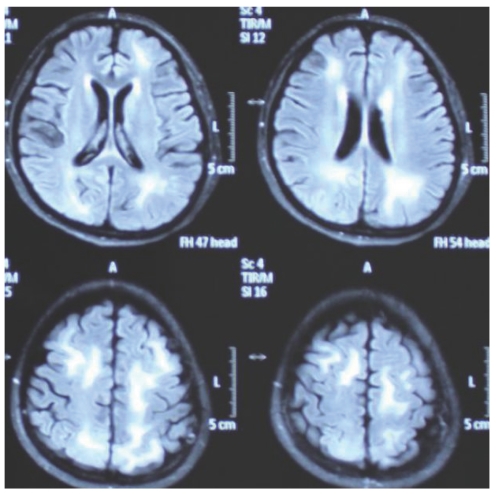
图7-52 2014年7月2日头颅MRI影像
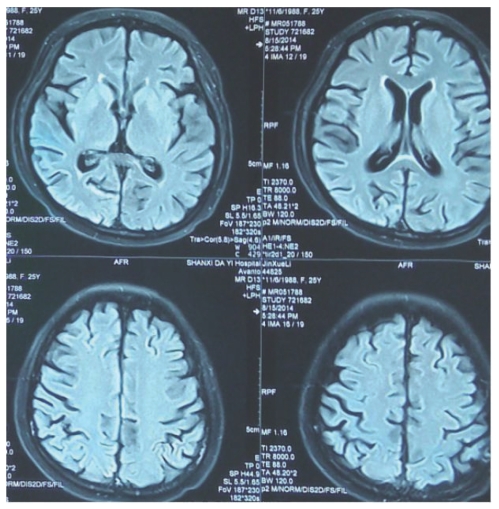
图7-53 2014年8月15日头颅MRI影像
总结:该患者为初发SLE,住院期间出现癫痫大发作、继之深昏迷,头颅MRI+DWI扫描提示可逆性后部脑病综合征(PRES),表现为DWI(图7-49)相额叶、基底节区、部分顶叶为低信号,相应病变在ADC(图7-50)呈现高信号(红色箭头),提示为血管源性水肿,以此与细胞毒性水肿鉴别。PRES常见病因有高血压脑病、子痫或先兆子痫、肾脏疾病,而该患者有明确的SLE病史,无高血压病史,住院期间血压基本波动在正常范围内,故考虑为SLE的神经系统受累,经过大剂量激素冲击治疗、鞘内注射甲氨蝶呤+地塞米松2次等治疗后病情好转。随访至今,患者病情平稳,无后遗症。
病例提供者:杨艳丽、张莉芸、张改连[山西医学科学院(山西大医院)风湿免疫科]
【病例7-15】SLE合并神经精神狼疮
SLE患者,女,21岁。患者半年前无明显诱因出现全身多关节疼痛,以膝关节及肘关节为甚。2个月前,逐渐出现肌肉酸痛伴乏力。近半月颜面部及后背部出现红色斑片状皮疹。2天前出现步态不稳,1天前出现口齿不清、小便失禁、四肢软瘫。
查体:神志淡漠,反应迟钝,不能发音,不能伸舌、张口及吞咽,颈软,双侧瞳孔等大等圆,直径3 mm,对光反射灵敏,可睁眼、闭眼、左眼球运动正常,右眼向左凝视,颜面部及前胸部可见斑片状皮疹。颈部及腋窝可触及多发肿大淋巴结,质软,活动度尚可。双肺呼吸音粗,可闻及喘鸣音,心率86次/分,律齐,未闻及病理性杂音,腹软,肝脾肋下未及,左上肢肌张力升高,双上肢远端肌力Ⅱ级,近端肌力Ⅰ级,双下肢肌力0级、肌张力减低,双下肢不肿,双侧巴氏征(+)。
辅助检查:血常规检查提示中度贫血。尿常规检查提示血尿、脓尿、蛋白尿。转氨酶及肌酶升高。血沉100 mm/1 h,CRP 29.1 mg/L,降钙素原0.47 ng/ml。ANA 1∶10 000均质型,抗U1RNP抗体、抗SSA抗体、抗核糖体P蛋白、抗核小体抗体、抗组蛋白、抗dsDNA抗体阳性,抗核小体抗体>200.0 RU/ml,P-ANCA阳性,ANCA、抗磷脂抗体阴性。补体C3 0.19 g/L、C4 0.01 g/L。12月17日检查抗心磷脂抗体、抗β2糖蛋白1抗体均阴性。Coomb's试验阳性。
12月16日头颅增强MRI扫描(图7-54)显示:双侧内囊后肢、脑干(中脑、脑桥、桥臂及延髓)见对称性线样及片状稍长T1、长T2信号(圆圈所示),信号不均,边界欠清,局部脑实质较疏松;T2-Flair序列示上述区域呈明显不均匀高信号,增强扫描未见异常强化。
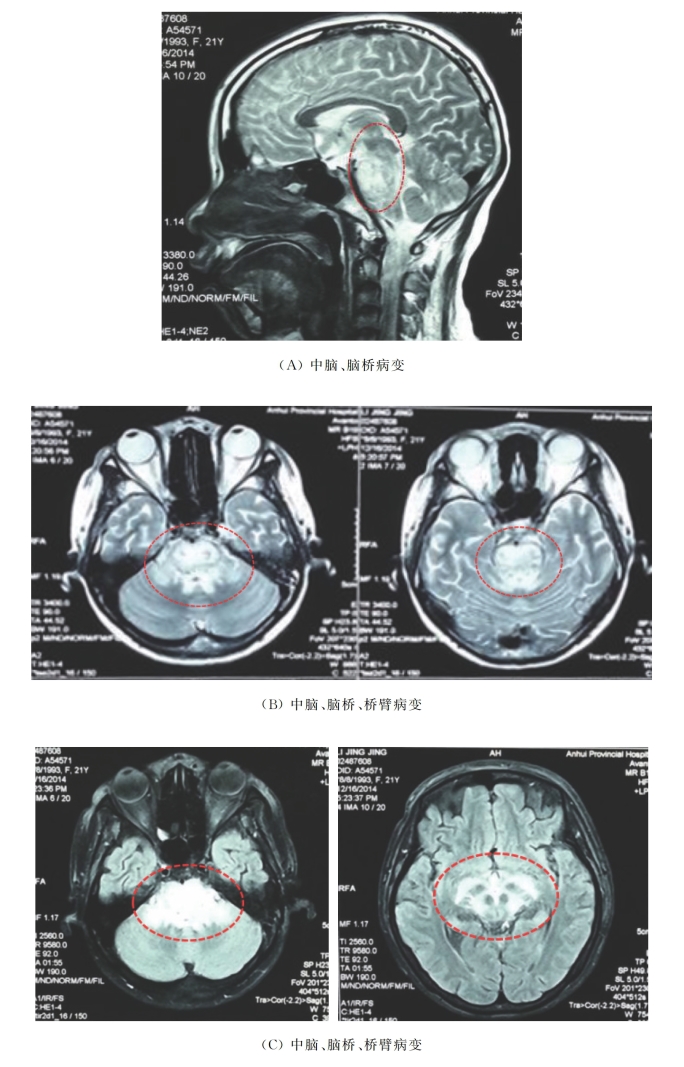
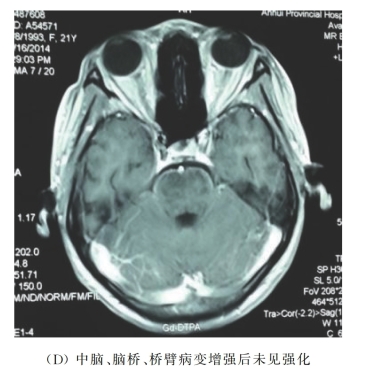
图7-54 头颅MRI影像
诊断为SLE、狼疮性肾炎、神经精神性狼疮。
治疗予甲泼尼龙、地塞米松、环磷酰胺、丙种球蛋白、脱水降颅压、对症支持。治疗前与治疗20天后头颅MRI对比(图7-55),治疗5个月后复查头颅MRI(图7-56)扫描显示:原病变异常信号范围缩小。
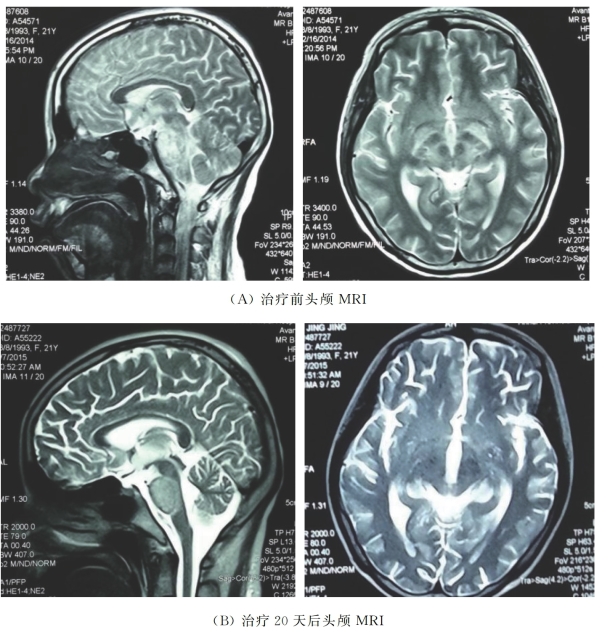
图7-55 治疗20天后头颅MRI对比
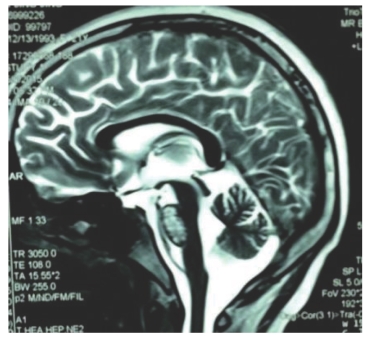
图7-56 治疗5月后头颅MRI影像
院外治疗及随访:口服泼尼松、羟氯喹维持;尿蛋白(-)、血常规及炎症指标等均正常。目前,患者病情稳定、言语清晰、大小便能自解,思维清晰、生活自理。
总结:约2/3的SLE患者出现不同程度的神经精神症状,但像该患者引起广泛颅内病变者罕见。因此,在临床上应高度重视SLE的神经系统病变。发现有头痛、耳鸣、口齿不清、肢体瘫痪等症状者,应积极完善脑脊液、头颅MRI,必要时行脊髓MRI等检查。通常情况下,脑脊液检查可见蛋白及免疫球蛋白水平升高,且有助于排除感染。其次,头颅MRI检查对诊断结构性脑部病变具有重要价值,该患者表现为双侧内囊后肢、脑干(中脑、脑桥、桥臂及延髓)对称性线样及片状稍长T1、长T2信号、边界欠清、T2-Flair序列示上述区域呈明显不均匀高信号,增强扫描未见异常强化,证实为弥漫性脑炎,可解释患者的临床症状。SLE引起的神经系统病变,部分患者可出现病情快速进展、甚至危及生命,因此,早期诊断、有效治疗对快速控制病情、保护脏器功能、改善预防至关重要。
病例提供者:马艳(安徽省立医院风湿免疫科)
【病例7-16】SLE合并中枢神经系统结核
SLE患者,女,20岁,病史2年,使用糖皮质激素及免疫抑制剂治疗,因“持续高热、头痛1个月”入院。查体提示颈强直,脑膜刺激征阳性,血沉62 mm/h,CRP 12 mg/L,PPD试验阴性,TSPOT-TB阴性,多次血培养阴性。头颅MRI(图7-57)提示双侧丘脑及胼胝体压部可见点片状长T1长T2信号(红色箭头),DWI表现为高信号(圆圈所示),增强扫描后未见上述病灶明显强化,沿小脑幕有强化,脑沟内增强的小血管明显增多。双侧丘脑及胼胝体压部点片状异常信号影。腰穿提示脑脊液压力显著升高(260 cmH2O),脑脊液蛋白20 g/L,脑脊液的糖及氯化物降低,脑脊液多次浓缩找抗酸杆菌均阴性,脑脊液培养42天报告为抗酸杆菌阳性。最终诊断:SLE合并中枢神经系统结核。
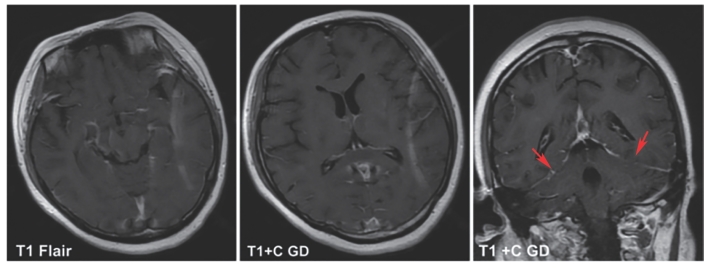
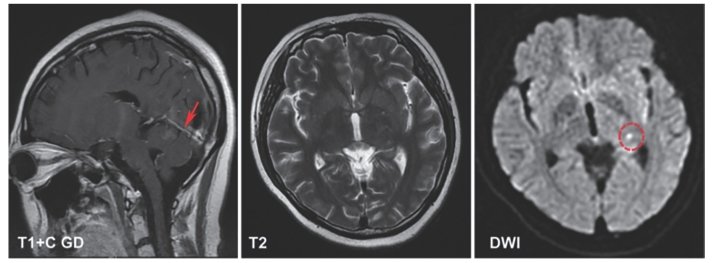
图7-57 头颅MRI影像
总结:该患者的主要表现是头痛,使用糖皮质激素及免疫抑制剂治疗,这是感染的高危因素。患者有颅内感染的阳性体征脑膜刺激征,脑脊液蛋白非常高,头颅MRI提示脑膜有明显强化,应该高度怀疑感染,最终脑脊液培养阳性证实是结核感染。
病例提供者:姚海红(北京大学人民医院风湿免疫科)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




