4.1.1.1 概述
金属元素,特别是有毒有害重金属元素的分析是环境监测的重点内容之一。金属元素及其化合物的毒性大小与其元素种类、理化性质、浓度及存在的价态和形态关系密切。因此,确定元素的种类、总量和形态是金属元素分析最主要的目的。通过对金属元素种类、总量和形态的认识,帮助研究者评价或预测样品的环境效应、生态效应的元素分析在环境样品分析中起重要作用。
金属元素仪器分析技术发展至今,常用的分析方法包括原子光谱法和原子质谱法等。其中原子光谱法由于技术成熟、成本相对较低,是最常用的金属元素定量仪器分析方法。原子光谱法的理论依据是原子核外电子在基态和激发态之间迁移时引起能量变化从而导致光谱变化,根据原子光谱的特征谱线及其强度可以对金属元素进行定性定量分析。原子光谱包括原子吸收光谱(Atomic Adsorption Spectrometry,AAS)、原子发射光谱(Atomic Emission Spectrometry,AES)和原子荧光光谱(Atomic Fluorescence Spectrometry,AFS)等。原子质谱法(Atomic Mass Spectrometry,AMS)则是利用元素在等离子体中形成的一价阳离子的质荷比及强度来对金属元素进行定性定量分析。
上述仪器分析方法在金属元素定量分析中各有优势。从测量的元素范围来看,AES和AMS适用分析的元素范围较广,可用于分析元素周期表中绝大部分金属元素及部分类金属的非金属元素;从分析灵敏度来看,AFS对于分析波长小于300nm 的元素有更低的检测限,AMS对大多数元素来说都具有较低的检出限;从标准曲线的动态范围来看,AAS通常小于2个数量级,AFS为4~5个数量级,AES和AMS甚至更宽;此外,从分析仪器的操作应用来看,AAS、AFS和AMS的仪器设备相对简单,易于操作,AAS和AFS运行成本较低,AES和AMS运行成本较高,特别是当AMS在超净间中运行时,运行成本会更高。
在环境样品实际分析时,需根据样品性质及监测目的选择合适的仪器分析方法来实现元素含量及形态的定性定量分析。
4.1.1.2 仪器分析对样品的要求
环境样品有气、固、液三种状态,不同状态、性质样品的保存、预处理及分析方法不同。气态样品主要是指室内外空气样品;固体样品主要有风干土壤、垃圾、沉积物、底泥、污泥以及动植物样品等;液体样品主要指水样,水样包括范围很广。常见的有饮用水、地表水、雨水、污废水以及各种处理设施净化后出水等多种。
由于特定仪器构造及分析过程对基体的要求,上机分析的样品需为液体(配备特殊进样系统除外)、样品中有机物和盐的含量尽量低、不含颗粒物等容易堵塞仪器管路系统的物质。
虽然不同状态的样品可以选择不同的进样方法,但目前市面上大多数仪器的配置不支持气态或固态等特殊状态样品的直接进样分析。将液体引入分析仪器(溶液雾化法)仍是应用最广泛、优先考虑的方法。实践也表明,溶液雾化法相对具有较好的稳定性,能获得良好的分析准确度和精密度,操作较易掌握。混浊水样和固体样品则需事先进行预处理,将待测元素转移到水相后再进行检测。空气中的金属元素主要是附着在颗粒物上,测定含量时须先采集颗粒物及尘埃(采样时通常使用滤片收集颗粒物)。采集到的样品连同滤片一起,可参考固体样品方法进行保存、预处理及分析。
样品中的有机物和盐对分析过程的影响主要体现在基体效应和长期稳定性上。基体匹配是外标分析法的基本原则之一。市售常规元素标样的基体为稀酸体系,不含有机物,含盐量也很低,去除样品中的有机物并降低含盐量可以获得较高的分析准确度。此外,有机样品分解时需要更高的能量,容易导致仪器火焰或等离子体熄灭。对于发射光谱和等离子体质谱而言,有机物在分析过程中容易形成积碳,盐分也容易积累在样品通道中,导致分析灵敏度的变化,从而影响分析结果的稳定性。因此,对于含有机物的样品建议先消解处理分解有机物后再进行分析,对于不适合消解的有机样品可考虑选择基体匹配的标准溶液并更换有机进样系统,调整进样条件后再进一步分析。而高含盐样品则应通过稀释、增加系统清洗频率或更换基体匹配的标准溶液等方法提高分析准确度。
仪器的雾化器喷嘴及进样毛细管,由于管径细小,极易被颗粒物堵塞,同时颗粒物也容易造成样品均匀性差,导致结果偏差大等,因此待测样品应事先去除颗粒物。此外,随着环境功能材料的开发,含纳米颗粒的样品也逐渐发展为一类新型的环境样品。纳米颗粒本身十分细小,肉眼不可见,虽然不会堵塞管路,但也需注意样品均匀性及颗粒阻抗等可能导致分析结果不准确的因素。
4.1.1.3 样品的采集与保存
样品采集和保存必须具有足够的代表性且在分析前不受任何污染。对于元素分析而言,主要是从保存的容器和方式两方面避免样品中待测元素的污染和损失。保存容器方面,包括玻璃容器和塑料容器两种,以塑料容器为首选。当被测物是痕量金属或是玻璃的主要成分为钠、钾、硼、硅等元素时,特别要避免使用玻璃容器。水样可存放在塑料瓶中,固体样品可保存在洁净的塑料袋中。塑料器皿相对价格较低,有条件可考虑一次性使用。对于样品处理过程中需重复使用的器皿则应用稀酸和去离子水充分清洁后再使用,以免引起交叉污染。国标推荐的部分元素监测项目的保存方法见表4-1。
表4-1 国标推荐部分元素监测项目样品的保存方法
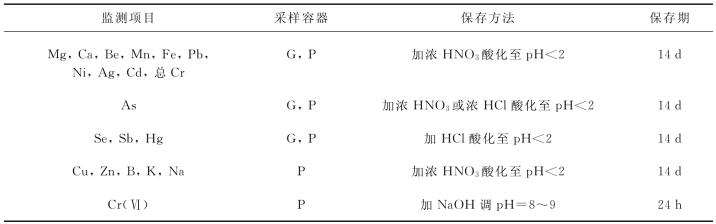
注:①G 为硬质玻璃瓶,P为聚乙烯瓶(桶);②d为天,h为小时。
实验室常用塑料器皿的材质有:高密度聚乙烯(High Density Polyethylene,HDPE)、低密度聚乙烯(Low Density Polythylene,LDPE)、全氟代烷氧乙烯(Perfluoroalkoxene,PFA)、聚四氟乙烯(Polytetrafluoroethylene,PTFE)、聚乙烯(Polyethylene,PE)、聚丙烯(Polyproylene,PP)、聚甲基戊烯(Polymethylpentene,PMP)、聚酯(Polyethylene terephthalate,PET)等。(https://www.xing528.com)
4.1.1.4 水样的消解
水样预处理的目的是使待测组分达到方法和仪器要求的形态、浓度,消除共存组分干扰。水样大都需要预处理才能上机分析。水样预处理包括消解、富集和分离。消解是最常用的预处理方法。消解处理的目的是破坏有机物,溶解悬浮性固体,将各种价态待测元素氧化成单一高价态,或转变成易于解离的无机化合物。消解后的水样应清澈、透明、无沉淀。
水中金属元素状态分为可溶态和悬浮态两种。为避免管路堵塞,仪器分析一般要求溶液中不含直径在0.45μm 以上的颗粒。因此,通常以能否通过0.45μm 微孔滤膜为区分标志,能通过滤膜的金属形态称为可溶态,被截留的为悬浮态,二者之和为水中金属元素的总量。当水样中含有悬浮颗粒时,测试溶解态金属含量需用滤膜等过滤后测试滤液中的金属含量;而分析金属元素总量时则往往先将水样消解后再测定;若需测定悬浮物中的金属,则需用玻璃砂芯、滤膜或滤纸将新鲜水样抽滤,滤渣在103℃~105℃烘干至恒重,然后进行消解和分析。
1.消解试剂和装置
消解试剂通常选用无机酸,包括硝酸(HNO3)、盐酸、氢氟酸(HF)、高氯酸(HClO4)、硫酸(H2SO4)、磷酸(H3PO4)等。硫酸与磷酸介质的黏滞性会在样品的处理中产生影响,且沸点高,难以蒸干,在处理样品时应尽量避免使用。需要特别说明的是HF 和HClO4,HF本身易挥发,具腐蚀性,且能分解以硅为基质样品的无机酸,处理样品时常与HCl、HNO3、HClO4等同时使用。在用HF分解样品时不能用玻璃、石英陶瓷等器皿,经典的是采用以PTFE为材料的烧杯、坩埚等器皿。另外,HF会腐蚀仪器中的玻璃或石英进样系统和炬管等。因此,这类样品在测试之前需先驱赶HF 酸。HClO4是已知最强的无机酸。经常使用它来驱赶HCl、HNO3和HF。需要特别注意的是,热的浓HClO4是强氧化剂,会与有机化合物发生强烈(爆炸)反应。因此,对有机样品应先用HNO3或HNO3/HClO4混合酸处理(HNO3的用量大于HClO4用量的4倍),以避免单用HClO4发生爆炸。
对于仪器分析而言,H2SO4 由于易产生分析吸收,选用火焰原子吸收法时一般不用H2SO4 处理水样;H2SO4 和HClO4 由于基体干扰较严重,在选用石墨炉原子吸收时避免使用,HCl,H2SO4,H3PO4 等易形成盐的酸在质谱中尽量减少使用或不用。试剂纯度的要求与待测元素的含量及试剂的用量有关。对于浓度在mg/L 级以上的样品,消解试剂应为分析纯以上;对于mg/L级以下的样品,消解试剂应使用优级纯级别或经过提纯后的分析纯。通常,当消解试剂的用量是样品量的10倍时,试剂中元素的含量应比样品中元素的含量至少低两个数量级。若消解过程使用酸量较大、酸种类较多或分析准确度要求较高,为避免试剂对待测元素含量的影响,在消解样品的同时应平行制备试剂空白以消除试剂干扰。水中痕量或超痕量元素分析有时需要先预分离和富集,然后再进行含量检测。
金属元素的定性定量分析,特别是痕量分析,比较适合的是惰性材料,如石英聚四氟乙烯或高压聚乙烯制成的器皿。消解常用的容器为硼硅酸耐热玻璃(对含氟样品不适用)或聚四氟乙烯烧杯。所有使用的器皿都要清洗干净,避免器皿对溶液组成的影响导致分析误差。消解过程一般在电热板上进行。为了确保安全,消解应在通风橱中操作。
2.湿式消解法
湿式消解法有多种,适用于不同性质或测试目的的水样。①硝酸消解法,适用于较清洁水样。具体方法如下:取50~100mL代表性水样置于消解容器,加入5mL硝酸,在电热板上加热蒸发至5mL左右,冷却后将消解液及消解容器润洗液全部转移至容量瓶,定容后待测。②硝酸-高氯酸消解法,适用于含难氧化有机物的水样,但不适用于含铅和银的水样。③硫酸-磷酸消解法,适用含Fe3+等离子的水样,磷酸能与Fe3+等金属离子络合,有利于消除Fe3+等离子的干扰。④硫酸-高锰酸钾(5%)消解法,主要适用于消解含汞水样。对于某些特殊水样还可采用多元(三元以上酸或氧化剂组成的消解体系)消解方法,如处理测定总铬的水样时用硫酸、磷酸和高锰酸钾消解。
若水样经消解后仍含颗粒物,一般为不溶性二氧化硅或其他不溶性杂质。可用0.45μm的微孔滤膜过滤后使用。需要特别说明的是,滤膜由于材质或生产过程中的污染,过滤后可能会有杂质(特别是K、Na等元素)溶出,引起测量误差。
4.1.1.5 土壤样品制备
土壤样品在进行消解预处理前应经过风干、研磨、过筛等制备过程。
风干是将土样倒在塑料薄膜或瓷盘内在阴凉处慢慢风干,半干状态时压碎土块,除去植物根茎、叶、石块等杂物,铺成薄层,在室温下经常翻动,充分风干,要防止阳光直射和尘埃落入,并防止酸、碱等气体的污染。风干后的样品易混合均匀,分析结果的重复性、准确性都较好。风干后的土样用有机玻璃棒或木棒碾碎后,反复按四分法[1]弃取,最后留下足够分析用量(重金属测定,可留约100g),再用有机玻璃棒或玛瑙研钵磨细,全部过100目尼龙筛。过筛后的样品,充分摇匀,装入塑料袋中,贴上标签做好记录备用。在制备样品时,必须注意不要被所分析的化合物或元素污染。另外,制备后的样品在最终分析前还可进行含水率的测定以获得更高的分析准确度。上述风干、研磨、过筛的方法常用于土壤、沉积物等环境样品的制备,也可扩展到其他类型的固体样品。
4.1.1.6 固体样品消解
目前常用的固体样品预处理方法主要有酸、碱敞开式容器消解法、干法灰化法和微波消解法。酸、碱敞开式容器消解法基本原理及操作程序和水样消解方法类似。干法灰化法是利用高温除去样品中的有机质,灼烧剩余的灰分用酸溶解作为样品待测溶液,该方法不适用于汞、铅、镉、锡、硒等易挥发元素的分析。
微波消解是指利用微波加热封闭容器中的消解液(各种酸、部分碱液以及盐类)和样品,在高温增压条件下使样品快速溶解的湿法消化法。选择合适的消解试剂及消解程序,能更有效地提取各种固体样品中的金属元素。密闭容器反应和微波加热这两个特点,决定了其提取完全、快速、低空白的优点。商用的微波消解仪一般配有电脑控制系统,可以根据需要设定消解功率、温度及时间程序。为避免实验过程中高温高压以及强酸蒸气带来的安全隐患,操作需严格按照厂商提供的说明书进行。微波消解法已被收录在EPA 及我国环保部的标准方法中,加之商品化的微波消解装置已经相当成熟,使得该项技术成为目前固体样品消解的主流技术之一。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




