液体吸收法净化氮氧化物时,可采用的吸收剂很多,如水、酸、碱、盐溶液都有吸收氮氧化物的能力,可因地制宜地进行选择。下面讨论几种液体吸收法的反应基本原理及有关工艺。
(一)水吸收法
用水吸收氮氧化物时,二氧化氮易溶于水,并与水反应生成硝酸和亚硝酸:
2NO2+H2O→HNO3+HNO2
亚硝酸在一般情况下很不稳定,容易分解:
3HNO2→HNO3+2NO+H2O
NO不与水发生化学反应,在水中的溶解度也很低。水不仅不能吸收NO,并且还在吸收NO2的过程中放出NO,因此水吸收法效果不好,不能用于烟气脱氮。但该法比较简单、经济,可用于含NO2的少量废气的治理。
(二)酸吸收法
可用浓硫酸或稀硝酸作为吸收剂吸收氮氧化物。但两种吸收方法的作用原理是不同的。
浓硫酸吸收氮氧化物是化学吸收。浓硫酸与氮氧化物反应生成亚硝基硫酸,其反应式为:
NO+NO2+2H2SO4→2ONOSO3H+H2O
生成的亚硝基硫酸可用于硫酸生产及浓缩硝酸。在同时生产硫酸和和浓硝酸的企业中,可采用这种方法净化含氮氧化物废气。
稀硝酸吸收法基于氮氧化物在稀硝酸中溶解度大的原理,用稀硝酸吸收净化含氮氧化物废气,这一过程是物理吸收。
在吸收操作中,吸收剂用浓度为15%~20%的硝酸。
(三)碱性溶液吸收法
碱性溶液如NaOH、Na2CO3、Ca(OH)2等,可与NO2反应生成硝酸盐和亚硝酸盐,与H2O3反应生成亚硝酸盐,反应式如下:

由上列反应式中看出,NO不与碱液反应,但是当NO与NO2同时存在,则吸收反应能够进行。当氮氧化物中NO2的量等于或大于NO的量时,吸收将会进行得比较完全。
通常将NO2在NOx中所占的百分比(以摩尔分数计),称为NOx的氧化度。因此,可以说当氧化度等于或大于50%时,吸收较完全。若氧化度小于50%,那么多余的NO就不能被吸收。所以,碱液吸收法不适合于净化以NO为主的燃烧废气,而比较适合于净化氧化度较高的硝酸尾气及硝化废气。(https://www.xing528.com)
在应用碱液作吸收剂时,除了考虑吸收剂的吸收效果外,还要考虑其他操作问题。如用石灰乳吸收,石灰价格便宜,但Ca(OH)2溶解度小,未溶的石灰易堵塞管道,故不常用。氨水也可以吸收NOx,但生成物亚硝酸铵很不稳定,在某些条件会产生爆炸,使氨水吸收法使用受到限制。
碱性溶液吸收法采用较多的是以NaOH和Na2CO3溶液为吸收剂。Na2CO3便宜,吸收净化费用低,但效果略低于NaOH吸收法。
(四)氧化吸收
氧化吸收法主要是用于以NO为主的氮氧化物净化过程,先将NOx中的NO氧化,将废气的氧化度提高到易于吸收的程度,再进行吸收脱氧。常用的氧化剂有臭氧(O3)、次氯酸钠(NaClO2)、过氧化氢(H2O2)、重铬酸钾(K2Cr2O7)等。例如主要反应:
2NO+NaClO2+2NaOH→NaNO3+NaNO2+NaCl+H2O
还可用44%~47%的硝酸作氧化剂,其反应如下:
NO+2HNO3→3NO2+H2O
有许多催化剂对NO的氧化过程有显著的催化作用,其中活性炭最为廉价,而且在较低的温度下有良好的催化作用。但用活性炭为催化剂进行NO催化氧化时,要将温度控制在573K以下,防止活性炭自燃。
氧化吸收法可以除去单纯用碱液吸收不能除去的NO,因此在液体吸收法脱氮中很有意义。氧化吸收法因采用的氧化剂不同又可分成硝酸氧化法、活性炭催化氧化法、通氧吸收法、次氯酸盐法、高锰酸钾法、原子氧法等。
(五)吸收还原法
吸收还原法是将吸收到液相的NOx,通过还原反应,将其转化为氮气的方法。采用的吸收剂有尿素[CO(NH2)2]、亚硫酸盐[(NH4)2SO3]或其他的等。吸收反应以(NH4)2SO3为例,方程式如下
2NO+2(NH4)2SO3→2(NH4)2SO4+N2↑
NO2+4(NH4)2SO3→4(NH4)2SO4+N2↑
吸收还原法的脱氮效果很好。但要注意,当吸收液中存在亚硫酸氢铵时,会抑制亚硝酸铵的产生而不利于吸收。必要时可控制亚硫酸氢铵在吸收液中与亚硫酸铵的比例,反应如下:
NH4HSO3+NH4OH→(NH4)2SO4+H2O
图7.13是亚硫酸钠吸收还原法NOx的工艺流程。该法不足之处是NOx不能有效利用。
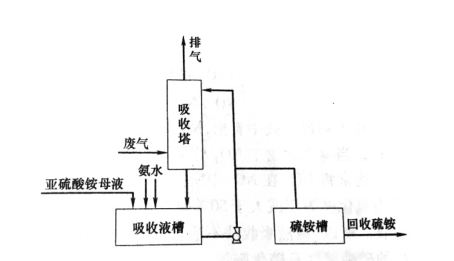
图7.13 吸收还原法工艺流程
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




