烟气脱硫方法通常有两种分类方法:一是根据脱硫过程中生成物的处置分为抛弃法和回收法;二是根据脱硫剂的形态分为干法和湿法。
目前抛弃法在技术上比较成熟,经济上也容易被接受。干法是利用固体吸附剂或催化剂脱除烟气中的SO2;湿法则是采用水或碱性吸收液或含触媒离子的溶液吸收烟气中的SO2。干法脱硫净化后烟气温度降低很少,由烟囱排入大气时利于扩散,生成物容易处理,但反应速度较慢;而湿法脱硫效率高,反应速度也快,但生成物是液体或泥浆,处理较为复杂,而且烟气在吸收过程中的温度降低很多,不利于高烟囱扩散或稀释;喷雾干燥法是将吸收剂浆液喷入烟流中进行吸收,高温烟气使吸收液中水分蒸发,生成物呈干粉状,易于收集。
表7.1汇集了常用的烟气脱硫方法。
本任务将主要介绍锅炉烟气脱硫方法的基本原理、工艺流程和设备。合理选取脱硫工艺需要考虑环境、经济、社会等多方面因素。
表7.1 主要烟气脱硫方法

(一)石灰/石灰石法
石灰石资源丰富,成本低廉,是最早用于烟气脱硫的吸收剂,目前仍为广泛采用。石灰/石灰石法又可以分为湿式石灰/石灰石-石膏法、改进的石灰/石灰石法和喷雾干燥法。
1.湿式石灰/石灰石-石膏法
这种方法是将SO2烟气送入吸收塔内,用石灰石浆液(一般含量5%~10%)作为吸收剂,在塔内与烟气接触,吸收SO2,生成石膏。该法优点是原料易得、价格低廉;缺点是容易发生设备堵塞和磨损。
(1)反应原理
石灰石或石灰浆液吸收烟气中的二氧化硫,先生成亚硫酸钙,然后再氧化为硫酸钙。吸收过程在吸收塔内主要反应如下:

因烟气中有氧,已生成的亚硫酸钙和亚硫酸氢钙氧化成硫酸钙,反应如下:

(2)工艺流程及设备
石灰/石灰石浆液吸收法脱硫工艺流程简单,如图7.1所示。石灰浆液在制备槽中配置,送入循环槽,由循环泵送到吸收塔顶部喷淋。吸收SO2后,得到含亚硫酸钙和硫酸钙的混合浆液由塔底流回循环槽。将pH调整到4左右经泵送入氧化塔,向氧化塔内鼓入空气,进行氧化得到石膏。所得的石膏浆料经过增稠、离心过滤和清洗获得石膏产品。滤液除去杂质后送至石灰石浆液制备槽。常用的吸收设备有喷淋塔、湍球塔、筛板塔、文丘里洗涤器等。
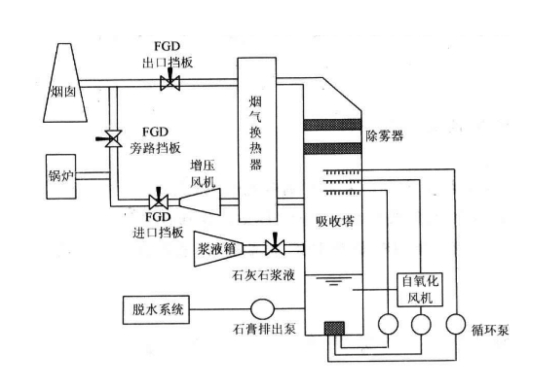
图7.1 石灰/石灰石工艺流程
结垢和堵塞是影响吸收塔操作的最大问题。为防止固体沉积、结晶析出以保证吸收效率,在操作中应注意以下几点:将浆液pH控制在6左右;保持适当的气、液、固比例,以免水分蒸发使固体沉积或结晶析出;在吸收液中加入二水硫酸钙晶种,以提供足够的沉积面积,使溶解盐优先沉淀于其上,来控制因溶液过饱和而沉淀物析出而结垢。在选用吸收器时,应选用持液量大、气液间相对速度高、气液接触面积大,塔内构件少、压力降小的设备。
2.改进的石灰/石灰石法
为了提高SO2去除效率,克服湿式石灰/石灰石-石膏法的结垢问题,发展了改良的方法,即将吸收塔内的吸收介质改为清液以避免结垢问题,吸收SO2之后的溶液用石灰石或石灰再生,生成石膏,再生后的吸收液循环使用。改良方法有很多,如加己二酸缓冲剂法、碱性氧化铝法以及双碱法等。这里简要介绍常用的双碱法。
所谓双碱法是采用碱性金属盐类(Na、+K+、 等)或碱类水溶液吸收SO2,然后用石灰石或石灰再生吸收SO2后的吸收液,将SO2以亚硫酸钙或硫酸钙沉淀形式析出,获得高纯度石膏,再生后的吸收液返回吸收系统循环使用。设计中主要考虑固体容易析出及钠易回收。常用的是钠碱双碱法。
等)或碱类水溶液吸收SO2,然后用石灰石或石灰再生吸收SO2后的吸收液,将SO2以亚硫酸钙或硫酸钙沉淀形式析出,获得高纯度石膏,再生后的吸收液返回吸收系统循环使用。设计中主要考虑固体容易析出及钠易回收。常用的是钠碱双碱法。
钠碱双碱法是用Na2CO3或NaOH(第一碱)溶液进行吸收,反应后的吸收液用石灰石或石灰(第二碱)再生,制取石膏,再生的吸收液循环使用。
用氢氧化钠溶液吸收:
2NaOH+SO2→Na2SO3+H2O
用碳酸钠溶液吸收:
Na2CO3+SO2→Na2SO3+CO2↑
Na2CO3+SO2+H2O→2NaHSO3
在吸收过程中,一部分亚硫酸钠氧化为硫酸钠:
2Na2SO3+O2→2Na2SO4
用石灰石再生:
2NaHSO3+CaCO3→Na2SO3+CaSO3+CO2↑+H2O
用石灰再生:
2NaHSO3+Ca(OH)2→Na2SO3+CaSO3↓+2H2O
Na2SO3+Ca(OH)2→2NaOH+CaSO3↓
Na2SO4+Ca(OH)2→2NaOH+CaSO4↓
2CaSO3+O2→2CaSO4↓
双碱法工艺梳程如图7.2所示。该法优点是吸收效率高,可达95%以上;吸收系统不产生沉淀物,没有结垢与堵塞问题。
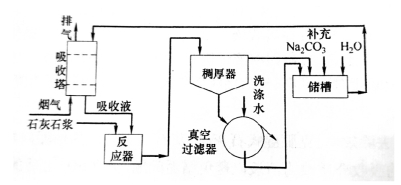
图7.2 钠碱双碱法工艺流程
由于烟气中有氧,部分亚硫酸钠被氧化成硫酸钠,硫酸钠不易再生。因此需要补充Na2CO3或NaOH,钠的补充量约为0.05mol/molSO2。另外,由于Na2SO4的存在降低了石膏质量,这也是双碱法的主要不足之处。
3.喷雾干燥法
喷雾干燥法是20世纪80年代,由美国Joy公司和丹麦Niro Atomizer共同开发的,故又称Joy/Niro法。这种方法是以Ca(OH)2和Na2CO3溶液为吸收剂,经喷雾装置喷入反应器内,同烟气接触而吸收SO2,SO2在与碱性雾滴进行反应的同时也干燥了液滴,水分蒸发,到达反应器出口,形成的生物为干固体粉末连同未曾发生反应的吸收剂干化的颗粒及飞灰经除尘器进行气固的分离,排出尾气。因此该流程在吸收器内反应之后,将在除尘器内继续分离,如图7.3所示。

图7.3 喷淋干燥法工艺流程
喷雾干燥法脱硫效率可达70%~90%。该系统的关键是喷雾装置,通常用的有两种:喷嘴和离心转盘喷雾器。操作方式可以逆流,也可以并流。
喷雾干燥法的主要优点是工艺简单、设备少;运行可靠,生产过程中不会发生结垢和堵塞现象;生成物易处理;只要将排烟温度控制在适宜的范围内,不会产生严重的腐蚀问题;能量消耗低、投资省、运行费用小、耗水量低;对烟气量和SO2浓度适应性较强;净化后的尾气温度较高,不必再加热,可以直接排放。影响SO2去除的因素主要是SO2吸收率和吸收剂利用率随烟气出口温度接近饱和温度的程度而提高,一般喷雾干燥法的操作温度在绝热饱和温度之上11~28k。还需要防止出口烟气接近湿饱和,避免在袋式除尘器中出现凝结问题。
目前喷雾干燥吸收法主要用于低硫煤脱硫操作中。
(二)金属氧化物法
一些金属氧化物如MnO2、ZnO等可以吸收烟气中的SO2。下面以氧化镁法为例简要介绍金属氧化物法脱硫的基本反应及工艺流程。
氧化镁法是以氧化镁浆料吸收烟气中的SO2,生成MgSO2,加热可再生MgO,再生获得高浓度SO2用来生产硫酸和硫黄。氧化镁吸收脱硫的工艺过程包括四部分:烟气预处理、SO2吸收、固体分离与干燥和MgSO3再生。
1.工艺过程中的主要化学反应
(1)烟气预处理
主要用于燃煤系统,主要去除飞灰,防止使循环使用的吸收剂遭受严重污染。烟煤飞灰含有钒和铁等化合物,它们是催化剂,促使下面副反应发生:
MgSO3+½O2→MgSO4
(2)SO2吸收
用氧化镁浆液,即Mg(OH)2做吸收剂,其主反应如下:
Mg(OH)2+SO2+5H2O→MgSO3·6H2O
MgSO3+SO2+H2O→Mg(HSO3)2
Mg(HSO3)2+Mg(OH)2+10H2O→2MgSO3·6H2O
副反应:
Mg(HSO3)2+½O2+6H2O→MgSO4·7H2O+SO2
MgSO3+½O2+7H2O→MgSO4·7H2O
Mg(OH)2+SO3+6H2O→MgSO4·7H2O
(3)干燥过程(https://www.xing528.com)
MgSO3·6H2O→MgSO3+6H2O↑
MgSO4·7H2O→MgSO4+7H2O↑
(4)分解过程
MgSO3→MgO+SO2↑
MgSO4+½C→MgO+SO2↑+½CO2↑
经熔烧干燥后的镁盐可得到氧化镁,同时放出SO2,焙烧炉排气中含有10%的SO2,经过除尘净化,可送至硫酸生产制造单元。焙烧温度对MgO性质影响较大,适宜的焙烧温度是933~1143K。
2.工艺流程与设备
氧化镁脱硫的工艺流程如图7.4所示。

图7.4 氧化镁法工艺流程
该工艺流程主要设备是文丘里吸收装置,常用的是开米科(Chmico)洗涤器,如图7.5所示。开米科洗涤器是一种组合式的文丘里吸收装置。其特点是气液接触好,净化效果高;处理气体量大,单台设备处理能力可达250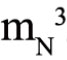 /s;无结垢故障,稳定性好,可长期连续运转。
/s;无结垢故障,稳定性好,可长期连续运转。

图7.5 开米科洗涤器构造示意
但氧化镁法脱硫的缺点是要求预处理必须除尘除氯,大约有8%的MgO流失而产生二次污染。
(三)活性炭吸附法
低浓度SO2除了用前面介绍的吸收法净化之外,也可以采用吸附净化法,常用的吸附剂是活性炭。活性炭吸附SO2,在干燥、无氧条件下主要是物理吸附,当有氧和水蒸气存在时会发生化学吸附。
1.基本原理
烟气通过活性炭床时,SO2、O2和H2O被吸附,然后它们之间在活性炭表面上发生化学反应:
SO2+½O2+(n+1)H2O→H2SO4·nH2O
如果用铜、铁、钴、镍、铬、和铈等金属盐浸渍活性炭,就可以发现:活性炭对SO2的吸附能力提高了,这可能是有催化氧化SO2的作用的缘故。一般来说,活性炭对SO2的吸附容量是40-140g/kg活性炭。
到达吸附平衡时的活性炭可以用水洗再生,得到稀硫酸;也可以用加热再生的方法,这样可得到高浓度的二氧化硫。因为加热过程,碳将沉积在活性炭上硫酸还原成二氧化硫,反应式如下:
2H2SO4+C→2SO2+2H2O+CO2↑
2.工艺流程
活性炭吸附-水洗再生脱硫法又称鲁奇式活性炭吸附法,因为这种方法是由德国鲁奇化学协会和法兰克福的胡特惠逊公司开发的,其工艺流程如图7.6所示。

图7.6 活性炭吸附-水洗再生法工艺流程
烟气首先经文丘里洗涤器除尘并冷却,然后进入一个活性炭吸附器。图7.6中是两个固定活性炭吸附器,一个吸附,另一个再生。平均吸附脱硫效率可达80%。用水冲洗再生得到稀硫酸溶液进入循环液槽,作为文丘里洗涤器的洗涤液。在洗涤过程中,由于一部分水分蒸发而提高了硫酸浓度,可达25%左右。硫酸进一步经过浸没燃烧器、冷却器和过滤器除去杂质,最后可得到65%~70%的硫酸。
该工艺主要优点是工艺简单、运转方便、副反应少、无污水排放、可回收稀硫酸。但也有很多缺点,主要是由于活性炭吸附容量有限,所以需要较大的吸附设备,一次性投资高,吸附剂需要频繁再生。
我国湖北省松木坪电厂已成功地用活性炭吸附-水洗再生法处理低浓度SO2烟气,脱硫率高达90%。
(四)催化转化法
烟气中的SO2可以在催化剂的作用下被氧化为SO3,再转变为硫酸回收利用;也可在催化剂作用下还原为H2S,再用特殊工艺回收硫黄。
下面就分别来讨论催化氧化和催化还原两种方法对SO2的净化原理及工艺流程。
1.催化氧化法脱硫
二氧化硫的催化氧化又可根据反应组分在催化转化过程中的物相分为干式和湿式两种。干式催化氧化是SO2在固体催化剂表面被转化的过程;湿式催化氧化是SO2被吸收液吸收后催化转化的过程。
(1)干式催化氧化法脱硫
有称气相催化法,多用于处理硫酸生产尾气和有色金属烟气制酸。
干式催化氧化法常以V2O5作催化剂,催化氧化SO2使之成为SO3再制酸。也就是说在该法中,SO2是在V2O5催化剂的表面发生氧化反应的:
SO2+½O2→SO3
这是一个放热可逆反应,其平衡关系为:

平衡常数Kp是温度的函数,随温度的升高而减小,温度越低,平衡常数越大,SO2的平衡转化率也越高。当然温度低,反应速度就越缓慢。增加反应时间、增加催化剂用量,而实际转化率也可能不高。
为了使反应进行得快,最终的转化率高,因此在实际的操作中采用了变温措施。在反应初期,因为反应体系还远离平衡状态,为了加速反应,可采用高温操作。而在反应后期,当反应体系已接近平衡状态时,可采用低温操作,使反应向深度发展以获得最终的高转化率。当然对温度的选择要考虑到催化剂的催化活性温度范围。V2O5的活性温度通常为400-600℃,这也是实际生产的操作温度范围。图7.7表达了最适合的温度曲线,根据它们之间的相互关系来确定操作条件。

图7.7 SO2催化转化平衡线及操作线
干式催化氧化法脱硫系统流程如图7.8所示。该系统是比较传统的制酸工艺,复杂而庞大。因为烟气在进入转化器前必须先经过除尘,转化生成的热量可利用锅炉的省煤器和空气加热器输送出来。由于烟气中的SO2含量低,采用一次转化、一次吸收即可达到净化要求。但是所得的产品相对甚少,使用价值不大。因此该法多用于高浓度SO2尾气的净化过程。

图7.8 烟气脱硫的催化氧化流程
(2)湿式催化氧化法脱硫
又称液相催化法,是用含有铁(Fe3+)、锰(Mn2+)等金属离子的稀硫酸溶液(2%~3%)作吸收剂,吸收SO2,再经催化氧化转化为硫酸。因此,转化过程可分为两个步骤:吸收和氧化。
吸收反应:
Fe2(SO4)3+SO2+2H2O→2FeSO4+2H2SO4
氧化反应:
2FeSO4+SO2+O2→Fe2(SO4)3
总反应式可写成:
2SO2+O2+2H2O→2H2SO4
铁离子作催化剂的湿式催化氧化法的工艺流程如图7.9所示,该法又称千代田法。该法要求烟气首先经过除尘器除去灰尘,同时增湿冷却到60℃左右,然后再送入吸收塔用含Fe3+的稀硫酸吸收,废气脱硫后经过除雾器由烟囱排出。由于烟气和吸收液中的氧不足以使SO2充分氧化,多数只转化成H2SO3。因此,含有H2SO3的稀硫酸还需再进入氧化塔。氧化塔内通入压缩空气,使吸收液充分氧化,全部生成H2SO4。当H2SO4浓度达到5%时,导入结晶槽,加入石灰石粉反应生成石膏。

图7.9 千代田法工艺流程
1—除尘塔 2—压滤器 3—吸收塔 4—除雾器 5—氧化塔
6—吸收液槽 7—结晶槽 8—增稠槽 9—离心分离器 10—母夜叉槽
该法工艺简单,运行可靠,无设备堵塞问题,还可获得石膏。但缺点是液气比要求大,一般为40L/m3;由于SO2在稀硫酸中溶解较小,故需要较大的液比,设备也就比较庞大;因稀硫酸液腐蚀性强,需用钛、铝等特殊材料制作,设备投资大。
2.催化还原法脱硫
催化还原法脱硫是用H2S或CO将SO2还原为硫,反应如下:
SO2+2H2S→H2O+3S
SO2+2CO→2CO2+S
该过程可以活性炭为催化剂。由于操作过程中有H2S和CO二次污染问题及催化剂中毒问题尚未得到适宜的解决方法,因此催化还原法处理低浓度SO2气体还未达到实用阶段。对于炼油厂高浓度H2S气体,可用克劳斯装置进行回收单质硫的操作。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




