知识链接
1.EDTA
EDTA(乙二胺四乙酸的简称)是一种重要的配合剂。EDTA 是白色、无臭、无味结晶性粉末,熔点240 °C(分解)。不溶于冷水、醇及一般有机溶剂,微溶于热水,溶于沸水、氢氧化钠、碳酸钠及氨的溶液中。EDTA 用途很广,可用作钙离子配合剂、洗涤剂、血液抗凝剂。生化研究中用作钙螯合剂,消除微量重金属导致的酶催化反应中的抑制作用等。
EDTA 是化学中一种良好的配合剂,它有6 个配位原子,形成的配合物叫作螯合物。EDTA 在配位滴定中经常用到,一般是测定金属离子的含量;在生物应用中,用于排除大部分过渡金属元素离子如铁(Ⅲ)、镍(Ⅱ)、锰(Ⅱ)的干扰;在蛋白质工程及试验中可在不影响蛋白质功能的情况下去除干扰离子。
配合剂EDTA 可以与绝大多数的金属离子形成稳定的配合物,因此EDTA标准溶液是配位滴定中最常用的滴定剂。乙二胺四乙酸(简称EDTA)难溶于水,常温下其溶解度是0.2 g/L,不能用于配制滴定用的标准溶液,故在分析中通常使用其二钠盐配制标准溶液。
标定EDTA 常用的基准物有Zn、ZnO、CaCO3 等,通常选用其中与被测组分相同的物质作为基准物,这样滴定条件一致,可减少误差。
2.水的硬度
水的总硬度指水中钙、镁离子的总量,其中包括碳酸盐硬度和非碳酸盐硬度。硬水不适宜于工业使用,如锅炉里使用了硬水,经过长期烧煮后,能形成锅垢,既浪费资源,又易阻塞管道,造成重大事故。
碳酸盐硬度:通过加热能以碳酸盐形式沉淀下来的钙、镁离子,又叫暂时硬度。
非碳酸盐硬度:加热后不能沉淀下来的那部分钙、镁离子,如钙镁的氯化物、硫酸盐、硝酸盐等,又称永久硬度。
碳酸盐硬度和非碳酸盐硬度之和称为总硬度。水中钙的含量称为钙硬度,水中镁的含量称为镁硬度。
硬度的表示方法:目前尚未统一,我国使用较多的表示方法有两种,一种是将所测得的钙、镁折算成CaO 的质量(单位:mg)表示,单位为mg/L;另一种以度计:以每升水中含10 mg CaO 为1 度来表示。
不同国家的表示方法:
德国度(°d):1 L 水中含有相当于10 mg 的CaO,其硬度即为1 个德国度(1 °d)。这是我国目前最普遍使用的一种水的硬度表示方法。
美国度(mg/L):1 L 水中含有相当于1 mg 的CaCO3,其硬度即为1 个美国度。
法国度(°f):1 L 水中含有相当于10 mg 的CaCO3,其硬度即为1 个法国度(1 °f)。
英国度(°e):0.7 L 水中含有相当于10 mg 的CaCO3,其硬度即为1 个英国度(1 °e)。
安全提示
(1)实验中使用氨试液和氨-氯化铵缓冲溶液,挥发性较强,应保持实验室通风,尽量减少氨吸入量。
(2)按照操作规程进行操作。
(3)配位滴定中,一定注意终点的判断。
(4)实验中多玻璃器皿,实验过程中一定轻拿轻放,谨防摔碎。
(5)按照操作规程进行操作。
(6)滴定过程中,一定注意终点的判断。
任务一 EDTA 溶液的配制与标定(铬黑T 法)
一、实训目的
(1)练习移液管的正确使用;
(2)学习EDTA 标准溶液的配制和标定方法;
(3)熟练掌握配位滴定的原理,了解配位滴定的特点;
(4)进一步熟悉K-B 指示剂颜色的变化及观察。
二、实训原理
乙二胺四乙酸二钠标准溶液主要采用间接法制备,国标规定以氧化锌基准试剂标定。标定以氨-氯化铵缓冲溶液控制pH=10,采用铬黑T(EBT)做指示剂。
![]()
当滴加EDTA 时,溶液中游离的Zn2+首先与EDTA 阴离子进行配位反应
![]()
溶液为酒红色,到达计量点时,稍过量的EDTA 便夺取ZnIn-中的Zn2+,释放出指示剂,呈蓝色,为滴定终点。
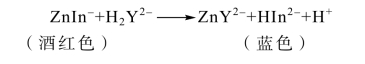
三、实训用品及准备
1.实训仪器
表5-6 EDTA 溶液的配制与标定(铬黑T 法)实训仪器
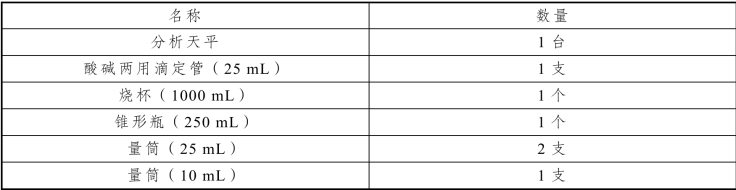
2.实训试剂
表5-7 EDTA 溶液的配制与标定(铬黑T 法)实训试剂
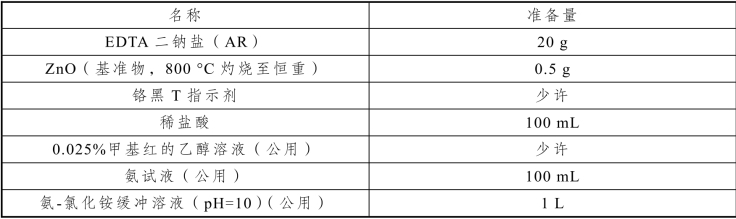
铬黑T 指示剂:铬黑T 与固体NaCl 按1∶100 比例混合,研磨均匀,贮于棕色广口瓶中。
钙指示剂:钙指示剂与固体NaCl 按2∶100 比例混合,研磨均匀,贮于棕色广口瓶中。
NH3·H2O-NH4Cl 缓冲溶液(pH=10):称取20 g NH4Cl 溶于水后,加100 mL 浓氨水,用水稀释至1 L,调节pH 为10。
四、实训内容
1.0.05 mol/L EDTA 标准溶液的配制
称取EDTA 二钠盐19 g 于1000 mL 烧杯中,加适量温蒸馏水溶解后,加蒸馏水稀释至1000 mL,摇匀备用。
2.0.05 mol/L EDTA 溶液浓度的标定
精确称取800 °C 灼烧至恒重的基准物氧化锌0.12 g 于250 mL 锥形瓶中,加稀盐酸25 mL 使之溶解,再加0.025%甲基红的乙醇溶液1 滴,滴加氨试液至显微黄色,再加蒸馏水25 mL 及氨-氯化铵缓冲溶液(pH=10)10 mL,加少量铬黑T 指示剂,用EDTA 滴定至溶液由紫红色变为蓝色,记录EDTA 消耗量。
五、数据记录与处理
表5-8 EDTA 溶液的配制与标定(铬黑T 法)数据记录
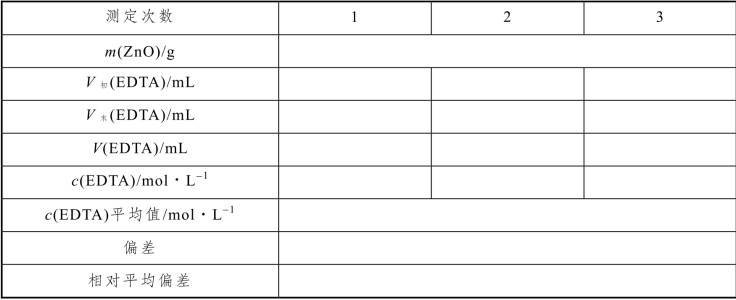
按下式计算EDTA 的物质的量浓度:
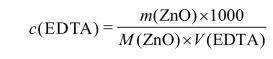
式中 m(ZnO)—— 氧化锌的质量,g;
M(ZnO)—— 氧化锌的摩尔质量,g·mol-1;
V(EDTA)—— EDTA 溶液的体积,mL。
六、注意事项
(1)配位反应进行的速度较慢,故滴定时加入EDTA 溶液的速度不能太快,在室温低时更要注意,尤其在接近终点时,应逐滴加入,并充分摇匀。
(2)实验中指示剂为固体,在水溶液中有溶解过程,因此加入时应注意用量,加入指示剂充分摇匀溶解后,注意观察深浅判断是否足量,同时对于三个平行实验的颜色尽量保持一致。(https://www.xing528.com)
(3)配位滴定中,加入指示剂的量是否适当对于终点的观察十分重要,在实践中不断总结经验,熟练掌握。
(4)测定时如果水温过低,应将水样加热到30~40 °C 再进行测定。
七、实训评估
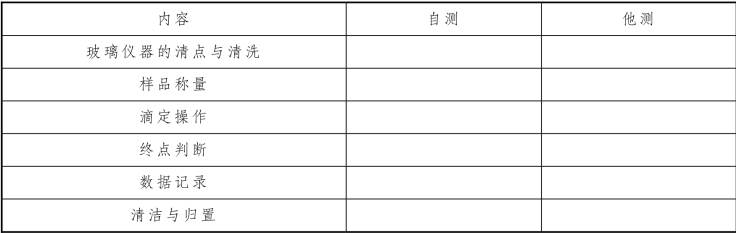
表5-9 EDTA 溶液的配制与标定(铬黑T 法)实训评估
八、拓展练习
(1)试解释以铬黑T 为指示剂的标定实验中的几个现象:
① 滴加氨水至开始出现白色沉淀;② 加入缓冲溶液后沉淀消失;③ 用 EDTA 标准溶液滴定至溶液由酒红色变为纯蓝色。
(2)用铬黑T 指示剂时,为什么要控制pH≈10?
(3)配位滴定法与酸碱滴定法相比,有哪些不同?操作中应注意哪些问题?
(4)配位滴定中为什么加入缓冲溶液?
任务二 天然水中钙、镁含量的测定
一、实训目的
(1)掌握配位滴定法测定Ca2+、Mg2+的原理和水的总硬度的表示方法。
(2)掌握移液管、滴定管的使用和正确操作。
(3)熟悉金属指示剂的变色原理和应用。
二、实训原理
水的总硬度是指水中Ca2+、Mg2+的总量。
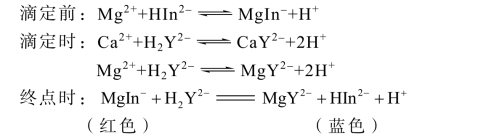
测定时,取一定量水样,调节pH=10,以铬黑T 为指示剂,用EDTA 标准溶液直接滴定水中Ca2+、Mg2+。其反应式为:Ca2+含量测定,先用NaOH 调节pH=12,使Mg2+以Mg(OH)2 沉淀析出,再以钙指示剂指示终点,用EDTA 标准溶液滴定Ca2+。
Mg2+含量是由等体积水样Ca2+、Mg2+总量减去Ca2+含量求得。
三、实训用品及准备
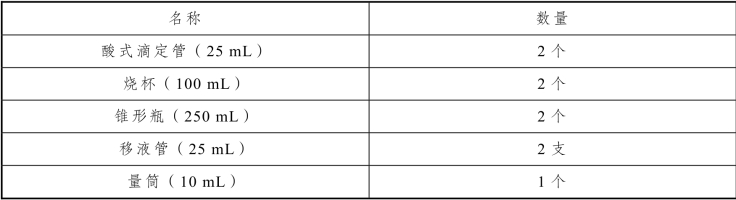
1.实训仪器
表5-10 天然水中钙、镁含量的测定实训仪器
2.实训试剂
表5-11 天然水中钙、镁含量的测定实训试剂

铬黑T 指示剂:铬黑T 与固体NaCl 按1∶100 比例混合,研磨均匀,贮于棕色广口瓶中。
钙指示剂:钙指示剂与固体NaCl 按2∶100 比例混合,研磨均匀,贮于棕色广口瓶中。
NH3·H2O-NH4Cl 缓冲溶液(pH=10):称取20 g NH4Cl 溶于水后,加100 mL 浓氨水,用水稀释至1 L,调节pH 为10。
四、实训内容
1.总硬度的测定
用移液管移取水样50 mL 于250 mL 锥形瓶中,加pH=10 的NH3·H2O-NH4Cl 缓冲溶液5 mL、铬黑T 指示剂少许,充分摇匀。在充分摇动下,用EDTA 标准溶液滴定,溶液由酒红色变为蓝色即为终点,记录EDTA 标准溶液的体积V1。平行测定3 次。
2.钙含量的测定
用移液管移取水样50 mL 于250 mL 锥形瓶中,加入6 mol/L NaOH 溶液2 mL,摇匀,加钙指示剂少许,溶液为紫红色,在充分摇动下用EDTA 标准溶液滴定,当溶液变为蓝色即为终点,记下EDTA 标准溶液的体积V2。平行测定3 次。
五、数据记录与处理
表5-12 天然水中钙、镁含量的测定数据记录
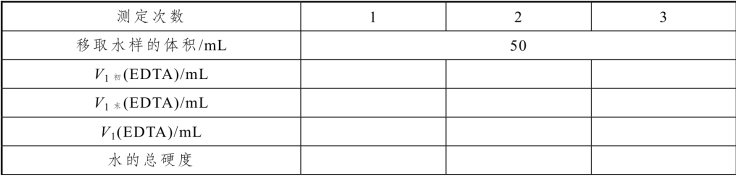
续表
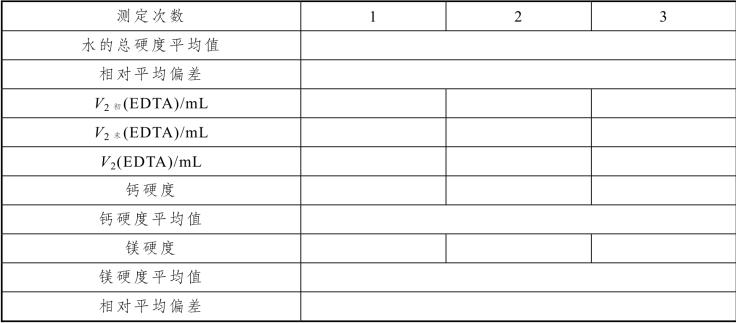
计算公式:

式中 c(EDTA)—— EDTA 的物质的量浓度,mol/L;
V1(EDTA)—— 测定水的总硬度时消耗EDTA 的体积,mL;
V2(EDTA)—— 滴定Ca2+含量所消耗的EDTA 的体积,mL;
M(CaO)—— CaO 的摩尔质量,g/mol;
M(Ca)—— Ca 的摩尔质量,g/mol;
M(Mg)—— Mg 的摩尔质量,g/mol。
六、注意事项
(1)实验中所用指示剂为固体,在水溶液中有溶解过程,加入时应注意用量,依据少量多次加入原则,每加入一次充分摇匀溶解后观察颜色深浅判断是否足量。平行实验溶液颜色尽量保持一致。
(2)当水样中Mg2+含量较低时,可在标定前加入适量的Mg2+或在缓冲溶液中加入一定量的Mg-EDTA 盐,来提高显色灵敏度。
(3)滴定至接近终点时,要慢滴多摇,以免超过终点或返红。
![]()
七、实训评估
表5-13 天然水中钙、镁含量的测定实训评估

八、拓展练习
(1)什么叫水的硬度,水的硬度有哪几种表示方法?
(2)软硬水的区分标准是什么?
(3)为什么滴定Ca2+、Mg2+总量时要控制pH≈10,而滴定Ca2+分量时要控制pH 为12~13?若pH>13 时测Ca2+对结果有何影响?
(4)测定水样中若有少量的Fe3+、Cu2+,如何消除影响?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




