该工艺使用固体状碳酸氢铵作为脱硫剂。固体碳酸氢铵比液氨、氨水、氨气更不易挥发而造成氨气臭味污染。固体亚硫酸铵工艺流程如图4-23所示。
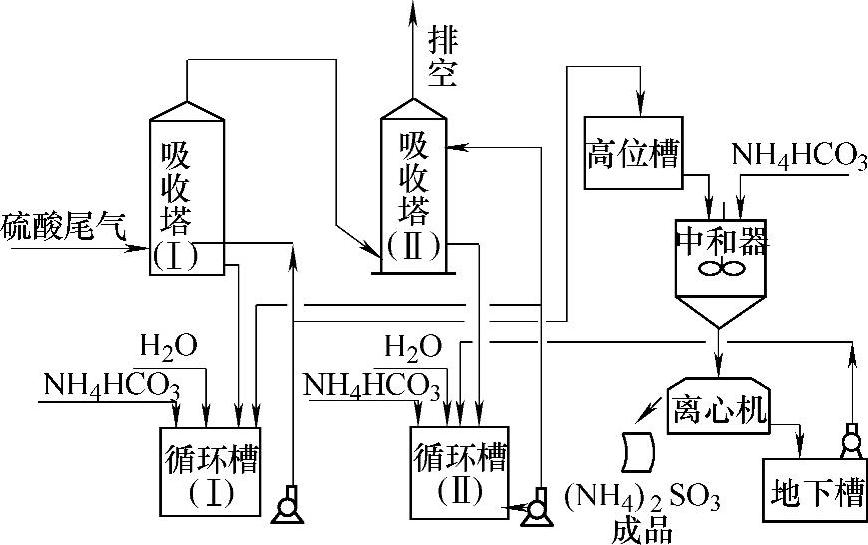
图4-23 固体亚硫酸铵脱硫工艺流程图
制取固体亚硫酸铵的工艺流程可分为吸收、中和、分离三部分。为了制取固体亚硫酸铵,吸收SO2后引出去中和的吸收液必须是高浓度NH4HSO3溶液,吸收液S/C值应维持高值,以提高固体亚硫酸铵结晶的产率。要使吸收SO2效率高,吸收液S/C值应维持低值,即碱度较高,因而吸收系统采用两段吸收法。
固体亚硫酸铵法化学反应式:
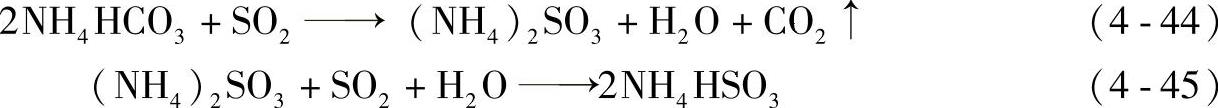
吸收过程实际上以反应式(4-45)为主,而NH4HCO3在吸收过程中只是补入吸收系统,使部分NH4HSO3再生为(NH4)2SO3,以此保持脱硫吸收液碱度基本稳定(即S/C不变)
因烟气中含有氧,就会发生以下副反应:

所以吸收液中含有少量硫酸铵。
吸收SO2的脱硫液中含有NH4HSO3的组分,呈酸性,加固体碳酸氢铵中和后,使NH4HSO3转变为(NH4)2SO3:
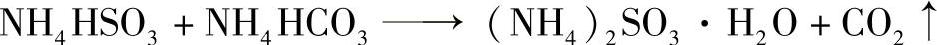
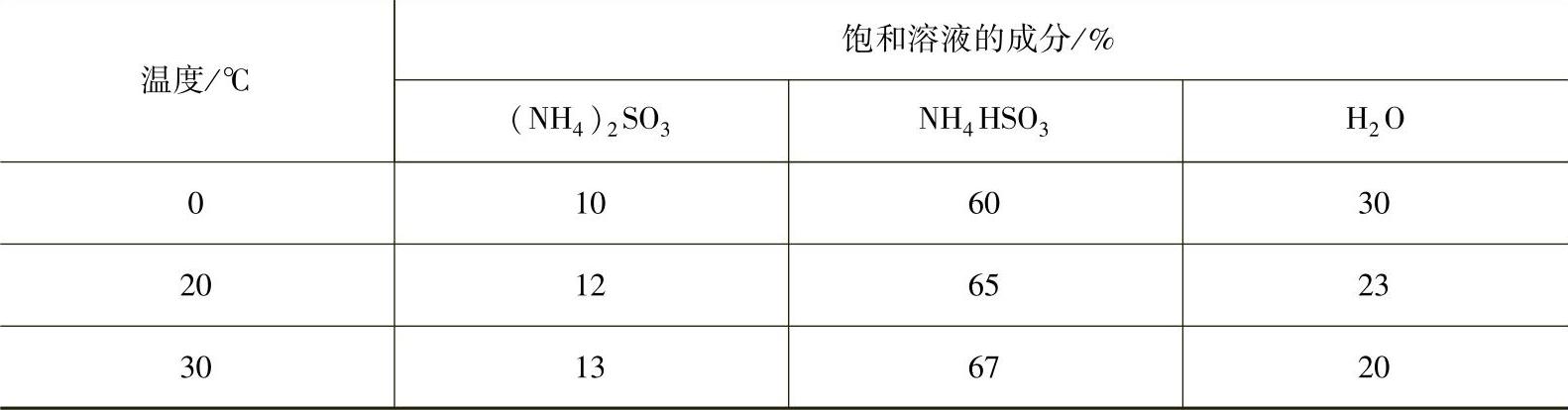
此化学反应为吸热反应,溶液温度不经冷却即可降到0℃左右。由于(NH4)2SO3比NH4HSO3在水中的溶解度小(见表4-6),因此生成的(NH4)2SO3·H2O过饱和而从溶液中结晶析出。用离心机分离此悬浮液,便可制得固体亚硫酸铵结晶体。
表4-6 (NH4)2SO3-NH4HSO3-H2O系统内的溶解度
(1)吸收 含SO2的烟气依次经过两个串联的吸收塔。在第一吸收塔中,吸收SO2的吸收液应尽可能维持较高浓度和尽量提高吸收液的S/C值,以便生成较多的NH4HSO3,并不断导出部分溶液送至中和工序,以制取固体亚硫酸铵。一般可控制吸收液的总亚盐含量为700g/L。碱度为10滴度左右(S/C为0.88~0.9),折算到pH值为5.36~5.28。
第二吸收塔的吸收液则应维持较高的碱度(S/C值低)和较低浓度,以保证有较高的SO2去除率,使排烟中SO2浓度达到环保排放标准,同时不断引出部分吸收溶液串入第一吸收塔。吸收液总亚硫酸盐含量应控制在350g/L左右,碱度控制在13~15滴度,以满足系统串液时的水平衡,同时降低氨的消耗。为保持各塔循环液的碱度不变,分别在各塔循环槽中加入NH4HCO3和水。
(2)中和 由第一吸收塔引出的高浓度NH4HSO3溶液,在中和器内与加入的固体碳酸氢铵经搅拌进行反应。NH4HSO3转变为(NH4)2SO3,由于过饱和而有大量结晶析出,溶液呈黏稠悬浮状,终温可达0℃左右。
(3)分离 由中和器底部引出的含(NH4)2SO3·H2O晶体的悬浮液进入离心机,分离出固体亚硫酸铵作为产品,滤液进入母液储槽由泵送入第二吸收塔的循环槽中,继续循环吸收SO2。
(4)副反应及处理 吸收液吸收SO2的过程中,由于烟气中有较多的氧,会把(NH4)2SO3氧化成(NH4)2SO4。氧化率与吸收塔型式和操作条件有关,一般可达5%~14%。当循环吸收液中(NH4)2SO4含量积累到一定浓度时,如果不及时除去,不仅降低SO2吸收率,而且硫酸铵会从溶液中结晶析出而堵塞设备,所以必须抑制亚硫酸铵氧化。通常可在吸收液巾加入阻氧化剂,如对苯二胺、对苯二酚等。加入阻氧剂,使发生氧化的量大为减少,但仍无法避免吸收液中硫酸铵的积累上升。可采用7%~8%SO2气体处理吸收液,使吸收液转变成NH4HSO3,饱和溶液。由于溶解度相差较大,所以吸收液中(NH4)2SO4会结晶出来,可从吸收液中除去。
亚硫酸铵结晶在空气巾容易氧化。为了防止潮湿的亚硫酸铵氧化,应把亚硫酸铵干燥制成无水亚硫酸铵。(https://www.xing528.com)
亚硫酸铵可用于制浆造纸,也可用于感光材料、日用化工染料中问体等。
为了控制脱硫后烟气中的氨含量,一般应控制好吸收液的碱度,即控制好吸收液的pH值,使进入吸收塔的氨全部快速吸收SO2,生成(NH4)2S03和NH4HSO3。这就要求选用高效吸收塔,一般可用筛板塔或泡沫塔等。
特别要注意的是氨吸收法与其他碱类的吸收不同,(NH4)2SO3-NH4HSO3水溶液的阳离子和阴离子皆有挥发性。S/C值小时,平衡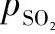 分压小,即SO2的吸收率高,但同时平衡
分压小,即SO2的吸收率高,但同时平衡 的分压高,即随脱硫炯气排空的氨量也多。工业上所用的吸收液的组成需兼顾SO2和NH3的分压(表示NH3的含量),因而发展两段法或多段法吸收。
的分压高,即随脱硫炯气排空的氨量也多。工业上所用的吸收液的组成需兼顾SO2和NH3的分压(表示NH3的含量),因而发展两段法或多段法吸收。
图4-24所示为南京化学·一业集团有限公司磷肥厂的实测数据。当控制(NH4)2SO3/NH4HSO3为0.3(即S/C为0.85)时,则吸收率可达92070-94%,排烟中氨损失为0.1~0.2g/Nm3。
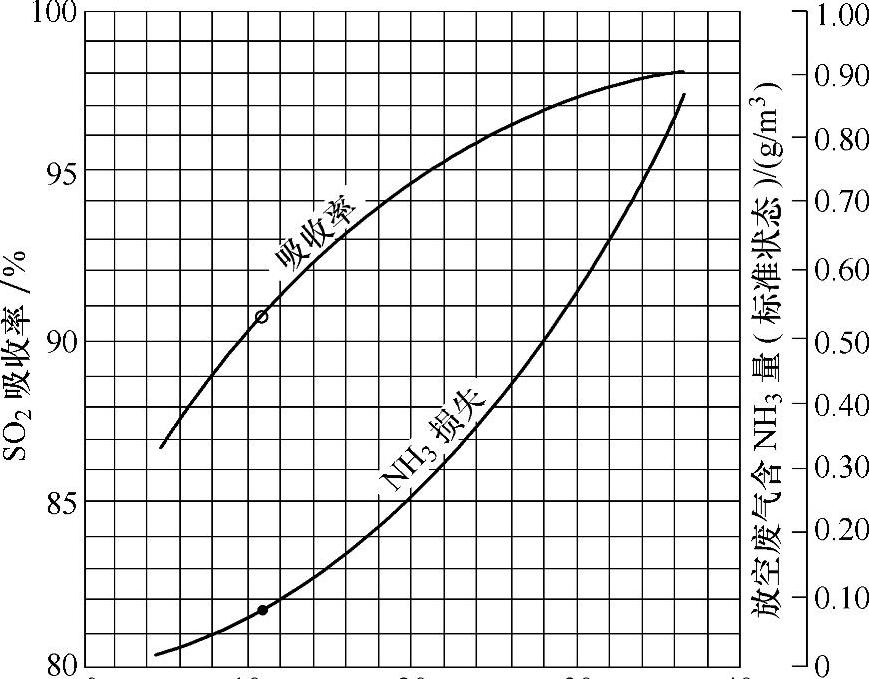
图4-24 吸收液碱度与SO2吸收率及NH3损失关系
pH值对(NH4)2SO3-NH4HSO3水溶液的影响,俄罗斯学者提出了S/C为0.5~0.95时,pH值经验公式:
pH=-4.0(S/C)+8.88
pH-S/C曲线如图4-25所示。
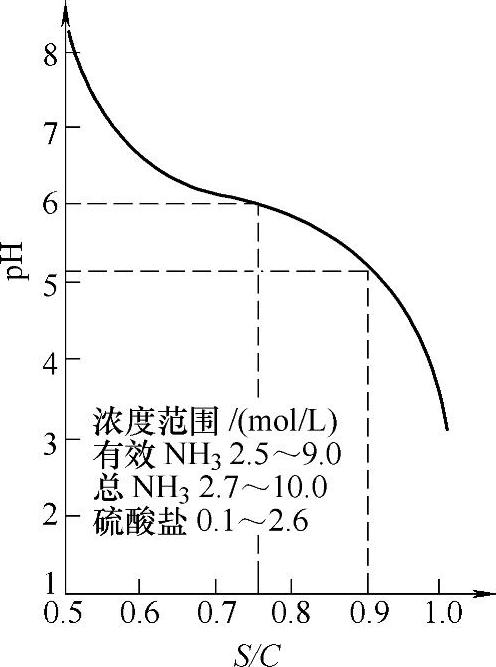
图4-25 pH-S/C曲线
图4-26所示为(NH4)2SO3-NH4HSO3水溶液中,根据pH值、温度、S/C表示出的NH3分压值。
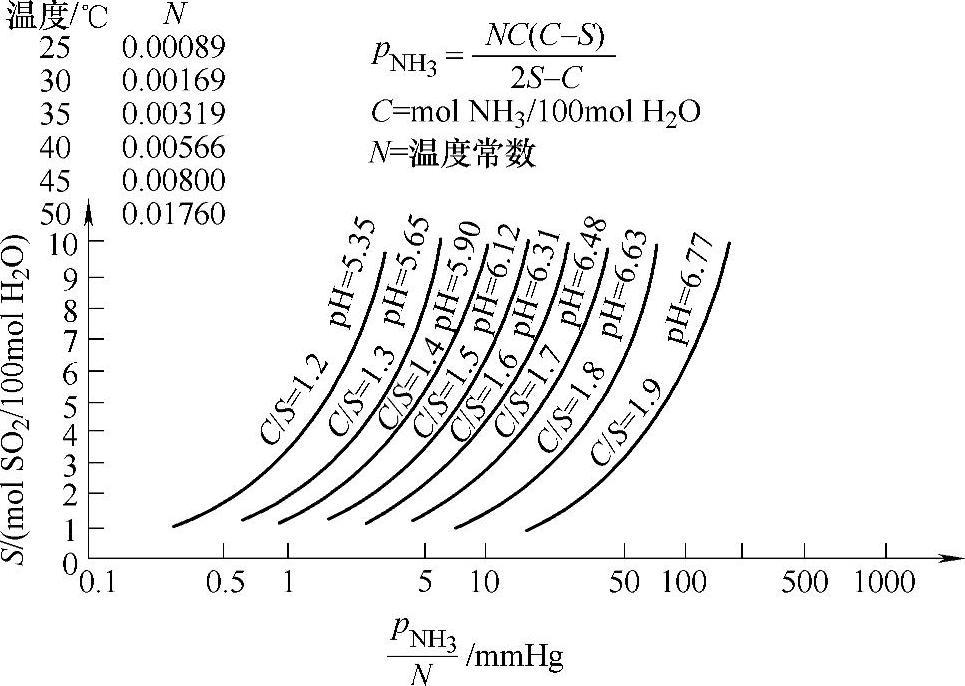
图4-26 pH、S/C、T对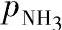 的曲线图
的曲线图
图4-27所示为(NH4)2SO3-NH4HSO3水溶液中,根据pH值、温度、S/C表示出的SO2分压值。
在氨法脱硫设计时,我们可以利用图4-24估算出SO2吸收率与吸收液碱度(滴度)和(NH4)2SO3/NH4HSO3分子比值的关系,以及与氨气损失的关系。利用图4-25,可以估计出pH值与S/C的关系,以及吸收液中(NH4)2SO3和NH4HSO3的组成。
滴度也是表示溶液碱度的单位。1个滴度的碱度表示铵盐溶液中的(NH4)2SO3含5.8g/L。
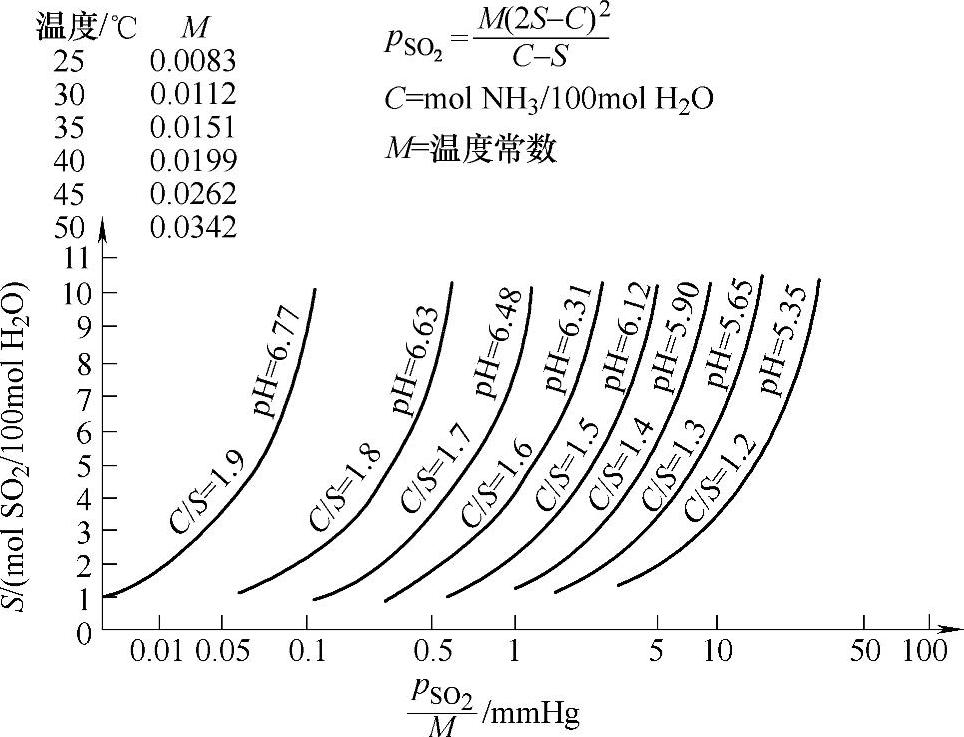
图4-27 pH、S/C、T对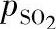 的曲线图
的曲线图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




