化学处理法是通过向被污染的水体中投加化学药剂,利用化学反应来分离和回收污水中的胶体物质和溶解性物质等,从而回收其中的有用物质,降低污水中的酸碱度、去除金属离子、氧化某些有机物等。这种处理方法可使污染物质和水分离,也能够改变污染物质的性质,因此可以达到比简单的物理处理方法更高的净化程度。化学法可以通过化学反应方程式来计算所需投加的药量,不容易造成浪费,而且操作技术容易实现,水量少时可以进行简单的手工操作,水量大时可以采用大型设备进行自动化操作。化学法包括化学中和法、化学沉淀法、化学混凝法、氧化还原法、铁氧体法等(见表3-9)。
由于化学处理法常需要采用化学药剂或材料,所以处理费用较高,运行管理也较为严格。通常,化学处理还需要与一定的物理处理法联合使用。
表3-9 化学处理方法的适用范围及处理对象

3.2.2.1 化学中和法
在废水中加入酸或碱进行中和反应,调节废水的酸碱度(pH值),使其呈中性或接近于中性或适宜于下一步处理的pH值范围。含酸废水和含碱废水是两种重要的工业废液。一般而言,酸含量(质量分数)大于3%~5%、碱含量大于1%~3%的高浓度废水称为废酸液和废碱液,这类废液首先要考虑采用特殊的方法回收其中的酸和碱。酸含量小于3%~5%或碱含量小于1%~3%的酸性废水与碱性废水,回收价值不大,常采用中和处理方法,使其pH值达到排放废水的标准。冶金生产过程中产生的废水,可能含有酸也可能含有碱,大部分酸性废水中都含有必须除去的重金属盐。为了防止净化设备腐蚀,避免破坏水和生物池中的生化过程,以及防止从废水中沉淀出重金属盐等,无论酸性还是碱性废水都要进行中和处理。最典型的反应是氢离子和氢氧根离子之间的反应,生成难解离的水。
选择中和方法时应考虑以下因素:
(1)含酸或含碱废水所含酸类或碱类的性质、浓度、水量及其变化规律。
(2)首先应寻找能就地取材的酸性或碱性废料,并尽可能地加以利用。
(3)本地区中和药剂或材料(如石灰、石灰石等)的供应情况。
(4)接纳废水的水体性质和城市下水管道能容纳废水的条件。
A 中和方法
中和方法有:
(1)酸性废水与碱性废水混合中和。酸、碱废水相互中和的方法是最经济的方法之一。一般来说,含酸废水和含碱废水的排放方式是不同的,酸性废水在一天之内均匀排放,浓度变化不大;而碱性废水常常是根据碱性溶液排放方式的不同间歇地进行的,因此排放碱性溶液时应设置贮槽以使其均匀地进入中和反应罐,与酸性废水进行中和。
(2)试剂中和。用试剂中和酸性废水的方法也很普遍,至于选择什么样的试剂中和酸性废水则完全取决于酸的种类、浓度和中和反应后生成的盐的浓度。最常用的是熟石灰和石灰乳,往往被称为石灰处理法。石灰处理(中和)过程中可以同时把锌、铅、镉、铜、铬等金属转入沉淀,有时中和反应常采用浆状的碳酸钙或碳酸镁。
上述试剂廉价易得,但其缺点主要有:中和前必须设置配匀装置,难以按被中和溶液的pH值调节试剂,操作管理比较复杂。
(3)中和材料过滤。盐酸、硝酸废水及质量浓度不超过1.5g/L的硫酸废水均可用连续式过滤器进行中和。可以采用中和材料(如白云石、石膏、菱镁矿石、白垩和大理石等)作为过滤器的填料,填料粒度为3~8cm。
这种过滤器只能在酸性废水中不含可溶性金属盐的条件下使用,因为当pH值大于7时,这些金属将生成难溶化合物沉淀下来,可能完全堵塞过滤器的孔隙。在实际中,很少采用中和过滤材料中和处理废水。
对于酸性污水而言,主要有酸性污水与碱性污水相互中和、药剂中和以及过滤中和三种。而碱性污水主要有与酸性污水相互中和和药剂中和两种。其中酸性污水的数量和危害要比碱性污水大得多。酸性污水的药剂中和法中主要用的药剂有石灰、苛性钠、碳酸钠、石灰石、电石渣等,最常用的是石灰(CaO)。药剂的选用要考虑药剂的供应情况、溶解性、反应速度、成本及二次污染等因素。过滤中和法是选择将碱性滤料填充成一定形式的滤床,酸性污水流过滤床的时候即被中和。
B 中和法设备
关于中和法设备,分别按普通过滤中和和升流膨胀式过滤中和予以介绍。
(1)普通过滤中和设备。普通中和滤池为固定床,一般采用石灰石作滤料。水的流向有平流和竖流两种,目前多用竖流,其中又分升流式和降流式两种,见图3-6。普通中和滤池的滤料粒径不宜过大,一般为30~50mm,不得混有粉料杂质,当水含有可能堵塞滤料的物质时,应进行预处理。过滤速度一般不大于5m/h,接触时间不少于10min,滤床厚度一般为1~1.5m。

图3-6 普通中和滤池
(a)升流式;(b)降流式
(2)升流膨胀式过滤中和设备。废水由底部进入池中,升流式膨胀床的过滤中和采用0.5~3mm小粒径的滤料。当滤料横截面固定不变、滤速为恒速时,可使滤料相互摩擦不易结垢,垢屑和CO2易于排走,不致造成滤床堵塞。图3-7为恒速升流膨胀中和滤池(滤料一般为石灰石)示意图。
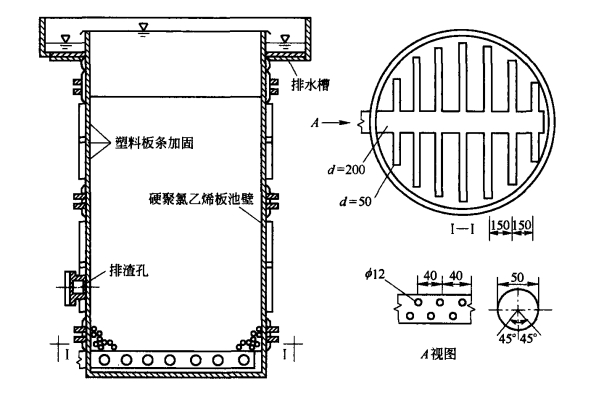
图3-7 恒滤速升流膨胀中和滤池
3.2.2.2 化学沉淀法
化学沉淀法是将要去除的离子变为难溶的、难解离的化合物的过程。化学沉淀法的处理对象主要是重金属离子(铜、镍、汞、铬、锌、铁、铅、锡)、两性元素(砷、硼)、碱土金属(钙、镁)及某些非金属元素(硫、氟等)。主要的化学沉淀工艺有:
(1)投加化学药剂,生成难溶的化学物质,使污染物以难溶沉淀的形式从液相中分离析出;
(2)通过凝聚、沉降、浮选、过滤、吸附等方法将沉淀从溶液中分离出来。
为了以沉淀的形式去除水中杂质,必须根据所生成化合物的溶度积选择试剂。利用某些生成化合物溶度积较小的沉淀剂,可以提高水的净化程度。根据每种沉淀化合物的溶度积常数,分析检测该物质在废水中的浓度,投加该物质于待处理的废水中,根据浓度求出其离子积。比较离子积和溶度积,如果:
(1)离子积小于溶度积,则固体物继续溶解,溶液没有达到饱和;
(2)离子积等于溶度积,溶液刚好饱和,物质的解离达到动态平衡;
(3)离子积大于溶度积,溶液过饱和,有沉淀物生成。
通常在物质的离子积大于溶度积的沉淀条件下,为了快速地形成沉淀,需要往废水中投加絮凝剂。常用的絮凝剂有:
(1)阳离子型的絮凝剂,如聚合氯化铝(PAC)、聚合硫酸铝(PAS)等;
(2)阴离子型的絮凝剂,如聚合硅酸(PS)、活化硅酸(AS)等;
(3)无机复合型的絮凝剂,如聚合氯化铝铁(PAFS)、聚硅酸硫酸铁(PFSS)等;
(4)有机高分子絮凝剂,应用最多的是聚丙烯酰胺(PAM);
(5)生物絮凝剂。
有机高分子絮凝剂同无机高分子絮凝剂相比,具有用量少、生成污泥量少、絮凝速度快等优点,而且受共存盐类、pH值、温度的影响较小。聚丙烯酰胺分为三种:阳离子型、阴离子型和非离子型。
生物絮凝剂是近年来研究开发的新型絮凝剂产品,优点主要有:易于固液分离,容易被微生物降解,形成的沉淀物较少,无毒害作用,无二次污染等。
在实际废水处理工艺中,为了提高混凝的效果,往往还要再添加助凝剂,通常为酸碱类、矾花类、氧化剂类的助凝剂。加入助凝剂的作用主要是提高絮凝体颗粒之间的碰撞效率,从而加速絮凝体的形成。其作用机理主要表现在以下几个方面:
(1)增加颗粒浓度,如加入矾花类助凝剂;(https://www.xing528.com)
(2)增加颗粒体积,如加入高分子絮凝剂可以通过强化搭桥作用来增加絮凝体体积;
(3)增加颗粒密度,水玻璃、铁盐助凝剂等具有这种作用;
(4)增加颗粒之间的碰撞次数。
3.2.2.3 化学混凝法
各种污水都是以水为分散介质的分散体系。根据分散粒度的不同,污水可分为三类:分散粒度在0.1~1nm间的称为真溶液;分散粒度在1~100nm之间的称为胶体溶液;分散粒度大于100nm的称为悬浮液,可以通过沉淀或过滤去除。部分胶体溶液一般用混凝法来处理。
混凝就是在污水中预先加化学试剂(混凝剂)来破坏胶体的稳定性,使污水中的胶体和细小悬浮物由于碰撞或聚合,搭接而形成可分离的絮凝体,再用下沉或上浮法分离去除的过程。混凝可降低废水的浊度、色度,除去多种高分子物质、有机物、某些重金属毒物和放射性物质等,因此在废水处理中得到广泛应用。
混凝分为凝聚和絮凝两种过程,凝聚是瞬时的,絮凝则需要一定的时间让絮体长大。
混凝法中必要的试剂就是混凝剂。混凝剂可分为凝聚剂和絮凝剂,低分子电解质为混凝剂,高分子药剂为絮凝剂,两者统称为混凝剂。用于水处理的混凝剂要求混凝效果好,对人体健康无害,价廉易得,使用方便。目前常用的混凝剂按化学组成有无机盐类(主要是铁系和铝系如三氯化铁、硫酸亚铁、硫酸铝聚合氯化铝等)和有机高分子类(可分为阳离子型、阴离子型、非离子型)。
化学混凝法主要用于处理含大量悬浮物的废水。自然沉降的方法处理大量细小的悬浮物是困难的,因此必须借助于混凝剂,采用混凝沉淀的方法实现对悬浮物的去除。
混凝机理涉及水中杂质成分和浓度、水温、水的pH值、碱度、混凝剂性能及其投加量、混凝过程中的混凝条件等。一般认为在混凝过程中起主要作用的混凝机理有双电层作用机理、吸附架桥作用机理和沉淀物的卷扫作用机理等。
对于不同的水质条件、反应条件及混凝剂类型,上述几种混凝机理发挥作用的程度不同。对于高分子混凝剂特别是有机高分子混凝剂,吸附架桥机理起主要作用;对于硫酸铝等金属盐混凝剂,同时具有吸附架桥和压缩双电层作用,当混凝剂投加量很多时还具有卷扫作用。
目前应用于废水处理的混凝剂种类较多,归纳起来主要有金属类混凝剂和高分子类混凝剂。金属类混凝剂中常用的为铝盐和铁盐,铝盐主要有硫酸铝和明矾两种;铁盐主要有硫酸亚铁、硫酸铁和三氯化铁。当单用混凝剂不能取得良好效果时,需要投加助凝剂以提高混凝效果,常用的助凝剂也大体上分为两类:改善絮凝体结构的高分子助凝剂,如聚丙烯酰胺、活化硅酸等;调节和改善混凝条件的药剂,如石灰等。
影响混凝效果的因素错综复杂,包括水温、水质、水力条件、混凝剂投加量等。
(1)水温。水温对混凝效果有明显的影响。低温条件下,金属混凝剂水解困难,导致絮凝体的形成非常缓慢,而且形成的絮凝体结构松散,颗粒细小、沉降性能差,同时较低的水温使水的黏度大、剪切力增强,成长的絮凝体容易破碎,水中杂质微粒的布朗运动强度减弱,不利于脱稳胶粒相互凝聚。
(2)pH值的影响。一般来说,pH值对金属类混凝剂的影响大于有机高分子混凝剂,有机高分子混凝剂的混凝效果受pH值的影响相对较小。如硫酸铝的最佳pH值范围为6.5~7.5,三价铁盐的最佳pH值范围为6.0~8.4,二价铁盐的最佳pH值范围为8.1~9.6,而有机高分子混凝剂没有严格的pH值限制。
(3)水力条件。水的混凝过程包括混合过程和絮凝过程。第一阶段混合过程是将被处理的水与混凝药剂进行混合掺混,最终使水中细小颗粒和胶体物质迅速脱稳。因水中杂质颗粒尺寸微小,需要剧烈搅拌,使药剂迅速均匀地扩散于水中。一般情况下,混合过程要求在10~30s内完成。第二阶段絮凝过程是使混合后水中脱稳的细小悬浮颗粒和胶体物质相互碰撞聚合逐渐成长为大而密实的絮凝体(矾花)。絮凝阶段主要采用水力絮凝池。
(4)混凝剂投加量和投配方法。混凝剂投药量是混凝处理的重要环节,一般通过混凝沉降实验来确定。混凝剂投配方法主要有干投法和湿投法,湿投法因其投药均匀稳定、节约药剂、混凝效果好而被普遍应用。
含大量悬浮物的废水经过混凝剂的混合和絮凝过程后,再通过沉淀、过滤等工序以实现对悬浮物质的去除。
3.2.2.4 氧化还原法
氧化还原法属于化学处理方法,是将废水中有害的溶解性污染物质在氧化还原反应的过程中被氧化或被还原,转化为无毒或微毒的新物质或转化为可以从污水中分离出来的气体或固体,从而使水得到净化处理。氧化还原法是转化污水中污染物的有效的方法。
在选择药剂和方法时要遵循以下原则:
(1)处理效果好,反应产物无毒或无害,不需要进行二次处理。
(2)处理费用合理,所需药剂和材料容易得到。
(3)操作性好,在常温和较宽的pH值范围内具有较快的反应速度;当负荷变化后,在调整操作参数后,可维持稳定的处理效果。
(4)与前后处理工序的目标一致,搭配方便。
化学氧化还原法的运行费用较高,因此目前的化学氧化还原法仅用于饮用水的处理、特种工业用水的处理、有毒工业污水处理和以回收为目的的污水深度处理等情况。
药剂氧化法是利用氧化剂,将废水中的有毒有害物质氧化为无毒或低毒物质,主要用来处理废水中的还原性离子CN-、S2-、Fe2+、Mn2+等,还可以氧化处理有机物质及致病微生物等。常用的氧化剂药剂有Cl2、O3、O2、Cl-等。
利用氯气及其化合物净化废水去除氰化物、硫化氢、硫氢化物、甲基硫醇等有毒有害物质是目前普遍使用的氧化还原法。例如处理含CN-废水的方法是将CN-转变成无毒的CNO-,再将CNO-水解成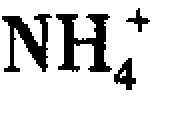 和
和 :
:
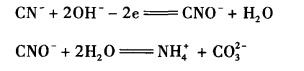
还可以将有毒氰化物转变为无毒的络合物或沉淀,然后通过沉降和过滤等方法将它们从废水中除去。
当向含氰废水中通入氯气时,氯气水解生成次氯酸和盐酸:
![]()
在强酸介质中反应平衡向左移动,水中会有氯分子存在;当pH值大于4时,水中不会有氯分子存在。用氯气氧化氰化物只能在碱性介质中进行(pH值不小于9~10):
![]()
生成的氰酸根可再氧化到单质氮和二氧化碳:
![]()
当pH值降低时,氰化物可直接进行氯化反应,生成有毒的氯化氰:
![]()
比较可靠和经济的方法是在pH值为10~11的碱性介质中采用次氯酸盐氧化氰化物。如漂白粉、次氯酸钙和次氯酸钠都可作为含次氯酸根的试剂。在所处理的废液中发生如下反应:
![]()
反应在1~3min内完成,生成的氰酸根不断地水解。对于以氯气及其化合物作为氧化剂的废水处理工艺与加入水中的氯化物形态有关。如果是用气态氯处理,则氧化过程是在吸收塔内进行;如果氯化剂是一种溶液,则一般是加到混合器中,然后再送进接触器,在接触器中保证与欲处理的废水有一定的混合效率和接触时间。
当所投加的药剂作为还原剂,将废水中的有毒有害物质还原为无毒或低毒物质的一种处理方法称为药剂还原法,主要是用于处理废水中的Cr6+、Cd2+、Hg2+等氧化性重金属离子。常用的还原剂有:气态,SO2;液态,水合肼;固态,硫酸亚铁、亚硫酸氢钠、硫代硫酸钠及金属铁、锌、铜、锰等。
3.2.2.5 铁氧体法
水中各种离子形成不溶性的铁氧体晶粒而沉淀析出的方法称为铁氧体沉淀法。铁氧体是指一类具有一定晶体结构的复合氧化物,它不溶于酸、碱、盐溶液,也不溶于水。铁氧体的通式为![]() 但尖晶石型铁氧体最为人们所熟悉,它的化学组成可用通式BO·A2O3表示。其中B代表二价金属,如Fe、Mg、Zn、Mn、Co、Ni、Ca、Cu、Hg、Bi、Sn等;A代表三价金属,如Fe、Al、Cr、Mn、V、Co、Bi及Ga、As等。许多铁氧体中的A或B可能更复杂一些,由一种以上的金属组成。由于阳离子的种类及数量不同,因而铁氧体有上百种之多。铁氧体有天然矿物和人造产品两大类,磁铁矿(其主要成分为Fe3O4或FeO·Fe2O3)就是一种天然的尖晶石型铁氧体。
但尖晶石型铁氧体最为人们所熟悉,它的化学组成可用通式BO·A2O3表示。其中B代表二价金属,如Fe、Mg、Zn、Mn、Co、Ni、Ca、Cu、Hg、Bi、Sn等;A代表三价金属,如Fe、Al、Cr、Mn、V、Co、Bi及Ga、As等。许多铁氧体中的A或B可能更复杂一些,由一种以上的金属组成。由于阳离子的种类及数量不同,因而铁氧体有上百种之多。铁氧体有天然矿物和人造产品两大类,磁铁矿(其主要成分为Fe3O4或FeO·Fe2O3)就是一种天然的尖晶石型铁氧体。
铁氧体沉淀法的优点是:一次能脱除废水中的多种金属离子,对铬、铁、砷、铅、锌、镉、汞、铜、锰等金属离子均有效果,设备简单,操作方便,沉淀易于分离,出水水质好。但是,消耗一定数量碱,硫酸亚铁用量较大,加热能耗高,出水中的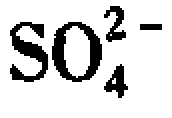 含量高。
含量高。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




