热学研究的是一切与热现象有关的问题,其研究对象可以是固体、液体或者气体,这些大量微观粒子(原子、分子)组成的宏观物体,称为热力学系统,简称系统.与系统发生相互作用的外部环境物质称为外界.按照系统与外界的交换特点,可将系统分为孤立系统、封闭系统和开放系统.如果一个热力学系统与外界不发生任何物质和能量的交换,则该系统被称为孤立系统.如果一个热力学系统与外界只有能量交换而无物质交换,则该系统被称为封闭系统.如果一个热力学系统与外界同时有能量和物质交换,则称为开放系统.
按照系统所处状态可将系统分为平衡态系统和非平衡态系统.人们在实践中发现,一个不受外界影响的系统,即孤立系统,在经过足够长的时间后,最终总会达到宏观性质不随时间变化且处处均匀一致的状态,这种状态称为平衡态.平衡态是系统状态的一种特殊情况,在此状态下系统化同时满足热学平衡条件、力学平衡条件和化学平衡条件。而不满足上述条件的系统状态称为非平衡态.比如,有一密闭容器,中间用一隔板隔开,将其分成A、B两室,其中A 室充满某种气体,B 室为真空室,如图7.1(a)所示,最初A 室气体处在平衡态,其宏观性质不随时间变化,然后将隔板抽去,A 室气体向B 室扩散.由于气体在扩散过程中,气体体积、压强不断变化,因此过程中的每一中间态都是非平衡态.随着时间的推移,气体充满整个容器,扩散停止,此时系统的宏观性质不再随时间而变化,系统达到新的平衡态,如图7.1(b)所示.
需注意:如果系统与外界有能量交换,即使系统的宏观性质不随时间变化,也不能断定系统是否处于平衡态.例如,将铁棒的一端与高温热源相接触,另一端与低温热源相接触,在经过足够长的时间后,铁棒上每一点的宏观性质不会随时间变化,但由于铁棒不是孤立系统,要受到外界条件的影响,因此这不是平衡态,而是一种稳定态.
平衡态是一理想概念,是外界条件变化很慢时的一种近似。因为任何一个系统不可能不受到外界的影响.一个实际系统处于平衡态时需要满足:
(1)系统与外界没有物质交换,且其能量交换可以略去不计,则可以认为系统不受外界影响;
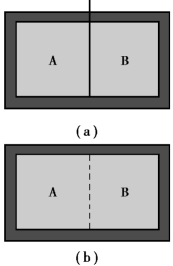
图7.1 平衡态(https://www.xing528.com)
(2)平衡态下系统的宏观性质不随时间变化.
系统平衡态是一种动态平衡,宏观性质不随时间变化,但从微观上看,组成系统的大量粒子的微观运动状态仍处于不停变化之中,只是大量粒子运动的总效果不变,在宏观上表现为系统的宏观性质不变.
要研究热力学系统的性质及其变化规律,需要对系统的状态进行描述,常采用一些表示物体有关特性的物理量作为描述状态的参数,称为态参量。对一定量的气体,其宏观状态可用气体的体积V、压强p 和热力学温度T 来描述.气体的体积、压强和温度这三个物理量称为气体的态参量,其中体积V 是几何量,压强p是力学量,而温度T 属热学量,它们都是宏观量.而组成气体的分子都具有各自的质量、速度、动量、能量等,这些描述个别分子的物理量称为微观量.宏观量和微观量都是描述同一物理对象,它们之间存在一定的内在联系。宏观量总是一些微观量的统计平均值。由于其统计本质,平衡状态下的宏观量数值会与确定值发生微小的偏差,这种现象称为涨落。由于宏观系统的大数粒子特性,这种涨落可以忽略不计。
气体的体积是气体分子所能达到的空间,与气体分子本身体积的总和是完全不同的概念.气体体积的国际单位制单位为立方米(m3),其他常用单位有升(L),换算关系为1 m3=103 L.
气体的压强是气体作用在容器器壁单位面积上的指向器壁的垂直作用力,即作用于器壁上单位面积的正压力,p=F/S.在国际单位制中,压强的单位为帕斯卡,简称帕(Pa),1 Pa=1 N/m2,其他常用压强单位有标准大气压(atm),毫米汞高(mmHg)等,其换算关系为:1 atm=1.013 25×105 Pa=760 mmHg.
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




