质谱中的离子,一般分为分子离子、碎片离子、同位素离子、亚稳离子和重排离子五类。从广义的角度来说,质谱中的离子只有分子离子和碎片离子两类。分子失去一个电子后键并未断裂即为分子离子,除此之外,由于键发生断裂、发生重排形成的碎片,都是碎片离子,即使是在飞行途中由亚稳离子形成的子离子也是碎片离子。至于同位素离子,在分子离子和碎片离子中都可能存在同位素离子,仅把含有同位素的分子离子命名为同位素离子。
1.分子离子
样品分子在离子化过程中失去(或得到)一个电子而未碎裂所形成的离子,称为分子离子,表示为M+·。离子化过程表示如下:
![]()
分子离子一般是质谱中质荷比m/z最大的离子峰,处于图谱的最右端。有些化合物在离子化过程中所产生的分子离子丰度可能很小、甚至没有。分子离子的质荷比m/z是检测化合物相对分子质量的重要依据。
2.碎片离子
在离子化过程中,分子离子发生化学键的断裂形成的离子,称为碎片离子。由于化合物结构不同,裂解方式不同,产生的碎片离子也不同。而最容易的裂解方式,并且产生的碎片离子数量多、稳定性好,这种碎片离子质谱峰多大,其中最多的碎片离子峰有可能就是基峰。
在质谱中,各种碎片离子都带有化合物的结构信息,它是质谱研究和鉴定化合物结构的重要依据。质谱中裂解时脱去的常见中性碎片和碎片离子,参见附录C。
3.同位素离子
每个元素的同位素都以一定丰度存在,其在化合物的同位素丰度仍然存在。在质谱图中会出现化学组成相同、电荷数相同,但质荷比m/z不同的同位素离子峰组,常把重质同位素的离子,称为同位素离子。有机化合物一些主要组成元素的同位素丰度比见表6-1。
表6-1 天然同位素的丰度比

有机化合物中最主要的两个元素是C和H。而13C的丰度比为1.08%,如果由12C组成的化合物质量数为M,存在1个13C原子,形成M+1的强度应为M的1.08%;存在2个13C原子,形成M+1的强度应为M的2.16%,由此可根据M和M+1的离子强度比来推算碳原子的个数,进而推测出可能的分子式。
而34S、37Cl和81Br的丰度比较大,其同位素离子峰非常特征,可利用其同位素峰强度比推断分子中含有这些原子的数目。
同位素峰强度比可用二项式(a+b)n的展开式各项求出,n为同位素原子数目,a与b分别为轻质与重质同位素的丰度比。
例如:1,2,4-三氯苯的质谱图及质谱表如图6-17所示。
(1)含三氯的同位素分子离子峰的二项式简约参数:a=3,b=1,n=3
展开式有四项:(a+b)n=a3+3a2b+3ab2+b3=27+27+9+1,4个峰
简约丰度比为:M﹕(M+2)﹕(M+4)﹕(M+6)=27﹕27﹕9﹕1(https://www.xing528.com)
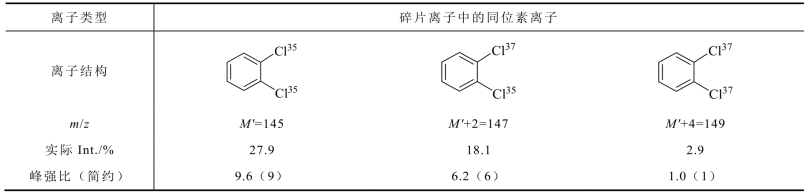
(2)含二氯的同位素碎片离子峰的二项式简约参数:a=3,b=1,n=2
展开式有三项:(a+b)n=a2+2ab+b2=9+6+1,3个峰
简约丰度比为:M′﹕(M′+2)﹕(M′+4)=9﹕6﹕1,M′=M-35
其同位素离子峰分析情况,参见表6-2。

图6-17 1,2,4-三氯苯的质谱图
表6-2 1,2,4-三氯苯的质谱同位素离子峰强度比分析

续表
1,3,5-三溴苯的同位素离子峰也有这种情况。
4.亚稳离子
在离子源中生成的离子![]() (称为母离子),若在离开离子源前,一部分被进一步裂解成离子m+2(称为子离子)和中性碎片Δm,即
(称为母离子),若在离开离子源前,一部分被进一步裂解成离子m+2(称为子离子)和中性碎片Δm,即![]() +Δm。
+Δm。![]() 和
和![]() 都可检测到,且它们的质荷比均为整数,是正常的离子峰。
都可检测到,且它们的质荷比均为整数,是正常的离子峰。
若这种裂解是在飞行途中发生,子离子![]() 的动能因被中性碎片Δm带走部分而变小,它的偏转半径R变小,在质谱中出现在比正常
的动能因被中性碎片Δm带走部分而变小,它的偏转半径R变小,在质谱中出现在比正常![]() 峰偏小的位置上,这种峰称为亚稳离子峰,以表观质量m*表示,三者有m*=
峰偏小的位置上,这种峰称为亚稳离子峰,以表观质量m*表示,三者有m*=![]() 的关系。亚稳离子峰弱而钝,一般不为整数(可跨2~5u)。通过大量质谱检索发现,亚稳离子峰在质谱中一般还是比较少见的。
的关系。亚稳离子峰弱而钝,一般不为整数(可跨2~5u)。通过大量质谱检索发现,亚稳离子峰在质谱中一般还是比较少见的。
5.重排离子
因重排裂解而得到的离子称为重排离子。根据分子结构不同情况,重排方式有很多,其中最典型的两个经验规律性的重排方式是麦氏重排和反狄尔斯-阿尔德裂解,参见“6.3.1”。
除了上述两种典型重排裂解产生重排离子外,还有通过四元环、五元环发生的重排,以及其它非典型的重排方式产生的重排离子。无论何种重排方式,其共同特点是两个或两个以上键的断裂并脱去中性碎片,生成的重排离子的质量数和电荷数的奇偶性不变。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




