1.胎盘亚全能干细胞概述
“亚全能干细胞学说”最早是由中国医学科学院组织工程研究中心主任、“长江学者”赵春华教授提出的[1]。该学说认为,在人体胚胎发育过程中,在多种组织中留存着具有多系分化能力的原始干细胞群体,并系统阐明了成体原始干细胞的等级结构性和功能。它们在胚胎发育成熟后逐渐失去部分原始干细胞表型,但在胚胎发育为成体后仍具有亚全能基因组,其中组织特异性基因在适当的微环境下可以被激活,因各自所处的微环境不同而向不同的组织分化,能够全方位地选择分化为各种组织细胞。

图2-2-1 干细胞按照多向分化能力划分的种类。

图2-2-2 胎儿多种组织源亚全能干细胞的细胞形态(比例=100μm)(A~G)。分别为心脏、肾脏、皮肤、肺、肝脏、肌肉、脂肪来源的亚全能干细胞[2]。
胎盘亚全能干细胞是来源于新生儿胎盘组织的一群亚全能干细胞,其在发育阶段与胚胎干细胞接近,同时具备多能干细胞的许多生物学特征(图2-2-2),是理想的原始干细胞来源。
2.胎盘亚全能干细胞的特点和优势(表2-2-1)
胎盘亚全能干细胞取自胎盘组织,其具有以下特性:
具有强大的增殖能力和多向分化潜能(图2-2-3)。在适宜的体内或体外环境下具有分化为间充质干细胞、上皮干细胞、神经干细胞、肝干细胞、肌细胞、成骨细胞、软骨细胞、基质细胞等多种细胞的能力。可以用来修复受损或病变的组织器官,治疗心脑血管疾病、神经系统疾病、肝脏疾病、骨组织病、角膜损伤、烧伤、烫伤、肌病等多种疾病。
具有免疫调节作用。通过负性免疫调节功能抑制机体亢进的免疫反应,使机体免疫功能恢复平衡,从而可以用来治疗造血干细胞移植之后的免疫排斥反应以及克罗恩病、红斑狼疮、硬皮病等自身免疫系统疾病。
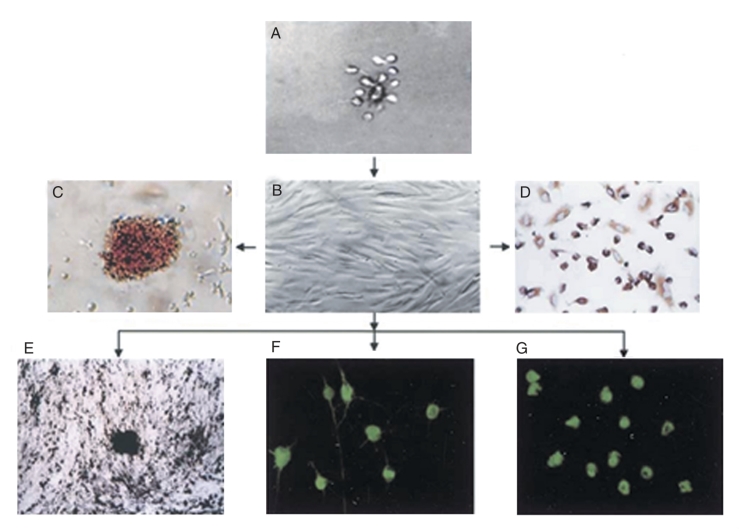
图2-2-3 亚全能干细胞的分化潜能。(A,B)
亚全能干细胞;(C)造血细胞集落;(D)内皮细胞;(E)成骨细胞;(F)神经细胞;(G)肝细胞[3]。
表2-2-1 胎盘亚全能干细胞的特点和优势

胎盘亚全能干细胞定向培养的间充质干细胞是人体微环境的重要组成部分,移植间充质干细胞可以改变造血微环境,重建免疫系统,促进造血功能恢复,与造血干细胞共移植能显著提高白血病和难治性贫血等的治疗效果。
3.胎盘亚全能干细胞的作用机制
适当的微环境可以激活亚全能干细胞的组织特异性基因表达程序,它们能够全方位选择分化为各种组织细胞,以维持人体发育和新陈代谢的平衡。
4.胎盘亚全能干细胞的适应证
国内外开展了许多关于胎盘干细胞临床前与临床研究,可用于以下疾病的治疗:
 神经系统疾病:脑瘫、卒中、脊髓损伤、帕金森病、多发性硬化、阿尔茨海默病等。
神经系统疾病:脑瘫、卒中、脊髓损伤、帕金森病、多发性硬化、阿尔茨海默病等。
 免疫系统疾病:系统性硬化、系统性红斑狼疮等。
免疫系统疾病:系统性硬化、系统性红斑狼疮等。
 消化系统疾病:肝硬化、克罗恩病等。
消化系统疾病:肝硬化、克罗恩病等。
 内分泌系统疾病:糖尿病等。
内分泌系统疾病:糖尿病等。
 皮肤病:烧伤等。
皮肤病:烧伤等。
 心血管系统疾病:心肌梗死、心肌缺血、动脉粥样硬化等。
心血管系统疾病:心肌梗死、心肌缺血、动脉粥样硬化等。
 血液病:再生障碍性贫血、移植物抗宿主病、白血病等。
血液病:再生障碍性贫血、移植物抗宿主病、白血病等。
 呼吸系统疾病:肺纤维化、肺支气管发育不良、肺气肿、慢性支气管炎等。运动系统疾病:股骨头坏死、骨关节炎等。
呼吸系统疾病:肺纤维化、肺支气管发育不良、肺气肿、慢性支气管炎等。运动系统疾病:股骨头坏死、骨关节炎等。
 其他:亚健康等。
其他:亚健康等。
5.临床应用案例简介
(1)帕金森病(Parkinson's disease)
帕金森病病理改变为:中脑黑质致密部、蓝斑神经元色素脱失,黑质色素变淡及出现路易小体,CT、MRI可发现脑萎缩、腔隙性脑梗死等,PET和SPECT检查可显示多巴胺代谢异常(图2-2-4)。
2013年,《中国组织工程研究》杂志报道了使用神经干细胞移植治疗30例帕金森病的有效性与安全性的临床研究[4]。该临床研究表明,30例帕金森病患者移植治疗无明显并发症。通过随访发现统一帕金森病评定量表评分结果以及帕金森Hoehn-Yahr分级下降,帕金森病Schwab&England日常活动分级评分增加,这说明神经干细胞移植能有效控制帕金森病病理进程、恢复受损脑功能、改善患者的神经功能。2012年,《中国微侵袭神经外科杂志》报道使用神经干细胞移植治疗12例帕金森病患者,帕金森病患者移植后3个月,其临床症状的改善率为75%,移植后6个月的改善率为83.3%[5]。2003年,《第二军医大学学报》就曾报道使用人神经干细胞移植治疗帕金森病患者,随访8~30个月(平均24个月),有效率为92%[6]。
现在,用于治疗帕金森病的干细胞有神经干细胞和非神经干细胞,非神经干细胞包括骨髓间充质干细胞、胎盘干细胞、脐带干细胞等。干细胞在许多神经系统疾病的细胞移植治疗方面取得很大进展,但其在促进神经功能恢复方面的体内作用机制可能相当复杂,目前尚不确切。
神经干细胞移植治疗帕金森病的可能作用机制[8]为向多巴胺能神经元分化、分泌多巴胺递质、改变细胞生物电变化、调节内环境、建立细胞间网络联系、减少炎症和神经元的退化、生长血管、改变帕金森病的自然进程。
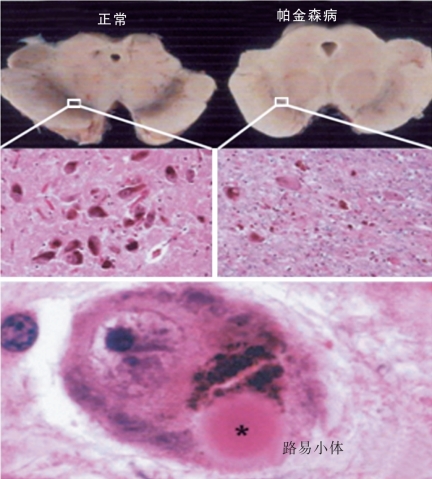
图2-2-4 普通人和帕金森病患者的中脑黑质体形态的比较[7]。
骨髓间充质干细胞治疗帕金森病的可能机制[4]是:①骨髓源基质细胞(BMSC)移植入脑内后,能形成表达神经标志性蛋白的神经元样细胞或星形胶质细胞,形成的细胞可在受损部位的周围存活甚至移行至全脑;②BMSC在脑内可与损伤的细胞融合,改变细胞表型并取代受损细胞,或者成为受损部位新生血管的主要组成细胞,并分化成血管内皮细胞和细胞外基质,帮助保护神经、促进血管发生;③BMSC在中枢神经系统微环境下能分泌脑源性神经营养因子、碱性成纤维生长因子等,或者刺激损伤部位产生内源性因子,从而促进损伤组织的修复并减少细胞凋亡。将骨髓间充质干细胞、胎盘干细胞、脐带干细胞等在体外先诱导分化为神经元细胞,再进行细胞移植以替代受损细胞,从而重建神经功能区和传导通路,最终达到治疗帕金森病的目的,这也是一种可行的实验方案。
(2)脑瘫
2010年,武警总医院对80例脑瘫患儿进行头部立体定向间充质干细胞移植治疗,术后患儿粗大运动功能评定(GMFM)、儿童精细运动功能评估(FMMF)、日常生活评定(ADL)、Barthel指数、Ashworth痉挛分级评估均明显改善[9]。患儿主要改善为:①肢体过高肌张力降低,尖足和交叉步缓解;②颈部和腰部力量增强,竖头和独坐时间延长;③增强肢体平衡性和协调性;④增加手部精细活动,拿硬币、拾豆子等动作更灵活;⑤改善言语功能,词汇增多,主动与人交流;⑥智力有不同程度的提高,反应能力增快,记忆力和理解力增强;⑦斜视和视力的改善等。其他研究结果表明,干细胞治疗后能够减弱脑瘫患儿第三室扩张等[10](图2-2-5)。
脑瘫患儿接受干细胞移植治疗后运动功能的改善次序与人体生长发育的基本规律一致,均为从上到下,从近端到远端,从粗大运动到精细运动,由此推测干细胞移植治疗脑瘫是通过修复损伤的脑细胞、重建神经网络,从中枢神经系统的起始部沿正常发育的轴线推动和促进神经系统发育而实现的,但是其深入的细胞分子学机制尚有待进一步研究[11]。
(3)心肌梗死
Strauer等将10例接受过标准治疗的心肌梗死患者,利用导管经冠状动脉进行了自体骨髓单个核细胞移植,3个月后移植组的梗死区面积明显下降,梗死区的室壁运动速度明显上升,移植组左心室的收缩末期容积、收缩率、梗死区的灌注均有显著改善[12]。浙江大学医学院附属医院对23例原发性扩张型心肌病患者,经冠状动脉内移植自身骨髓间充质干细胞治疗,结果发现,其可降低扩张型心肌病患者血浆B型利钠肽水平,并在一定程度上增加运动耐量,而无明显的致心律失常、栓塞和免疫炎症反应[13]。
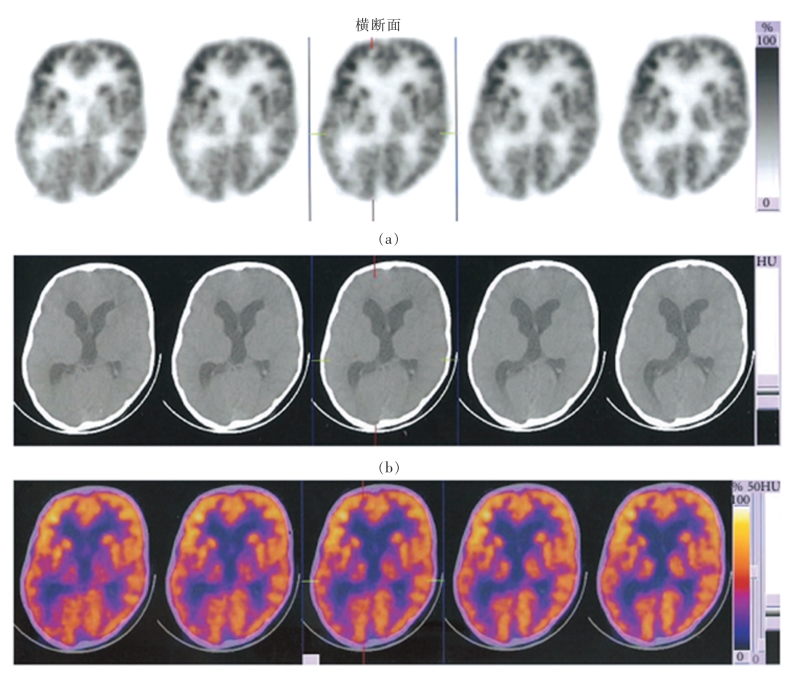
图2-2-5 干细胞治疗后PET和CT扫描结果:第三脑室扩张减弱,额叶中的橘黄色区域增加[10]。
目前用于心肌梗死治疗的干细胞主要有骨髓间充质干细胞、胚胎干细胞、胎盘干细胞、脐带血干细胞等多种干细胞。骨髓MSC移植改善心功能的可能机制[14]为:①移植细胞给心室壁提供了强有力的构架,能有效限制心肌的纤维化和坏死部位的扩张,改善心肌收缩性,增加其顺应性和弹性,并能与宿主的心肌细胞形成偶联,参与心脏的同步收缩;②移植的骨髓干细胞能表达多种细胞因子、生长因子、促血管生成因子,从而促进细胞增殖和血管再生;③血管再生有利于侧支循环建立,以及移植细胞的长期生存,抑制梗死区扩大与心肌细胞凋亡;④骨髓干细胞能表达肌钙蛋白-1和连接蛋白-43分子等心脏特异性标记物,这与心脏功能的改善密切相关。
(4)系统性红斑狼疮
系统性红斑狼疮(SLE)是一种由遗传、环境、激素等各种因素参与的、病因尚未完全清楚的、累及多脏器的自身免疫性疾病,临床治疗相当棘手。其易发于年轻女性,疾病多呈渐进性,病程中往往复发与缓解交替出现。
从中文期刊数据库和中华期刊数据库中查找干细胞治疗系统性红斑狼疮的资料,发现共计171例接受干细胞移植治疗[15]。总体自体外周血造血干细胞移植治疗系统性红斑狼疮患者1年内有效率达93.3%,复发率2.2%,有4.4%的移植相关死亡,1年后复发率7.3%。自体骨髓干细胞移植以及异体骨髓间充质干细胞移植治疗系统性红斑狼疮患者的近期临床效果好,随访1年无复发,无移植相关死亡。
Zhou等[16]在研究系统性红斑狼疮(SLE)治疗时提出,由于这类疾病的复杂性,健康供者来源的间充质干细胞(MSC)相对于患者自体来源的MSC更具治疗优越性。通过观察人骨髓来源的MSC对MRL/lpr老鼠的自身免疫性病理改善,证明了健康供者来源的MSC治疗SLE的优越性。此后,Sun等[17]又进行了一个采用脐带来源间充质干细胞(UC-MSC)治疗SLE的无对照临床研究。从2007年4月到2009年7月,共有16名活动性SLE患者(标准疗法治疗无效或者是出现危及生命的胃肠道并发症)进入研究,所有患者均做到知情并同意后方进行UC-MSC输注。移植后平均随访时间为15个月(3~28个月)。研究结果显示,SLEDAI评分(图2-2-6)、血清中ANA水平、抗-dsDNA抗体、血清白蛋白、补体C3和肾脏功能均有显著改善。伴随临床症状缓解,观察到了外周调节性T细胞的增加,以及Th1和Th2相关细胞因子间平衡的重建。所有患者的疾病活动性均显著降低,未观察到复发或治疗相关的死亡情况出现,故提出UC-MSC移植可以降低疾病活动性,改善血清学指标并稳定促炎性因子。

图2-2-6 间充质干细胞移植治疗(MSCT)后,系统性红斑狼疮疾病活动指数(SLEDAI)下降[17]。
干细胞治疗系统性红斑狼疮的可能机制[18]:利用同种异体MSC输注后重建骨髓造血微环境,修复系统性红斑狼疮患者造血干细胞的缺陷,并调节T、B细胞功能和炎症性细胞因子分泌,抑制自身反应性抗体如IgG、IgM、抗-dsDNA抗体和循环免疫复合物的产生,延缓或逆转狼疮肾病理改变,而达到治疗或缓解系统性红斑狼疮、减少免疫抑制药物应用的目的。
(5)肝硬化
肝硬化是肝进行性纤维化的终末病理表现,目前公认的有效治疗方法是肝移植,但由于供体来源不足、治疗费用高昂及术后免疫移植排斥反应等诸多难题,肝移植在临床上的应用受到了极大的限制。随着细胞治疗的兴起和成熟,细胞移植有可能成为肝硬化治疗的最佳备选方案。
在临床治疗方面,Terai等[19]报道了9名接受从周围静脉输注自体骨髓细胞治疗的肝硬化患者,在移植24周后,血清白蛋白、总蛋白水平明显改善(P<0.05),显著改善了Child-Pugh分级(P<0.05),并未观察到任何副作用。可见,自体骨髓间充质干细胞移植可以作为肝硬化的一种新的治疗方法。2007年10月,Mohamadnejad等[20]发表了骨髓MSC移植治疗失代偿期肝硬化的Ⅰ期临床试验结果。入选的为4名临床确诊的失代偿期肝硬化患者,通过静脉注射的方式给予体外扩增的自体骨髓MSC,在注射时及随后一年的观察期内,未见有明显副作用,其中有2名患者的肝病评分有改善。生活质量问卷调查显示,4名患者的生活质量均有较明显提高。虽然这些研究尚存在一些有待在进一步的临床试验中加以验证和解决的问题,但这并不妨碍我们对肝硬化的MSC移植疗法怀抱最美好的期望。
在国内,细胞移植治疗肝硬化也在进行临床试验。解放军第302医院肝病生物治疗研究中心采用间充质干细胞(脐带)治疗肝硬化腹水,升高了肝硬化腹水患者的白蛋白,下腹腹水也显著性减少。肝硬化腹水患者在间充质干细胞治疗前,腹水含量为(46.6±30.6)mm,治疗48周后为(6.6±13.6)mm[21]。黄强等对69例肝硬化采用自体骨髓干细胞移植治疗,可以明显减轻患者肝硬化、肝腹水、肝区疼痛等临床症状,谷丙转氨酶(ALT)也逐步恢复正常,其肝功能指标甲胎蛋白、总胆汁酸、谷丙转氨酶、总胆红素、白蛋白也显著性改善。另外,使用外周血干细胞、脐血干细胞也能够有效地改善终末期肝病患者的肝功能及临床症状[22]。
间充质干细胞治疗肝硬化的具体机制尚不清楚,当前推测主要有以下几个方面[23]:①MSC分化形成正常肝细胞,补充肝细胞数量,改善肝功能;②MSC分泌细胞因子/生长因子,抑制炎症反应;③MSC抑制肝星形细胞活化、阻止细胞外基质的生成;④MSC激活卵原细胞,促进肝细胞再生;⑤MSC降解肝内过量的细胞外基质。
(6)类风湿性关节炎
类风湿性关节炎(RA)是以手脚小关节发病,向心对称性发展,老年患者可能存在远端大关节受累,畸形常见为特征。RA发病可能与遗传、感染、性激素等有关(图2-2-7)。关节外表现包括血管炎、皮肤和肌肉萎缩、皮下结节、浆膜炎、(局限型)肺炎、淋巴腺病、脾肿大和白细胞减少[23]。
Augello[24]使用原代鼠源MSC代替MSC细胞系,在诱导小鼠关节炎的同时,腹腔注射原代鼠源MSC。结果显示,单次注射MSC可预防骨和软骨的严重不可逆性损伤,杀伤性T细胞增殖被抑制,炎性细胞因子如TNF-α、IFN-γ等表达量显著降低,同时调节性T细胞及IL-10和IL-4等调节性细胞因子分泌增多。这些结果提示,MSC细胞系与原代细胞相比,其分化潜能及免疫调节能力有所降低。另外,MSC免疫时间对炎症的抑制效果也起重要作用,MSC似乎对RA的预防比对RA的治疗效果更明显。González等[25,26]通过体外实验和体内实验均证明,人体脂肪来源的MSC(异体、异基因及自体)不仅可以有效改善RA的严重程度(评分改善)及缓解疾病症状,而且可通过对机体免疫分子的调控有效降低疾病的复发。
González等还从分子层面对这种治疗作用进行了阐述:MSC主要通过上调IL-10等抗炎症分子和下调Th1/Th2等炎症分子的分泌以实现其临床治疗效果,并发现MSC在炎症环境中表现出许多潜在的抗炎能力。(https://www.xing528.com)
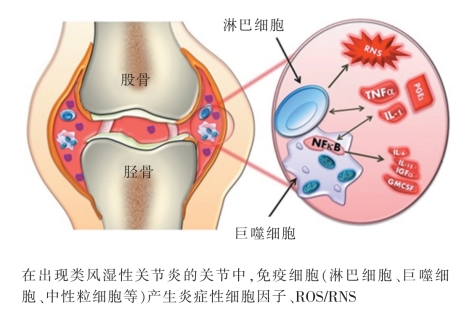
图2-2-7 类风湿性关节炎的发病机制[27]。
(7)克罗恩病
克罗恩病(Crohn's Disease)是原因不明的慢性炎症性疾病,可侵害由口腔至肛门的整个消化道,在消化道的任何部位均可发病,尤以小肠和大肠最多,患者主要是年轻人。最常见的症状为腹痛、腹泻、营养障碍以及随之而来的体重下降、发热等[23]。
荷兰等研究人员[28]为评估自体骨髓来源的MSC治疗难治性克罗恩病的可行性和安全性,将10位患者局部麻醉后抽出骨髓,分离出MSC后,进行扩增。9位患者分别接受了2次扩增的MSC,(1~2)×106/kg(细胞/体重),两次期间间隔7天。严格按本病疗效标准评估,结果6例有效,3例恶化而手术,未发现不良现象。因此,自体骨髓来源的MSC治疗难治性克罗恩病是安全可行的。
MSC移植可用于治疗IL-10缺乏动物所导致的自发性肠炎[23]。血管内皮生长因子和转化生长因子β1可表达于多种细胞,并参与肠炎的治疗。血管内皮生长因子是一种可以刺激淋巴细胞核血管内皮细胞聚集的细胞因子,血管内皮生长因子在肠道损伤修复中的作用已被详细阐明[23]。转化生长因子β1可以促进纤维及其他细胞增生并促进伤口愈合,而体内实验并没有发现间充质干细胞在创伤部位局部发生分化[23]。因此,MSC在溃疡性结肠等自身免疫性肠炎中可通过分泌并依靠血管内皮生长因子和转化生长因子β1发挥作用[23]。
间充质干细胞治疗克罗恩病的Ⅱ期临床研究在美国的4个主要中心进行,是一项前瞻性、随机、公开的试验。Osiris公司作为申请者公布了此项临床试验结果[29]。试验对象为10名类固醇和免疫抑制剂治疗失败的中度和重度的克罗恩病患者,克罗恩病活动指数(DAI)至少在220,患者每70天输注一次间充质干细胞,共进行两次输注,随访28天观察结果。患者被分为两组,一组为高剂量治疗组(8×106/kg),一组为低剂量治疗组(2×106/kg)。评价安全参数、CDAI的改变及炎性肠病调查表指标(IBDQ)的改善情况。为了排除药物治疗对结果的影响,在间充质干细胞治疗之前需要有90天的药物清除期。Ⅱ期临床研究的结果显示,经过28天的观察,平均CDAI从341降低到236,有统计学意义。平均IBDQ从113增加到146,有统计学意义。1/3的患者IBDQ在170以上,从而表明疾病得到减轻。结论为间充质干细胞的使用剂量和治疗效果呈明显正相关,高剂量组治疗效果更好。间充质干细胞对类固醇和英夫利昔单抗药物标准治疗失败的严重克罗恩病的治疗有很好的作用,同时患者有很好的耐受,无细胞毒性,无治疗相关的严重不良反应。
(8)多发性硬化症
在人的多发性硬化症(multiple sclerosis,MS)病理研究中,发现人MS与小鼠实验性变态反应性脑脊髓炎(experimental allergical encephalomyelitis,EAE)相似,提示MS可能是髓鞘碱性蛋白(MBP)抗原引起的自身免疫性疾病。该病的发生机制是针对MBP特异的Th细胞进入中枢神经系统后,接触MBP发生免疫应答,导致脊髓鞘破坏,引起疾病。MS是一种神经系统疾病,患者自身免疫细胞会错误攻击神经元髓鞘,造成患者出现视觉障碍、肌肉无力等症状[23]。
美国Burt等研究人员[30]利用自体无骨髓抑制的造血干细胞移植方法治疗了21名反复发作且干扰素治疗无效的MS的患者,结果81%的患者病情减轻。平均观察37个月后,16位患者未复发,全部患者病情未进展加重。Karussis等研究人员[31]报道利用自体骨髓MSC治疗MS患者15例和肌萎缩性脊髓侧索硬化症(ALS)19例。方法是将均值为63.2×106(±2.5×106)的MSC向鞘内注射(34例)或配合静脉注射(14例)给患者。按临床观察标准观察6个月,结果21例患者有短暂的与注射相关的发热,15例自述头痛,未发现较重的不良反应,试验取得成效,症状也显示出改善迹象。这提示临床采用MSC治疗MS患者和ALS患者是可行和相对安全的,其能迅速诱导出免疫调节作用。Yamout等研究人员[32]报道利用经扩增的自体骨髓MSC向鞘内注射治疗了10例MS患者,初步结果提示,临床采用经扩增的MSC治疗MS患者是有临床疗效和安全的,但放射影像结果未显示疗效。
目前,治疗多发性硬化的干细胞种类有造血干细胞、间充质干细胞和神经干细胞等。不同的干细胞发挥作用的机制也不一样。移植造血干细胞治疗多发性硬化的机制[33]主要是通过免疫抑制和免疫重建实现;胎脑神经干细胞和其他组织诱导的神经干细胞移植治疗多发性硬化的机制侧重于组织修复,神经干细胞可以分化细胞替代少突胶质细胞等。间充质干细胞通过MSC具有的免疫调节特性、修复功能以及通过分泌一系列复杂的神经营养因子保护神经功能等来发挥作用,其中MSC的神经保护功能及免疫抑制作用是治疗多发性硬化最重要的两方面机制[34]。
(9)脊髓损伤
脊髓损伤(spinal cord injury,SCI)是一种以损伤平面以下感觉、运动功能完全丧失和大小便失禁为主要临床表现的中枢神经系统的严重创伤(图2-2-8)。SCI使脊髓神经元大量丧失,导致了脊髓修复能力和促进修复因素(如神经营养因素)的缺乏,同时神经元坏死后形成的胶质瘢痕和空洞阻碍了轴突的生长,这些不可逆的病理过程是治疗SCI中最棘手的问题。近年,随着神经生物学和干细胞技术的发展,通过细胞移植时增加脊髓神经细胞数量、减少胶质瘢痕和空洞的形成成为可能。目前可供选择的抑制细胞类型有胚胎干细胞、神经干细胞、嗅鞘细胞、施万细胞、MSC等。
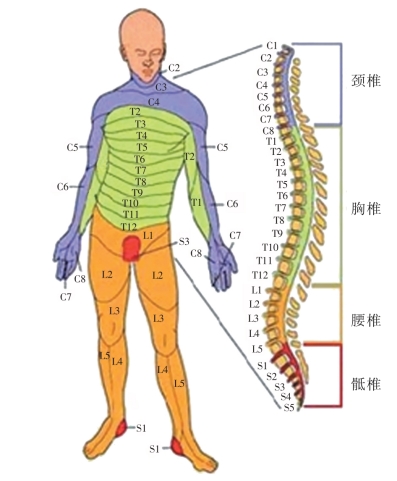
图2-2-8 脊髓损伤平面[40]。
临床研究方面,步星耀等[35]取自体髂骨MSC,将其脊髓内移植定向诱导分化与定向分化诱导椎管内移植相结合,采用直接移植法、经脑脊液注入移植法和经静脉注入移植法对87例SCI患者进行治疗。移植后患者的运动和感觉功能均有不同程度的恢复,且无任何不良反应。2006年,Moviglia等[36]对2名慢性脊髓损伤患者进行了骨髓MSC细胞移植治疗,其中一名19岁男性患者,治疗前T8以下截瘫,感觉平面位于T6,接受两次MSC治疗后6个月,运动平面恢复至S1,感觉平面恢复至S4。另一名21岁女性患者,C3~C5损伤表面为四肢瘫,C2以下感觉丧失,MSC治疗后3个月,动作和感觉平面恢复至T1~T2,且两名患者未发现移植后不良反应。这些研究初步证明了MSC治疗SCI的安全性和有效性。同时,MSC治疗SCI的移植方式、移植时间及移植细胞数的选择都是临床研究中仍待解决的问题。
干细胞移植修复脊髓损伤机制尚不十分清楚,目前一般认为有[37]:①替代受损的神经细胞。移植的干细胞在适合的微环境条件下具有分化为神经元和胶质细胞的可能,与宿主细胞重新建立神经联系,使受损的神经通路得以再通。②保护损伤脊髓中的内源性细胞,减少残存神经细胞的凋亡。植入的干细胞可下调与炎症和凋亡有关的基因并上调与神经保护有关的基因,减轻损伤脊髓的炎症和保护损伤的神经细胞,从而抑制细胞的凋亡。③促进残存神经元细胞轴突再生及突触形成。植入的干细胞与定居部位神经组织间相互作用,可分泌多种神经营养因子如脑源性神经营养因子、神经生长因子、血管内皮生长因子等,改变损伤脊髓局部微环境,为轴突再生提供合适的环境及支撑物,从而促进残存神经元细胞轴突再生及突触形成。④促进残存及再生轴突髓鞘形成。植入的干细胞可分化成少突胶质细胞,从而形成髓鞘,有助于脊髓损伤患者功能的恢复。⑤减少胶质瘢痕形成,增加抑制干细胞的可塑性,并为内源性修复机制创造有利的微环境。
(10)多系统萎缩
多系统萎缩(multiple system atrophy,MSA)是一组原因不明的、成人起病的、累及多部位的神经系统变性疾病,临床表现为不同程度的帕金森样症状、自主神经功能紊乱、小脑共济失调等,病理特征为神经胶质细胞质内形成α-突触核蛋白阳性包涵体。病情进展迅速,缺乏长期有效治疗药物,神经保护和神经再生不可避免地成为MSA治疗的切入点。Lee等[38]通过连续动脉注射和重复静脉注射的方式给予患者自体间充质干细胞(MSC)治疗,以评价MSC对于MSA的治疗效果及其对疾病预后的影响,在12个月的观察期内,MSC组(11名患者)相较对照组(18名患者),多系统萎缩统一评分量表(UMSARS)有显著改善,UMSARSⅠ量表中的直立性低血压和UMSARSⅡ量表中的小脑功能失调症状均有明显改善。对照组UMSARS评分12个月平均增加约14.2,比较而言MSC组则保持稳定,并显现出功能上的改善。
上述结果说明,MSC治疗MSA是安全有效的,可以延缓患者神经损害的进展,并促进随后的功能恢复。到目前为止,MSC确切的作用机制还未得到阐明,初步的推断是,MSC可能迁移至受损部位,产生多种营养因子,促进神经细胞的存货、功能恢复以及内源性再生作用[39]。
参考文献
[1]史明霞.骨髓和羊膜来源的Flk1+、CD31-、CD34-胚胎后亚全能干细胞生物学特性的研究[D].北京:中国协和医科大学,2006.
[2]Fang B,Li N,Song Y,et al.Comparison of human postembryonic,multipotent stem cells derived from various tissues[J].Biotechnol Lett,2009,31(7):929-938.
[3]Fang B,Liao L,Shi M,et al.Multipotency of Flk1CD34 progenitors derived from human fetal bone marrow[J].J Lab Clin Med,2004,143(4):230-240.
[4]张晓英.神经干细胞移植治疗帕金森病的有效性与安全性[J].中国组织工程研究,2013,17(27):5033-5040.
[5]陈涛,田增民,尹丰,等.神经干细胞移植治疗帕金森病的临床研究[J].中国微侵袭神经外科杂志,2012,17(10):452-453.
[6]田增民,刘爽,李士月,等.人神经干细胞临床移植治疗帕金森病[J].第二军医大学学报,2003,24(9):957-959.
[7]Frank C,Pari G,John PR.Approach to diagnosis of Parkinson disease[J].Can Fam Physician,2006,52(7):862-868.
[8]季正剑.骨髓间充质干细胞移植治疗帕金森病的实验研究[D].扬州:扬州大学,2011.
[9]程洪斌,伊龙,刘学彬,等.80例头部立体定向间充质细胞移植治疗脑瘫疗效分析[J].神经疾病与精神卫生,2010,10(4):355-357.
[10]Purandare G,Shitole DG,Belle V,et al.Therapeutic Potential of Autologous Stem Cell Transplantation for Cerebral Palsy[J].Case Rep Transplant,2012;2012:825-289.
[11]杨静,滑蓉蓉,郑培,等.间充质干细胞移植治疗小儿脑瘫疗效分析[J].武警医学,2012,23(7):586-592.
[12]Strauer BE,Brehm M,Zeus T,et al.Intracoronary,human autologous stem cell transplantation for myocardial regeneration following myocardial infarction[J].Dtsch med Wochenschr,2001,126(34-35):932-938.
[13]王建安,谢小洁,何红,等.骨髓间质干细胞移植治疗原发性扩张型心肌病的疗效与安全性[J].中华心血管病杂志,2006,34(2):107-110.
[14]蔡清明.骨髓间充质干细胞治疗心肌梗死的可能机制研究[J].中外医疗,2011,30(7):189.
[15]王亚莉,陈国军,方凤,等.干细胞移植治疗系统性红斑狼疮的国内临床报告分析[J].临床皮肤科杂志,2012,41(5):317-319.
[16]Zhou K,Zhang H,Jin O,et al.Transplantation of Human Bone Marrow Mesenchymal Stem Cell Ameliorates the Autoimmune Pathogenesis in MRL/Ipr Mice[J].Cellular & Molecular Immunology,2008,5(6):417-424.
[17]Sun L,Wang D,Liang J,et al.Umbilical Cord Mesenchymal Stem Cell Transplantation in Severe and Refractory Systemic Lupus Erythematosus[J].Arthritis Rheum,2010,62(8):2467-2475.
[18]黄金棋.骨髓间充质干细胞治疗系统性红斑狼疮鼠机制及疗效评价[D].福州:福建医科大学,2010.
[19]Terai S,Ishikawa T,Omori K,et al.Improved liver function in patients with liver cirrhosis after autologous bone marrow cell infusion therapy[J].Stem Cells,2006,24(1):2292-2298.
[20]Mohamadnejad M,Alimoghaddam K,Mohyeddin-Bonab M,et al.Phase 1 trial of autologous bone marrow mesenchymal stem cell transplantation in patients with decompensated liver cirrhosis[J].Arch Iran Med.2007,10(4):459-466.
[21]林泸,张政,施明,等.人脐带间充质干细胞治疗肝硬化腹水患者的前瞻性对照临床疗效观察.中华传染病杂志,2012,30(4):204-208.
[22]黄强.自体干细胞肝内移植术治疗69例肝硬化的临床分析[J].中国医药指南,2013,11(7):564.
[23]韩忠朝.间充质干细胞基础与临床[M].北京:科学出版社,2012.
[24]Augello A,Tasso R,Negrini SM,et al.Cell therapy using allogeneic bone marrow mesenchymal stem cells prevents tissue damage in collagen-induced arthritis[J].Arthritis Rheum,2007,56(4):1175-1186.
[25]González MA,Gonzalez-Rey E,Rico L,et al.Treatment of experimental arthritis by inducing immune tolerance with human adipose-derived mesenchymal stem cells[J].Arthritis Rheum,2009,60(4):1006-1019.
[26]Gonzalez-Rey E,Gonzalez MA,Varela N,et al.Human adipose- derived mesenchymal stem cells reduce inflammatory and T cell responses and induce regulatory T cells in vitro in rheumatoid arthritis[J].Ann Rheum Dis.,2010,69(1):241-248.
[27]http://www.nutritionremarks.com/wp-content/uploads/2013/03/Pat- hogenesis-of-Rheumatoid-Arthritis.png.
[28]Duijvestein M,Vos AC,Roelofs H,et al.Autologous bone marrow-derived mesenchymal stromal cell treatment for refractory luminal Crohn's disease:results of a phase I study[J].Gut.,2010,59(12):1662-1669.
[29]http://investor.oeiris.com/releasedetail.cfm?ReleaseID=215300.
[30]Burt R K,Loh Y,Cohen B,et al.Autologous non-myeloablative haemopoietic stem cell transplantation in relapsing-remitting multiple sclerosis:a phase I/II study[J].The Lancet Neurology,2009,8(3):244-253.
[31]Karussis D,Karageorgiou C,Vaknin-Dembinsky A,et al.Safety and immunological effects of mesenchymal stem cell transplantation in patients with multiple sclerosis and amyotrophic lateral sclerosis[J].Arch Neurol.,2010,67(10):1187-1194.
[32]Yamout B,Hourani R,Salti H,et al.Bone marrow mesenchymal stem cell transplantation in patients with multiple sclerosis:a pilot study[J].J Neuroimmunol,2010,227(1-2):185-189.
[33]耿同超,蔡哲,舒峻.干细胞移植治疗多发性硬化回顾和展望[J].中国康复理论与实践,2005,11(6):457-458.
[34]刘莹,侯宗柳.间充质干细胞移植治疗多发性硬化的研究进展[J].中国组织工程研究,2012,16(10):1889-1892.
[35]步星耀,张永福.骨髓间充质干细胞移植治疗脊髓损伤[J].实用诊断与治疗杂志,2004,18(14):259-261.
[36]Moviglia GA,Fernandez Vina R,Brizuela JA,et al.Combined protocol of cell therapy for chronic spinal cord injury.Report on the electrical and functional recovery of two patients.Cytotherapy.,2006,8(3):202-209.
[37]李亚梅,贾功伟,虞乐华.脊髓损伤治疗中干细胞的应用:移植时间、方式、次数及细胞选择[J].中国组织工程研究与临床康复,2010,14(49):9294-9297.
[38]Lee PH,Kim JW,Bang OY,et al.Autologous mesenchymal stem cell therapy delays the progression of neurological deficits in patients with multiple system atrophy[J].Clin Pharmacol Ther.,2008,83(5):723-730.
[39]http://www.aqavic.org.au/sci_facts/whats_sci.html.
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




