


与在纯水中相比,溶解度增加了38%。
如前所述,在重量法中为降低沉淀的溶解度应加入过量沉淀剂。但在产生同离子效应(使溶解度下降)的同时也必然存在着盐效应。盐效应会消弱由同离子引起的溶解度降低的效果。表7-1列出PbSO4在Na2SO4溶液中溶解度变化情况。
表7-1 PbSO4在不同浓度Na2SO4溶液中的溶解度






5.络合效应
在难溶化合物的溶解平衡体系中,加入络合剂可使溶解度增大,这种作用称为络合效应。
 (https://www.xing528.com)
(https://www.xing528.com)
有时沉淀剂本身也是络合剂,如Cl-既是Ag+的沉淀剂,又是络合剂。同离子效应可使AgCl的溶解度减小,络合效应又可使溶解度增大。究竟哪一个效应影响更大,这与〔Cl-〕的大小有关。〔Cl-〕对AgCl的溶解度的影响如图7-1所示。
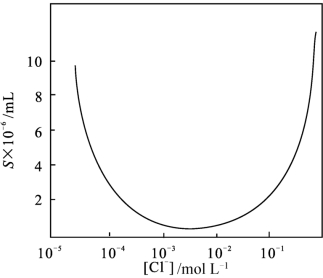
图7-1 AgCl的溶解度与〔Cl-〕的关系

6.其他影响因素
(1)温度的影响
大多数难溶化合物的溶解度随温度升高而增大,但不同化合物溶解度增大程度不一样,如图7-2所示。

图7-2 温度对几种难溶化合物溶解度的影响
分析时,由于某些原因(见第八章)往往需要在热溶液中进行沉淀。为减少沉淀因溶解而造成的损失,应放置冷却后再过滤、洗涤。当然对于溶解度极小或温度对溶解度影响不大的沉淀,可以趁热过滤。
(2)溶剂的影响
大多数无机盐易溶于水而难溶于有机溶剂。在重量分析时,有时可以在水溶液中加入一定量的可与水互溶的有机溶剂(如乙醇、丙酮)以降低沉淀的溶解度。当加入有机溶剂时也会减少干扰组分的溶解度,从而可增加杂质的共沉淀量,因此应该适当的控制有机溶剂的用量。
(3)沉淀颗粒大小的影响
同种沉淀,小颗粒沉淀比大颗粒沉淀的溶解度要大。这是因为,在相同质量的条件下,小颗粒沉淀的总表面积比大颗粒沉淀的总表面积大,而沉淀溶解平衡从微观上看是在溶液与沉淀相互接触的界面上发生的,沉淀的总表面积越大,与溶液接触的机会就越多,沉淀溶解的量也就越多。例如,BaSO4沉淀颗粒半径为0.05μm 时,溶解度为6.7×10-4 mol/L,而当颗粒半径为0.01μm 时,溶解度增大为9.3×10-4 mol/L,增大约39%。因此在沉淀重量法中,应尽可能地获得大颗粒沉淀。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




