1.缓冲剂和辅助络合剂的作用
络合滴定时因为EDTA 与金属离子的螯合反应不断释放H+〔反应式(5-1)〕,溶液酸度随之升高,KMY′ 下降,影响滴定突跃和准确度,因此络合滴定需在缓冲液中进行。
某些金属离子在滴定的条件下可能水解生成羟基络合物或沉淀,影响络合反应的速度和程度,因此络合滴定时有时还需加入辅助络合剂,如酒石酸、柠檬酸或氨水等,以防止金属离子的水解。例如在pH=10 的氨性缓冲液中,用EDTA 滴定Pb2+ 或Zn2+ 时,为防止Pb2+水解,需加酒石酸作辅助络合剂;对于Zn2+则其中的NH3既是缓冲剂又是防止水解的
辅助络合剂。
络合滴定时加入辅助络合剂会增加金属离子的副反应,降低条件形成常数,因此必须控制辅助络合剂的用量,使之不影响滴定的准确度。
2.单一离子滴定的最高酸度和最低酸度
当只考虑EDTA 的酸效应时(无其他副反应),单一离子被准确滴定的条件是


最低酸度pHmax=14.0-6.8=7.2,即在一般条件下又无其他辅助络合剂存在时,用2×10-2 mol/L EDTA 滴定Zn2+的适宜酸度为pH4.0~7.2。
3.目视法确定终点时准确滴定的酸度范围和最佳pH

【例5-8】用2×10-2 mol/L EDTA 滴定相同浓度的Mg2+,用EBT 作指示剂,终点误差在±0.1%范围内,求准确滴定的酸度范围和最佳pH。(https://www.xing528.com)
解 在适宜酸度范围内分别计算出下表所列各值:

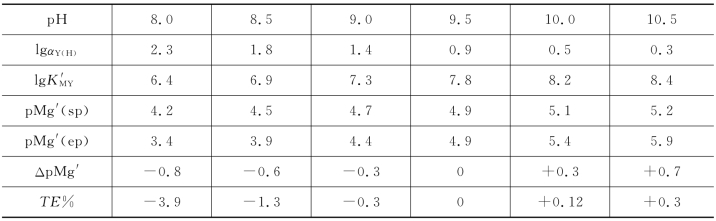
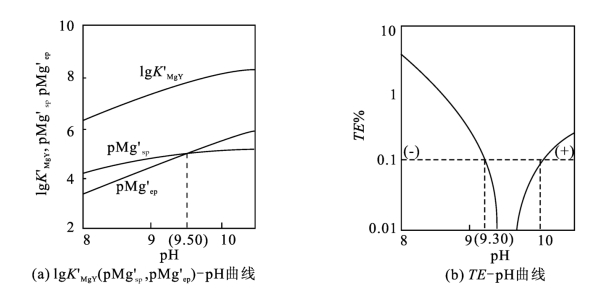
图5-11 作图法示例
图中曲线标“+”部分误差为正值,标“-”部分为负值
【例5-9】用2×10-2 mol/L EDTA 滴定相同浓度的Zn2+,用二甲酚橙作指示剂,要求|TE|≤0.1%,求准确滴定的酸度范围和最佳pH 值。
解 在pH4.0~7.2范围内选几个pH 值“点”,并按上例方法列表和作图(图5-12)。
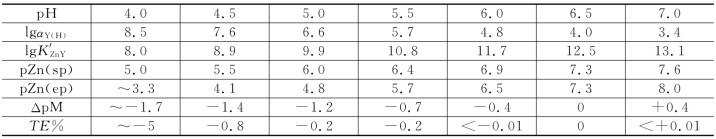
图5-12(a)![]() 线和
线和![]() 线交点处的pH 为6.5,故最佳pH 值为6.5。但由于使用二甲酚橙的最高pH 为6,而且从TE-pH 曲线可知,欲使TE≤0.1%,pH 低限为5.1,因此二甲酚橙作指示剂准确滴定Zn2+的酸度范围为pH5.1~6.0。这说明使用指示剂确定终点时,选择酸度时不仅要考虑终点误差,也应顾及指示剂的颜色变化。
线交点处的pH 为6.5,故最佳pH 值为6.5。但由于使用二甲酚橙的最高pH 为6,而且从TE-pH 曲线可知,欲使TE≤0.1%,pH 低限为5.1,因此二甲酚橙作指示剂准确滴定Zn2+的酸度范围为pH5.1~6.0。这说明使用指示剂确定终点时,选择酸度时不仅要考虑终点误差,也应顾及指示剂的颜色变化。
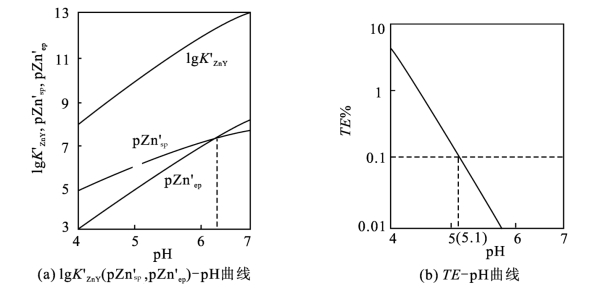
图5-12 作图法示例
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




