1.缓冲容量
一切缓冲溶液,只能在加入少量的强酸或强碱,或适当稀释时,才能保持溶液的pH 值基本不变。而当加入的强酸浓度接近缓冲体系的共轭碱的浓度,或加入的强碱浓度接近其共轭酸的浓度时,缓冲溶液的缓冲能力即消失。由此可见,缓冲溶液的缓冲能力是有一定限度的。早在1922年范斯莱克(Van Slyke)提出以缓冲容量作为衡量缓冲溶液缓冲能力大小的尺度。其定义为:向缓冲溶液中加入强碱或强酸使其浓度为d cb或d ca,d cb或d ca除以pH 的变化dpH 称为该缓冲溶液的缓冲容量,其数学表示式为:
![]()
β的单位为mol/L。
由于β为正值,加入强酸使溶液的pH 降低,故在d ca前加一负号。很显然,β值愈大,缓冲能力愈大。
2.影响缓冲容量的因素及有关计算
缓冲溶液的β值取决于溶液的性质、浓度和pH 值。根据式(4-50),结合各种溶液的具体条件,可以推导出β值的相应计算公式。
现以cHB(mol/L)HB-cB- (mol/L)NaB 体系为例来讨论。设缓冲组分总浓度为c(mol/L),则c=cHB+cB-,当加入cb(mol/L)NaOH,CBE为:

 (https://www.xing528.com)
(https://www.xing528.com)
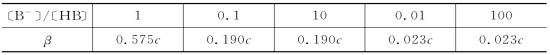
由式(4-54)可以清楚地看出,缓冲容量β与缓冲组分比及总浓度的关系,并且可以很方便地计算出〔B-〕/〔HB〕比值不同时相应的β值。


称为缓冲范围。
例如,HAc-Na Ac缓冲溶液,p Ka=4.76,其缓冲范围是pH=3.76~5.76。又如,NH3-NH4Cl缓冲溶液,p Kb=4.75(p Ka=9.25),其缓冲范围是pH=8.25~10.25。
图4-5是0.1 mol/L HAc在不同pH 时的缓冲容量。可见,当pH=p Ka=4.76时,即当〔HAc〕∶〔Ac-〕=1时,缓冲容量最大(β=0.057 5)。
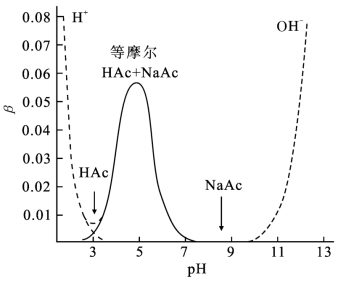
图4-5 0.10 mol/L HAc溶液在不同pH 值的缓冲容量
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




