在一定条件下,活泼金属元素的原子容易失去电子,而活泼非金属元素的原子容易得到电子,当这两种元素的原子相互接触时,容易发生化学反应,它们的原子有失去和得到电子变为离子的趋势,从而使核外电子层结构达到稳定状态。
例如,金属钠在氯气中燃烧生成氯化钠:![]()
在该反应中,钠原子失去最外层的一个电子,形成带有一个单位正电荷的Na+。
![]()
而氯原子最外层有7个电子,获得一个电子,形成带有一个单位负电荷的Cl-。
![]()
钠原子和氯原子得失电子后,都形成了稳定的结构。钠离子和氯离子之间通过静电吸引而相互靠近。随着两种离子的逐渐接近,两者之间的电子与电子、原子核与原子核的相互排斥作用也会逐渐增强,当两种离子接近至一定距离时,吸引和排斥作用达到平衡,此时阴、阳离子之间就形成了稳定的化学键。像氯化钠这样,凡由阴、阳离子间通过静电作用形成的化学键叫作离子键。
在化学反应中,一般都是原子的最外层电子参与反应。为方便起见,我们可以在元素符号周围用“·”或“×”来表示原子的最外层电子,这种式子叫作电子式。例如,H、Na、Mg、O、Cl原子的电子式分别为
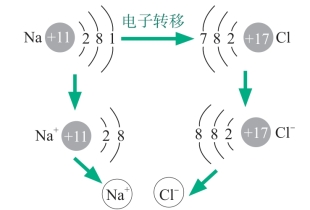
图5-10 氯化钠离子键形成过程示意图
![]() (https://www.xing528.com)
(https://www.xing528.com)
也可以用电子式来表示物质的形成过程。如氯化钠的形成过程可以这样表示:

表5-6 原子、离子、离子形成的化合物电子式表示方法
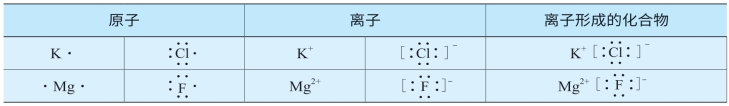
活泼金属(如钾、钠、钙等)和活泼非金属(如氯、溴、氧等)反应生成化合物时,都形成离子键。由离子键结合而成的化合物叫作离子化合物。绝大多数盐类、碱类和部分金属氧化物都是离子化合物,如MgBr2、Na2SO4、KOH、MgO等。
练一练
根据以上所学,尝试用电子式表示MgO、Na2S的形成过程。
想一想
上面我们研究的是活泼金属元素与活泼非金属元素以离子键结合形成离子化合物,那么非金属元素之间是如何结合形成化合物的呢?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




