议一议
下图中的蓝宝石和红宝石的主要成分是什么?颜色不同的原因是什么?

图4-16 蓝宝石

图4-17 红宝石
资料在线
红宝石和蓝宝石的主要成分都是Al2O3。它们之所以呈现不同的颜色,是因为除了Al2O3之外,还含有少量不同的金属元素。红宝石呈现红色是由于含有少量的铬(Cr)元素,蓝宝石呈现蓝色则是由于含有少量铁元素和钛(Ti)元素。
1.氧化铝(Al2O3)
Al2O3是白色、不溶于水的固体,熔点很高,是一种较好的耐火材料,它可以用来制造耐火坩埚、耐火管和耐高温的实验仪器。
天然产的Al2O3晶体叫刚玉,其硬度仅次于金刚石,可以用来制造钻头、砂轮等。在纯净的氧化铝中掺入少量其他金属氧化物,经过高温融合后,可制得人造宝石,如人造红宝石、人造蓝宝石等,它们大量用来做钟表里的轴承。
自然界存在的铝的氧化物主要有铝土矿,又称矾土。它是由一水氧化铝(Al2O3·H2O)、三水氧化铝(Al2O3·3H2O)以及少量氧化铁和石英等组成的。铝土矿可用来提炼纯的氧化铝。
Al2O3具有不同于一般金属氧化物的特殊性质,既能与酸反应也能与强碱反应。
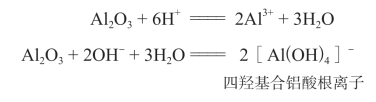
像Al2O3这样,既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,叫作两性氧化物。
读一读
铝的冶炼
铝是地壳中含量最多的金属元素,但人类大量使用铝制品却很晚。这是因为铝的化学性质活泼,在自然界以化合态形式存在,而从矿石中提取铝比较困难。19世纪中期,铝的价格甚至超过了黄金。1886年,23岁的美国青年化学家霍尔(C.M.Hall)发明了由Al2O3电解生产铝的方法。但由于Al2O3的熔点高,很难熔化,需要合适的助熔剂才能克服高温电解的困难,并降低能量消耗。经过反复探索,霍尔用熔化的冰晶石(主要成分是Na3AlF6)作为助熔剂,使Al2O3在1 000℃左右溶解在液态冰晶石中,成为二者的熔融体,然后通入直流电,电解出金属铝。同年,法国的埃鲁(P.T.Heroult)也独立发明了这种方法。1889~1892年,奥地利化学家拜耳(K.J.Bayer)发明了用碱从铝土矿中提取Al2O3的方法。这两种方法相结合,奠定了现代电解冶炼铝工业的基础。从此以后,铝的价格大大下降,铝真正得到了广泛的应用。
2.氢氧化铝[Al(OH)3](https://www.xing528.com)
氢氧化铝是几乎不溶于水的白色胶状物质,能凝聚水中的悬浮物,又有吸附色素的性能,可用于水的净化。
Al(OH)3既能与酸发生反应,又能溶于强碱溶液,是典型的两性氢氧化物。两性氢氧化物是既能与酸反应,又能与碱反应的氢氧化物。
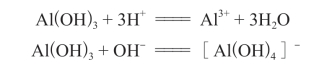
氢氧化铝加热时,可分解成氧化铝:
![]()
因为氢氧化铝能与强碱发生反应,因此,不能用铝盐和氢氧化钠来制备,实验室里一般采用在铝盐溶液中滴加氨水的方法来制取氢氧化铝。
![]()
Al(OH)3可用作医用胃酸中和剂。这是因为Al(OH)3可以与酸反应,使胃液酸度降低,起到中和过多胃酸的作用;同时Al(OH)3是一种两性氢氧化物,它的碱性不强,不至于对胃壁产生强烈的刺激和腐蚀作用。例如,复方氢氧化铝片(图4-18)是治疗胃酸过多的一种胃药,它的主要成分就是Al(OH)3。
3.明矾[KAl(SO4)2·12H2O]
明矾是KAl(SO4)2·12H2O的俗称,又称“白矾”“钾明矾”,是硫酸钾和硫酸铝的含水复盐。复盐是由两种不同的金属离子和一种酸根离子组成的,电离时能产生两种金属阳离子。

图4-18 含有Al(OH)3的胃药
![]()
明矾是一种无色晶体,易溶于水,与水发生水解反应生成Al(OH)3胶体。
![]()
明矾水解所产生的Al(OH)3胶状物质吸附能力很强,可以吸附水中的杂质,并生成沉淀,使水澄清。所以明矾常用作净水剂。

图4-19 明矾晶体
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




