对于一个系统的状态从整体上加以描述的方法叫宏观描述,这时所用的物理量称为宏观量。宏观量是反映大量气体分子的集体特性和状态的量,如压强p、体积V、温度T等。宏观量可以直接用仪器测量。
宏观状态有两种:平衡态和非平衡态。我们主要研究的是平衡态时的情况。
平衡态:在不受外界影响的条件下,一个系统的宏观性质不随时间变化的状态叫作平衡态。
这里所说的不受外界影响,是指外界对系统既不做功也不传热,即与外界无能量交换。平衡态是热动平衡,即从宏观上看,压强p、体积V、温度T等宏观量不变化;但从微观上看,气体分子在不停地运动,通过碰撞,各个分子的物理量在千变万化。平衡态是一种理想概念,严格的平衡态是没有的,只是在一定条件下,对实际情况的概括和抽象,因为任何系统不可能与外界无能量交换。但在许多实际问题中,经常可以把系统的实际状态近似地当作平衡态来处理,从而比较简便地得出与实际情况基本相符的结论。
系统的每一个平衡态都对应一组状态参量。在忽略重力的影响下,系统的任何一处的状态就是整个系统的状态,因为其压强、温度都是一样的。因此可应用压强p、体积V、温度T来描述系统的状态。在平衡态下,这些状态参量满足一定的关系,这个关系叫作物态方程。理想气体的物态方程为

式中,m为气体的质量,M为气体的摩尔质量,m/M为气体的物质的量。R为一常量,称为摩尔气体常量。在国际单位制中,其值为
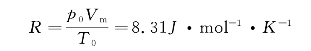
式中,p0、T0为标准状态(T0=273.15 K,p0=1.013×105Pa)下的压强和温度,Vm为标准状态下1mol理想气体的体积。实验表明,任何1mol物质所含有的分子数或原子数均相同,这个量称为阿伏伽德罗常量,用NA表示,NA=6.022×1023 mol-1。若以N表示体积V中的气体分子总数,则气体分子数密度n=N/V。引入一普适常量,称为玻尔兹曼常量,用k表示(https://www.xing528.com)
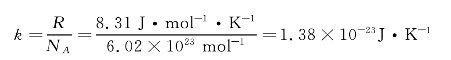
则理想气体物态方程可写为
![]()
平衡态可以用p—V图、p—T图、V—T图(见图8—1)上的点代表,即每个点代表一个状态

图8—1 平衡态示意图
非平衡态:若气体内部各处的压强和温度都不同,则气体处于非平衡态。气体在非平衡态时,不能用一组状态参量来描述系统的状态。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




