前述部分亚硝化的实验是在进水pH 8.7、湿干比1∶2、水力负荷1.0 m·d-1、温度(25±1) °C的条件下运行的,微生物的生长代谢与这些运行条件密切相关,当它们改变时,会影响微生物的生存环境和生长繁殖,进而可能破坏系统部分亚硝化的稳定性。因此,本节将选择稳定运行的部分亚硝化系统,通过改变进水pH、湿干比、水力负荷、温度等运行条件,考察系统内氮素污染物的变化规律,为进一步提高或稳定系统部分亚硝化性能提供参考。
(一)进水pH的影响
实际生活污水的pH一般为7.2~7.8,长期通过调节进水pH至8.7来维持部分亚硝化,是十分不现实的。因此,本研究选取了进水pH分别为8.4、8.7、9.0的CRI反应器(这些进水pH条件下NAR相对较高),编号P1、P2、P3,待系统运行稳定后将进水pH恢复到7.2~7.8,分别考察pH变化对各个系统运行稳定性的影响,进水pH恢复前后CRI系统内氮素污染物的变化如图2-8所示。
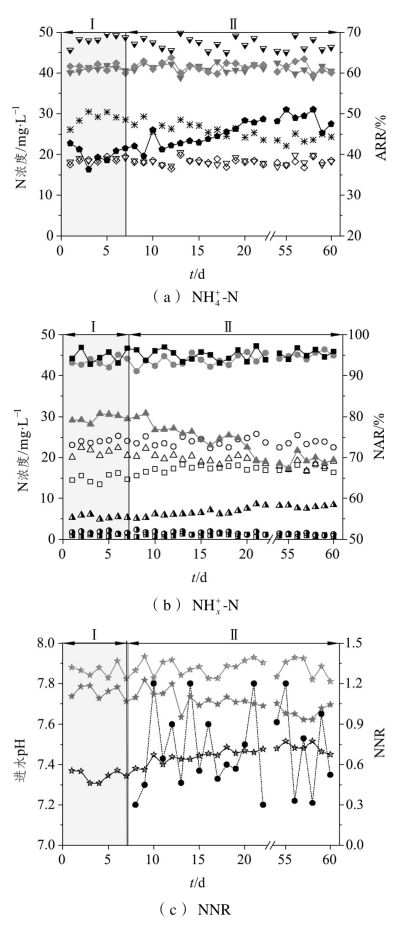
从图2-8(a)可以看出,当进水pH降回到7.2~7.8,连续运行53 d后,P1和P2反应器的NH4+-N去除率依然维持在60%左右,而P3反应器的NH4+-N去除率在运行至第3 d时开始升高,最后稳定在50%左右。由图2-8(b)可知,P1反应器的出水NO3--N浓度有所升高、NO2--N浓度有所下降,运行结束时NAR下降至69.5%;P2反应器的出水NO3--N和NO2--N浓度均较为稳定,NAR一直维持在90%以上;P3反应器的出水NO3--N浓度变化不大、NO-2-N浓度有所升高,因而NAR也有所提高。由图2-8(c)可知,P1、P2、P3反应器的出水NO-2-N/NH+4-N分别在1.0、1.3、0.7附近波动。
图2-8 进水pH恢复前后CRI系统内氮素污染物的变化
注:pH:阶段Ⅰ,P1=8.4,P2=8.7,P3=9.0;阶段Ⅱ,P1、P2、P3=7.2~7.8。
进水pH对部分亚硝化的影响与FA浓度密切相关。目前,关于FA抑制浓度的报道较多,但是关于FA抑制作用解除后AOB和NOB活性可否恢复的研究相对较少。孙洪伟等[125]在通过FA抑制协同过程控制成功实现SBR系统亚硝化的基础上,考察了FA抑制作用解除后硝化菌的活性变化,结果表明,当FA浓度逐步降至9.9、5.2、1.0 mg·L-1时,NO2--N积累率仍然维持在92.1%以上。本研究中,原初3个反应器内NOB的活性均处于受抑制状态,当FA降低时,P1反应器出水NO3--N浓度升高表明NOB活性抑制得到部分解除,P2、P3反应器出水NO3--N浓度波动较小表明受抑制的NOB活性难以恢复,较高浓度FA(13.15~21.68 mg·L-1)对NOB活性的抑制具有不可逆性;原初P3反应器内AOB的活性处于受抑制状态,当FA降低时,出水NO2--N浓度升高表明受抑制的AOB活性有所恢复,AOB对FA浓度变化的适应性更强。综上,通过调控进水pH至8.7成功启动CRI系统部分亚硝化后,将进水pH恢复至7.2~7.8,系统的部分亚硝化性能不会遭到破坏,仍能保持高效稳定的运行状态。
(二)湿干比的影响
CRI系统的一个运行周期包括一次淹水和一次落干的过程,淹水和落干的时间比(湿干比)对污染物的去除效果有重要影响,主要体现在两个方面:① 淹水时间的长短会影响污染物在滤料上的截留量或吸附量;② 落干时间的长短会影响生物膜上的微生物对污染物的转化量。在一个固定时长的运行周期内,淹水期过长,虽然可以截留或吸附更多的污染物,但是相应的落干期却被缩短,微生物没有充足的时间来转化这些截留或吸附的污染物,加上落干时间短,复氧效果差,微生物得不到充足的溶解氧,污染物的转化效率变得更低;相反地,落干期过长,微生物虽然可以获得较充分的降解时间和较充足的溶解氧,但是相应的淹水期却被缩短,污染物不能被高效的截留或吸附,随水流出而影响出水水质,同时由于落干期可被微生物利用的基质随之减少,微生物得不到充足的营养来维持生命活动进而影响处理效果。因此,选择一个合理的湿干比对系统的运行效果十分重要。
本节实验中,CRI系统每天运行2个周期,每个周期运行12 h,水力负荷1.0 m·d-1,温度(25±1) °C,进水pH为7.2~7.8。调节湿干比分别为1∶1(阶段Ⅰ)、1∶2(阶段Ⅱ)、1∶3(阶段Ⅲ)、1∶4(阶段Ⅳ)、1∶5(阶段Ⅴ)、1∶7(阶段Ⅵ),每个湿干比条件下运行10个周期,运行结果如图2-9、图2-10所示。
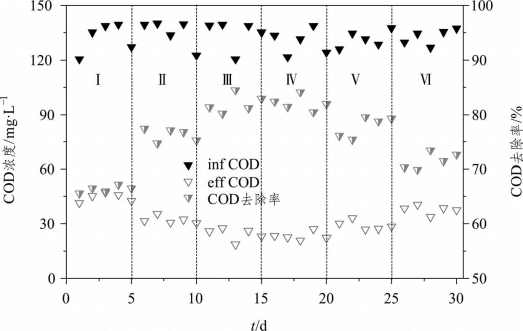
图2-9 不同湿干比下COD的去除情况
由图2-9可知,湿干比为1∶1~1∶3时,COD出水浓度随着湿干比的增大而减小,去除率则随着落干时间的增加而升高。湿干比为1∶3和1∶4时COD去除率均维持在80%以上,说明该湿干比范围内异养菌的生长状态最佳,系统既能在淹水期获得较好的有机物吸附效果,又能在落干期实现较好的有机物降解效果。当湿干比为1∶5和1∶7时,异养菌的营养基质随着淹水期的缩短而减少,COD去除率逐渐降低。
从图2-10来看,NH4+-N平均去除率在湿干比为1∶1时不足50%,当湿干比为1∶2~1∶4时稳定在60%左右,湿干比为1∶5和1∶7时分别降至50%和45%左右。NO2--N浓度表现出类似的变化规律,当湿干比为1∶2~1∶4时NO2--N浓度较高,在23 mg·L-1左右波动,湿干比为1∶1、1∶5、1∶7时有所减少,分别降至18、20、14 mg·L-1左右。NO3--N浓度在湿干比1∶1~1∶4时较低,湿干比1∶5和1∶7时分别升至3.78、4.88 mg·L-1。分析认为,湿干比为1∶1时,NH4+-N吸附量增大,但是由于复氧和落干时间太短,AOB缺少充足的溶解氧和反应时间,NH4+-N氧化成NO2--N的量减少,可供NOB氧化的NO2--N也减少,因而出水NH4+-N含量升高,NO2--N、NO3--N含量均减少。湿干比为1∶5和1∶7时,淹水时间分别减少至2.0、1.5 h,NH4+-N吸附量减少,可供AOB使用的基质总量减少,NH4+-N去除率降低,同时落干时间增加,复氧效率更高,然而可供AOB氧化的NH4+-N量却在减少,当NH4+-N被氧化为NO2--N后,系统内仍剩余较多的溶解氧,此时NOB利用这些剩余的溶解氧迅速氧化NO2--N,导致出水中NO3--N浓度升高。
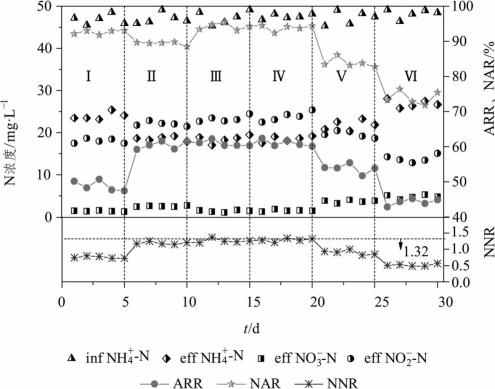
图2-10 不同湿干比下CRI系统内氮素污染物的变化
在湿干比为1∶3和1∶4时,平均NO2--N积累率分别为94.2%、93.9%,湿干比超过1∶4后NO2--N积累率逐渐降低。NO2--N/NH4+-N在湿干比为1∶3和1∶4时基本稳定在1.32附近,其余湿干比条件下则低于该值。综合考虑COD去除率、NH4+-N去除率、NO2--N积累率和NO2--N/NH4+-N,在湿干比为1∶3和1∶4时CRI系统均能实现部分亚硝化的稳定运行。
(三)水力负荷的影响
水力负荷反映了CRI系统在单位面积单位时间内处理的污水量,对系统的稳定运行至关重要[126]。主要体现在:① 水力负荷的大小决定了污水的投配量,水力负荷越大,处理的污水量越大,产水效率就越高,同时需要处理的污染物总量也在增加;② 水力负荷影响污水在反应器内的水力停留时间,水力负荷越大,污水流过滤料层的速率越高,污染物与滤料接触的时间就越短,进而影响系统的处理性能。因此,应根据CRI系统的实际承受能力来确定水力负荷,确保部分亚硝化出水水质的稳定。本节实验将水力负荷分别设置为0.25 m·d-1(阶段Ⅰ)、0.5 m·d-1(阶段Ⅱ)、0.75 m·d-1(阶段Ⅲ)、1.0 m·d-1(阶段Ⅳ)、1.25 m·d-1(阶段Ⅴ)、1.5 m·d-1(阶段Ⅵ),每个水力负荷条件下运行10~18个周期至稳定,每个周期运行12 h,湿干比1∶3,温度(25±1) °C,进水pH为7.2~7.8,运行结果如图2-11和图2-12所示。
从图2-11可以看出,水力负荷为0.25~1.0 m·d-1时,COD去除率随着水力负荷的增大而减小,水力负荷为0.25、0.5 m·d-1时,COD去除率均高于90%,可见水力负荷越低,COD的去除效果越好。水力负荷增加到1.25 m·d-1时,COD出水浓度升至49.2 mg·L-1,相应的COD去除率降至64.1%,比水力负荷为1.0 m·d-1运行结束时的COD去除率减少了20%,这是由于原先稳定运行的CRI系统已经适应1.0 m·d-1的水力负荷条件,当水力负荷突然增大,不仅COD负荷增大,水力停留时间也在减少,导致微生物表现出不适应性,因而COD去除效果变差。经过4 d的适应期后,COD去除率开始逐渐回升,最终稳定在75%左右。继续增大水力负荷至1.5 m·d-1,COD去除率降至38.1%,经2 d适应期后开始逐渐回升,最终稳定在55%左右。
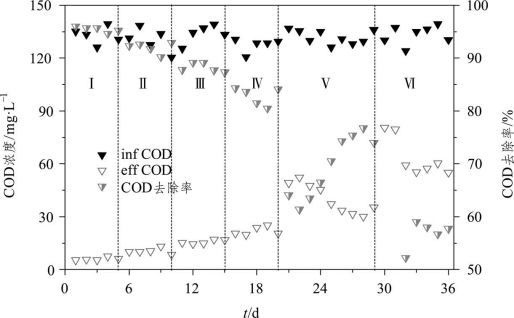
图2-11 不同水力负荷下COD的去除情况
由图2-12所示NH4+-N去除情况来看,水力负荷为0.25~1.0 m·d-1时,水力负荷越低,NH4+-N去除效果越好。水力负荷为1.25、1.5 m·d-1时,NH+4-N负荷增加,滤料表面对污染物的容纳能力有限,导致NH+4-N去除率下降,适应一段时间后NH+4-N去除率分别稳定在40%、35%左右。水力负荷为0.25~0.75 m·d-1时出水NO-2-N浓度相比水力负荷为1.0 m·d-1时更高,这是由于水力负荷越低,进入系统内的NH+4-N量越少,需要消耗的溶解氧也越少,因而NH+4-N转化为NO-2-N的效率也越高;相反地,水力负荷为1.25~1.5 m·d-1时,进入系统内的NH4+-N量增加,同时水力停留时间减少,AOB将NH4+-N转化为NO2--N的效率降低,因而出水NO2--N浓度进一步减小。出水NO3--N浓度随着水力负荷的增加而减小,对应的NO2--N积累率则随着水力负荷的增加而增大。值得注意的是,当水力负荷为0.25~0.75 m·d-1时出水NO3--N浓度明显高于水力负荷为1.0 m·d-1时的浓度,分析其原因如下:在淹水时间固定的情况下,水力负荷越低,进入系统内的污水量越少,NH4+-N总量减少,同时污水向下渗滤的速率减慢,由于上半段滤料颗粒表面的吸附点位较为充足,大部分NH4+-N在CRI系统的上半段就被完全吸附,而下半段滤料表面生物膜上的微生物特别是NOB处于相对“饥饿”的状态,待上半段滤料层中的AOB将NH4+-N氧化成NO2--N后,随下一次进水冲刷进入下半段滤料层,NOB利用过剩的溶解氧迅速将NO2--N氧化,因而NO3--N含量明显增加。因此,当水力负荷低于1.0 m·d-1时,为使出水能够耦合厌氧氨氧化的进水要求,应当考虑缩短滤料深度,以避免所生成的NO2--N被进一步氧化。
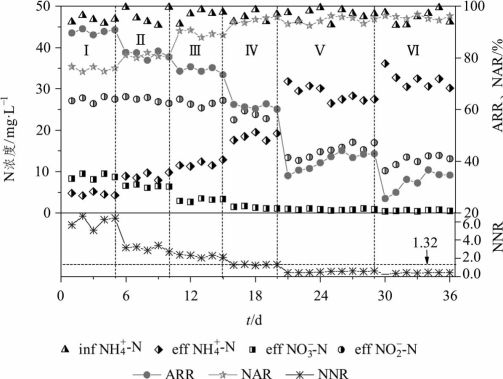
图2-12 不同水力负荷下CRI系统内氮素污染物的变化
结合NO2--N/NH4+-N可知,水力负荷为1.0 m·d-1时,出水NO2--N/NH+4-N为1.22~1.34;水力负荷低于1.0 m·d-1时,出水NO-2-N/NH+4-N大于1.32;水力负荷高于1.0 m·d-1时,NO-2-N/NH+4-N小于1.32。因此,水力负荷为1.0 m·d-1时,系统的部分亚硝化稳定性最好,能较为持续地匹配厌氧氨氧化的进水要求。
(四)温度的影响
温度是影响微生物生存的关键因素之一,它对微生物生长繁殖的影响主要体现在以下几个方面[127-129]:① 影响酶的活性,生物体内的各项代谢都需要在酶的催化作用下进行,酶多数属于蛋白质,温度的变化会影响酶促反应的速率,进而影响细胞的合成效率,不同类型的酶对温度的适应性不同,当高于或低于其最适温度范围时,酶活性就会下降甚至完全遭到破坏;② 影响细胞膜的流动性,细胞膜的流动性是细胞完成多种生理功能的基础,温度改变时,细胞脂质不饱和脂肪酸的含量受到影响,细胞膜的流动性发生变化,进而影响营养物质的吸收效率及代谢产物的分泌;③ 影响营养物质的溶解度,营养物质必须进入微生物细胞内才能被微生物利用,而营养物质在介质中的溶解性影响着其进入细胞的难易程度,温度的改变会影响营养物质的溶解性,进而影响微生物对营养物质的吸收。因此,温度的变化对系统的处理性能具有重要影响,探讨系统稳定运行的适宜温度范围十分必要。
本节实验在湿干比1∶3、水力负荷1.0 m·d-1、进水pH为7.2~7.8的条件下进行,为避免低温和高温对部分亚硝化系统造成不可逆的影响,故选择2个以25 °C为温度起点启动的部分亚硝化反应器,通过恒温循环水浴分别进行降温(25 °C→10°C,阶段Ⅰ~Ⅳ分别为25、20、15、10 °C)实验和升温(25 °C→40°C,阶段Ⅰ~Ⅳ分别为25、30、35、40 °C)实验,之后再将温度调回至25 °C(阶段Ⅴ),以考察温度变化对污染物去除性能影响的可恢复性。每个温度条件下运行10~20个周期至稳定,每个周期运行12 h,实验运行结果如图2-13至图2-16所示。
1.降温-升温实验
图2-13反映了降温-升温过程中部分亚硝化系统COD去除效果的变化。可以看到,当温度由25 °C降至20 °C时,系统的COD去除率依然维持在80%以上,可见适当的降温对COD去除效果影响不大。当温度降至15和10 °C时,COD去除率逐渐下降,但仍维持在70%以上,可见CRI系统中的异养微生物抵御低温冲击的能力较强。当温度回升至25 °C,异养微生物的活性逐渐恢复,降解有机污染物的能力也逐渐增强,运行6 d后COD去除率可恢复到80%以上。
 (https://www.xing528.com)
(https://www.xing528.com)
图2-13 降温-升温过程中COD的去除情况
由图2-14可知,当温度由25 °C降至20 °C时,出水NH+4-N、NO-2-N、NO3--N浓度的变化不大,NH+4-N去除率、NO-2-N积累率、NO-2-N/NH+4-N分别维持在60%、95%、1.3左右,在20~25 °C内系统的部分亚硝化性能十分稳定。当温度降至15 °C时,AOB的活性受到抑制,NH+4-N氧化为NO-2-N的过程受阻,出水NH+4-N浓度升高,NO-2-N浓度降低,但是该温度对NOB活性的抑制作用较小,因而NO3--N浓度变化不大。温度继续降至10 °C时,AOB和NOB的活性均受到严重抑制,NH+4-N氧化为NO-2-N的量大幅减少,可供NOB转化的NO-2-N量也大幅减少,导致出水NH+4-N浓度进一步升高,NO-2-N和NO3--N浓度减小,且NO-2-N浓度的减小程度更显著,该温度条件下运行稳定时NH+4-N去除率、NO-2-N积累率、NO-2-N/NH+4-N分别为17%、92%、0.15左右,此时NO-2-N积累率虽然较高,但是出水NO-2-N浓度仅为5 mg·L-1左右,系统的部分亚硝化性能处于较低水平。
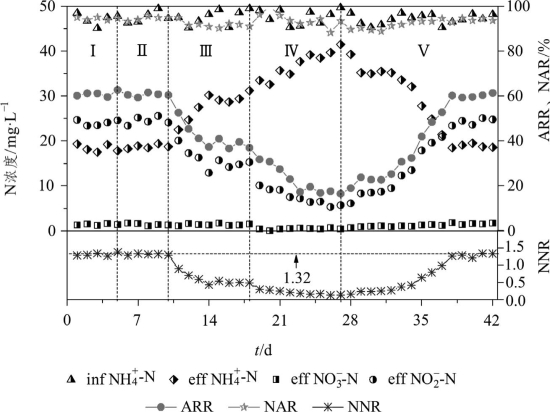
图2-14 降温-升温过程中CRI系统内氮素污染物的变化
郭宁等[130]研究了温度对SBR系统亚硝化过程的影响,结果发现温度为25 °C时的氨氧化率比15 °C时高出15.7%,温度为15 °C时的NO2--N积累率比25 °C时降低了12.1%。荣宏伟等[131]研究表明,温度由25 °C降低到5 °C时,NH4+-N去除率和NO2--N积累率分别为17.3%和6.9%,相比25 °C时分别降低了79.2%、88.3%。本研究也同样发现系统的亚硝化性能在温度为10~15 °C条件下远弱于20~25 °C,且低温(10~15 °C)对AOB菌群活性的影响要大于NOB,这是由于NOB的温度系数要比AOB小,因而AOB比NOB对温度的变化表现得更加敏感。
当温度回升至25 °C时,出水NH+4-N浓度减小,NO-2-N浓度增加,NO3--N浓度也略有增加,运行至第11 d起NH+4-N去除率、NO-2-N积累率、NO-2-N/NH+4-N基本恢复至原初水平。由此推测,低温(10~15 °C)主要是减弱了AOB和NOB菌群的生长代谢活性,使其生长繁殖受到抑制,导致生长缓慢或停滞。这也是AOB和NOB对低温胁迫表现出的一种抵御方式,低温虽然抑制了其生长繁殖,但是并不会致其大量死亡,它们仍能较长时间地维续生命。当温度回升至25 °C时,AOB和NOB的活性逐渐增强,系统的部分亚硝化性能随着温度的回升而逐渐恢复。综上,温度为20~25 °C时,CRI系统的部分亚硝化可实现稳定运行。
2.升温-降温实验
图2-15反映了升温-降温过程中部分亚硝化系统COD去除效果的变化。可以看到,温度为25~35 °C时有利于异养微生物的生长,COD去除率随着温度的升高而增加。温度升高至40 °C时,异养微生物的生长受到抑制,COD去除率明显下降,温度恢复至25 °C后,COD去除率有所回升但难以恢复至原先状态。
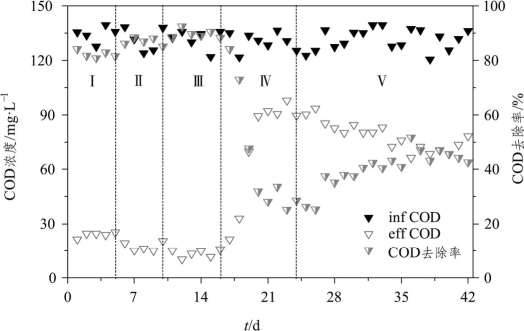
图2-15 降温-升温过程中COD的去除情况
部分亚硝化系统在升温-降温过程中氮素污染物的变化如图2-16所示。由图可知,温度为25~30 °C时,NH+4-N去除率、NO-2-N积累率、NO-2-N/NH+4-N较为稳定,可见温度升高至30 °C时系统依然能保持良好的部分亚硝化性能。当温度升至35 °C时,AOB和NOB的活性均得到增强,但是对NOB活性的提升效果更明显,因此虽然NH+4-N被AOB氧化为NO-2-N的量增多,但被NOB进一步氧化为NO3--N的量也在增多,因而出水NH+4-N浓度下降,NO-2-N浓度与前阶段相差不大,虽然NO3--N浓度明显增加,NO-2-N积累率反而下降。继续升温至40 °C时,AOB和NOB活性均开始下降,系统部分亚硝化性能遭到破坏,表现为出水NH+4-N浓度明显升高,NO-2-N、NO3--N浓度明显降低,该阶段运行结束时的NH+4-N去除率仅为27.8%,NO-2-N/NH+4-N仅为0.21,远达不到厌氧氨氧化的进水要求。
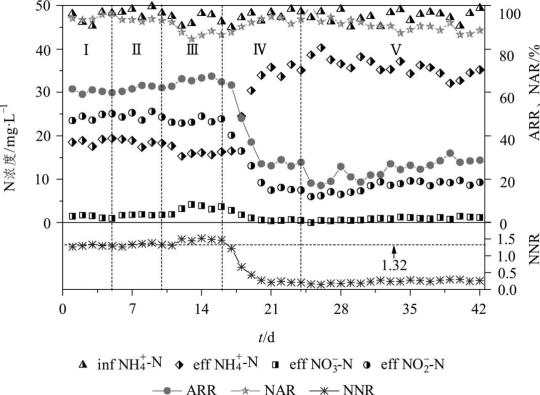
图2-16 降温-升温过程中CRI系统内氮素污染物的变化
当温度降回至25 °C后,出水NH4+-N的浓度不但没有降低,反而略有升高。分析认为,在一定温度范围内,硝化反应速率随着温度的升高而加快,但是超过一定限度(40 °C)后,细胞内的酶蛋白易发生热变性,导致大部分AOB和NOB菌群失活或死亡,硝化菌在数量和活性上均受到严重影响。此时温度由40 °C降回至25 °C,剩余的AOB和NOB再次受到温度冲击,因不能迅速适应而表现为NH+4-N的去除率进一步降低,出水NO-2-N、NO3--N浓度也较低。经过一段时间的适应后,少部分对温度变化耐受范围较宽的硝化菌存活下来,NH+4-N去除率略有回升,但回升空间十分有限,在25 °C下连续运行18 d后,NH+4-N的去除率仍然仅有28.7%,NO-2-N/NH+4-N仅为0.26,系统的部分亚硝化性能无法得到完全的恢复。综上,温度为25~30 °C时,CRI系统均能保持良好的部分亚硝化性能,可为厌氧氨氧化提供稳定的进水条件。
(五)基质浓度的影响
1.氨氮浓度
本节实验控制进水COD浓度为120~140 mg·L-1,pH为7.2~7.8,湿干比1∶3,温度(25±1) °C,通过改变NH4Cl的添加量,将进水NH4+-N浓度设置为10~15 mg·L-1(阶段Ⅰ)、25~30 mg·L-1(阶段Ⅱ)、45~50 mg·L-1(阶段Ⅲ)、65~70 mg·L-1(阶段Ⅳ)、95~100 mg·L-1(阶段Ⅴ)、145~150 mg·L-1(阶段Ⅵ)共六个水平,改变每个水平后运行10个周期,每个周期运行12 h,每天取样检测出水水质,结果如图2-17和图2-18所示。
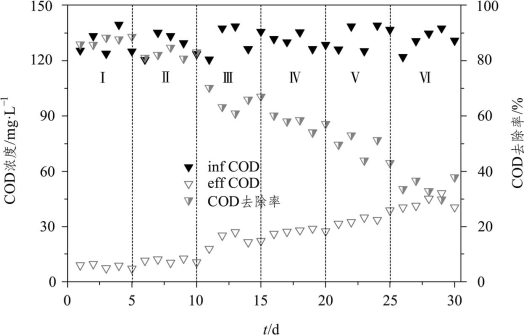
图2-17 不同氨氮浓度下COD的去除情况
由图2-17可知,进水NH4+-N浓度为10~15 mg·L-1和25~30 mg·L-1时,出水COD浓度在均在15 mg·L-1以下,去除率维持在90%以上,可见低NH4+-N浓度有利于COD的去除。NH4+-N可为好氧异养菌的生长繁殖提供氮源,适量的NH4+-N即可满足其合成自身物质所需要的氮量,因此进水NH4+-N含量较低时COD去除效果不但没有降低,反而可为好氧异养菌腾出更多的氧源和吸附点位,使得COD去除效果更好。随着进水NH4+-N浓度的提高,COD去除效率逐渐降低,当NH4+-N浓度为45~50 mg·L-1时,COD去除率为80%~85%,而当NH4+-N浓度达到145~150 mg·L-1时,出水COD浓度高于40 mg·L-1,去除率仅为65%左右。进水NH4+-N浓度的大幅增加导致吸附点位减少,同时硝化菌与降解有机物的好氧异养菌争夺氧源,导致COD去除率下降。
由图2-18可知,随着进水NH4+-N浓度的升高,NH4+-N去除率逐渐降低。但是当进水NH4+-N浓度在10~50 mg·L-1时,NH4+-N去除量随着NH4+-N浓度的升高而增加,出水NO2--N浓度逐渐升高、NO3--N浓度逐渐降低。这是由于FA是AOB的真正基质,其浓度与进水NH4+-N浓度、pH、温度等密切相关。本实验中pH、温度保持不变,FA主要与进水NH4+-N浓度有关,适当提高NH4+-N浓度可给AOB提供充足的基质,从而促使其更好地将NH4+-N转化为NO2--N,因而NH4+-N去除量升高。由于AOB氧化NH4+-N的过程消耗了更多的氧,NOB可利用的氧量减少,因而NO3--N浓度降低。当进水NH4+-N浓度在65~150 mg·L-1时,NH4+-N去除量开始低于前一阶段且随着NH4+-N浓度的升高而逐渐减少,相应的出水NO2--N和NO3--N浓度进一步降低。
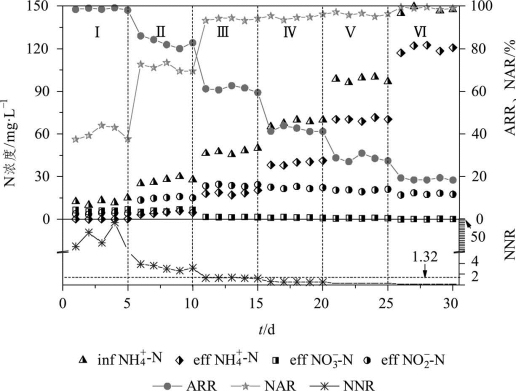
图2-18 不同氨氮浓度下CRI系统内氮素污染物的变化
进水NH4+-N浓度过高时影响系统部分亚硝化效果的主要原因有两个:① 当FA浓度处于只抑制NOB阈值范围内时,部分亚硝化脱氮效果较稳定,而进水NH4+-N浓度升高导致FA浓度处于抑制AOB阈值范围内时,NH4+-N的氧化过程就难以进行[132];② CRI系统内滤料表面生物膜的生态系统已经基本处于平衡状态,系统内的吸附点位和氧源有限,进水NH4+-N浓度过高时,由于吸附点位有限,不足以容纳过多的NH4+-N,与此同时,在溶解氧量有限的情况下,AOB难以氧化过多的NH4+-N,导致出水NH4+-N过剩。经计算,本实验中FA的浓度范围为0.14~8.12 mg·L-1,不处于抑制AOB和NOB阈值范围内,因此进水NH4+-N浓度对硝化效果的影响与FA的抑制作用关系不大,而主要与系统内的吸附点位和氧量有关。
2.有机物浓度
控制进水NH4+-N浓度为45~50 mg·L-1,其余条件不变,通过改变C6H12O6的添加量,将进水COD浓度设置为50 mg·L-1(阶段Ⅰ)、100 mg·L-1(阶段Ⅱ)、150 mg·L-1(阶段Ⅲ)、200 mg·L-1(阶段Ⅳ)、300 mg·L-1(阶段Ⅴ)、500 mg·L-1(阶段Ⅵ)共六个水平,改变每个水平后运行10个周期,每个周期运行12 h,每天取样检测出水水质,结果如图2-19和图2-20所示。
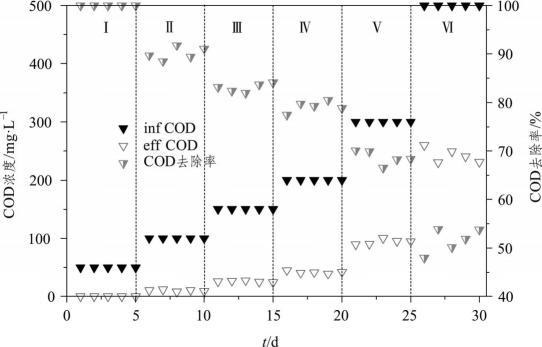
图2-19 不同有机物浓度下COD的去除情况
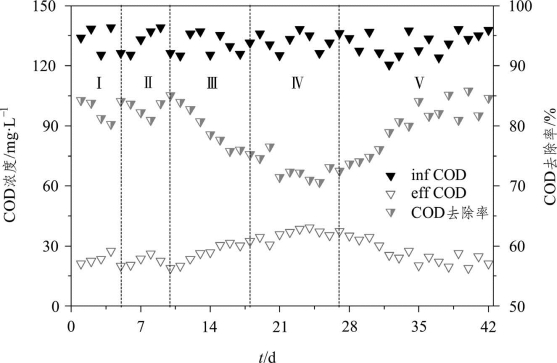
由图2-19可知,随着进水COD浓度的提高,出水COD浓度也不断提高,COD去除率逐渐降低,当进水COD浓度为500 mg·L-1时,平均去除率仅为51.5%。然而,阶段Ⅰ~Ⅵ的平均COD去除量却在逐渐增大,分别为50.0、90.1、124.6、158.3、205.9、257.7 mg·L-1,这表明有机物浓度提高后,为好氧异养菌提供了更多的营养底物,促使其增殖速率加快,因而能去除的有机物量也逐渐增大。
由图2-20可知,出水NH+4-N浓度随着进水有机负荷的提高而增加,NH+4-N去除率逐渐降低。当进水COD浓度为50 mg·L-1时,为NH+4-N的转化提供了更多的空间和溶解氧,因此NH+4-N去除率最高,但溶解氧过剩导致生成的部分NO-2-N又被NOB利用进一步转化成NO3--N,因此NO-2-N积累率反而下降。当进水COD浓度为100~150 mg·L-1时,NH+4-N去除率、NO-2-N积累率、NO-2-N/NH+4-N分别维持在60%、95%、1.3左右,基本能达到厌氧氨氧化的进水要求。进水COD浓度继续升高至200 mg·L-1时,NH+4-N去除率略有降低,但仍维持在60%左右,可见系统对COD冲击具有一定的“弹性”适应力,适当提高COD浓度并不会导致NH+4-N去除效果的明显下降。进水COD浓度升高至300和500 mg·L-1时,出水NH4+-N浓度继续升高,NO2--N和NO3--N浓度继续减小,NO2--N/NH4+-N逐渐偏离理论值1.32,这是由于在稳定运行阶段反应器中各类菌群处于一种平衡状态,有机物浓度升高后,好氧异养菌凭借其自身生长繁殖快的优势,利用充足的有机物作为碳源和营养物质不断增殖,与AOB和NOB竞争生存空间和溶解氧,抑制了AOB和NOB的生长,阻碍了硝化反应的进行,因而NH4+-N和NO2--N的氧化过程均会受阻。
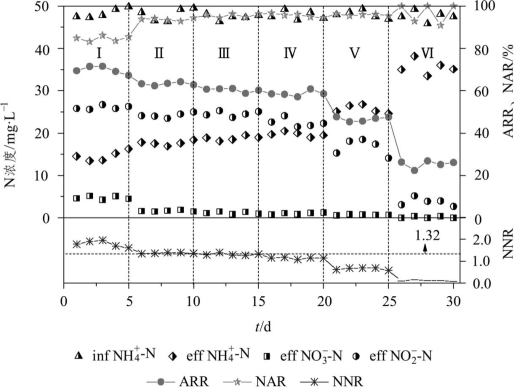
图2-20 不同有机负荷下CRI系统内氮素污染物的变化
但是,阶段Ⅳ、Ⅴ、Ⅵ的平均TN损失率相比阶段Ⅲ分别提高了3.5%、4.4%和11%,分析认为,较高的进水COD浓度为反硝化提供了充足的有机碳源,同时在本实验条件下CRI反应器内可能存在部分缺/厌氧区域,为反硝化菌将NO2--N或NO3--N转化为N2提供了有利条件,因而TN去除率反而得到提升。总体而言,低有机负荷对CRI系统部分亚硝化的影响比高有机负荷低,进水COD浓度在100~150 mg·L-1时,CRI系统可较稳定地维持部分亚硝化效果。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




