高分子材料的品种很多,按用途和性能可分为合成高分子材料(包括塑料、合成纤维、合成橡胶、黏合剂和涂料等)、功能高分子材料和复合材料。其中,应用最为广泛的是“三大合成材料”——塑料、合成纤维、合成橡胶。
1.塑料
日常生活中,人们天天与塑料打交道,究竟什么是塑料呢?塑料的主要成分是合成高分子化合物即合成树脂,如聚乙烯、聚氯乙烯、聚苯乙烯、酚醛树脂等。此外,还有根据需要加入的具有某些特定用途的添加剂,如防止塑料老化剂、提高塑料塑性的增塑剂等。
塑料制品的原料是高分子聚合物,其主要缺点是不易降解和具有一定的毒性。人们随意抛弃在自然界中的废旧塑料包装制品(塑料袋、薄膜、餐盒、饮料瓶、包装填充物等),飘挂在树上,散落在路边、街头、水面、农田等的这种随处可见的污染环境现象,称为“白色污染”。我国自2008年6月1日开始实施的“新塑令”,就是为了限制和减少塑料袋的使用,遏制“白色污染”。
据国外报道,泡沫塑料餐具在一定温度下会析出剧毒物质二噁英,严重危害人体健康。遗弃的塑料制品如黏有污染物,会成为蚊蝇和细菌生存、繁殖的温床,同样也会危及人体健康。
现在研制出的一种以淀粉为主要成分的塑料餐具,既能做餐具盛放食物,又能做饲料。即使扔在野外遇到雨水也会自行分解,不会污染环境。可以预料,用不了多久,这种可食用的塑料餐具将会日益推广使用,但目前,脲醛树脂仍在餐具市场占有优势。这是造成环境白色污染最主要的来源。
塑料的品种很多,用途也各不相同。根据受热时所表现的性能不同,塑料可分为热塑性塑料(线型高分子)和热固性塑料(体型高分子)。按照实际应用,塑料又可分为通用塑料、工程塑料、耐高温塑料和特种塑料等。
塑料具有质量轻、优良的介电性能和机械性能、化学稳定性高、生产效率高、成本低等优点,因此,塑料制品广泛应用于工业、农业、国防建设和人们日常生活等各个领域。
■资料卡片
制作聚氯乙烯塑料薄膜采用的基本原料是聚氯乙烯树脂和适量的增塑剂、稳定剂等。常用的增塑剂是邻苯二甲酸二丁酯和邻苯二甲酸二辛酯,它们都易溶于油中。如果该薄膜接触到油腻食品,增塑剂便会溶解在油中,人吃了这些物质,对健康是有害的。此外,常用的稳定剂三盐基硫酸铅也是有害物质,它能在人体内积蓄,危害身体。因此,日常生活中,不宜用聚氯乙烯塑料薄膜包装食品。
2.合成纤维
纤维分为天然纤维和化学纤维两大类,其中化学纤维又分为人造纤维和合成纤维。人造纤维是利用不能直接纺织的天然纤维(如木材、棉短绒)做原料,经化学处理制成;合成纤维是利用石油、煤、天然气等为原料,经过化学合成和机械物理加工制成的一种纤维。
合成纤维工业创立于20世纪40年代,由于原料丰富、价格低廉、用途广泛等,得到了迅速发展。被称为合成纤维的“六大纶”(涤纶、锦纶、腈纶、丙纶、维纶和氯纶,由于具有强度高、弹性好、耐腐蚀、不缩水、质轻保暖等优点,大大地改善了人们的衣着水平。此外,在工农业生产和高科技领域,合成纤维也有广泛的应用。如工业用的绝缘材料、渔业用的缆绳、医疗用的输液管、航天用的太空服等都离不开合成纤维。
■生活中的化学
聚乳酸纤维是一种极易水解的合成纤维,独特的降解作用使之在医学领域具有神奇的应用。比如,将聚乳酸纤维用作外科手术缝合线,当伤口愈合时,常常不必拆线。因为,在生物体内,聚乳酸纤维分子会发生水解反应降解为乳酸,并最终通过身体的正常代谢循环排出体外。
不仅如此,使用聚乳酸及其共聚物作支持材料,移植上器官、组织的生长细胞,还可以形成自然组织,这无疑为重度烧伤及大面积皮肤缺陷病人的康复治疗带来了希望。
3.合成橡胶
橡胶是一种弹性高聚物,具有高弹性,当施以外力时形状发生改变,去除外力后,又能很快地回复到原来的形状,这也是橡胶区别于塑料、纤维等其他高分子材料的主要标志。
橡胶可分为天然橡胶和合成橡胶两种。天然橡胶由橡胶树(图8-7-2)或橡胶草中的乳胶加工而制得的,而合成橡胶是以石油、天然气或煤等为原料生产出的二烯烃作为结构单元,再使它们聚合而制成的高分子化合物。
合成橡胶自20世纪40年代起得到了迅速发展。目前已有的丁苯橡胶、顺丁橡胶、氯丁橡胶、硅橡胶等,由于在耐磨、耐热、耐燃、耐寒、耐腐蚀和耐老化等方面具有独特的性能,因此在生产生活中得到了广泛应用。图8-7-3所示为汽车轮胎。

图8-7-2 橡胶树

图8-7-3 汽车轮胎
■生活中的化学
涂料,通常我们称之为“漆”,是一种流动状态或粉末状态的、能均匀覆盖并牢固地附着在物体表面上的有机物质。人造漆又称“油漆”,是含有干性油、颜料和树脂的合成涂料。油漆有清漆、喷漆、调和漆、瓷漆和防锈漆等。油漆的成分一般包括成膜物质、溶剂和颜料三个部分。成膜物质是油漆的基础,它能使油漆在物体表面形成漆膜,油料、树脂(如天然树脂、合成树脂、硝化纤维)等都是成膜物质;溶剂是油漆的另一种重要成分,如乙醇、甲苯、二甲苯等能把成膜物质树脂变成稀薄的液体以便于刷漆和喷漆。
木质家具是家具环境中必不可少的一种用具,供存放衣物、食品、书籍及其他物件等。木制家具的表面都上有一层涂料,其作用不仅是为了美化表面,更重要的是为了保护家具,延长使用时间。因为家具制作时,木材虽然干燥处理,但由于木材比较稀疏,随着环境温度和湿度的变化会变形开裂。有些木材在加工成型后,表面有一种纹理清晰、色彩鲜艳的自然花纹,若长期暴露会氧化变质,失去原来的天然美,因此都需要涂料保护。所以说,涂料是人类现代生活的美容剂。
课堂反馈
1.选择题:
(1)下列物质中,属于合成高分子化合物的是( )。
A.有机玻璃 B.淀粉 C.蛋白质 D.棉花
(2)下列关于高分子化合物性质的说法中,正确的是( )。
A.只有线型结构的高分子化合物才具有弹性
B.高分子化合物中每个分子的相对分子质量是相同的
C.每个高分子中链节的数目叫做聚合度
D.无论何种结构的高分子化合物都具有可塑性
(3)通常所说的“白色污染”指的是( )。
A.聚乙烯等塑料垃圾 B.白色的建筑废料
C.炼制石灰时产生的白色粉尘 D.金属冶炼厂的白色烟尘
(4)不能用于商品包装的物质是( )。
A.聚乙烯 B.聚氯乙烯 C.聚丙烯 D.牛皮纸
2.填空题:
(1)高分子化合物简称__________,系指__________的化合物。在高分子里,每个特定的结构单元称为__________,其数目的多少称为__________。
(2)高分子化合物的基本特性主要有________、________、________和________等。
(3)__________、_________、_________,被称为用途广泛的“三大合成材料”。
(4)塑料分为__________塑料和__________塑料,前者为__________型高分子,后者为__________型高分子。
■知识链接
新型有机高分子材料
社会进步和科技发展极大地推动了高分子材料的改进和革新,以塑料、橡胶、纤维、薄膜、胶黏剂和涂料等为代表的传统材料已远远不能满足需要,新型有机高分子材料如雨后春笋不断涌现,它们或者使传统材料的结构、性能、价格、产量、寿命发生根本性的革命,或者因具备光、电、磁分离、生物智能等特殊功能而在各个尖端领域扮演着神奇的角色。这里,我们简单介绍几种重要的新型有机高分子材料。
一、功能高分子材料
所谓功能高分子材料,是在合成有机高分子材料的主链或支链上显示某种功能的官能团,使高分子具有特殊的功能,从而满足其在光、电、磁分离、生物智能、医学应用等方面的要求。
功能高分子材料的品种很多(如图8-7-4所示),有高分子膜、高分子吸附剂、医用高分子、超导高分子、光致变色高分子等。它们在物质分类、能量转换、环境保护、临床治疗、药物合成、日常生活以及军事和尖端科技等领域都得到了成功的应用。例如,由人造羊毛——聚丙烯腈和喷镀铝钛金属的反射膜制成的“太空棉”,由于具有优于鸭绒的高保暖性在市场上颇受青睐;由高吸水性高分子材料制成的婴儿纸尿片,在吸收超过自重几百倍甚至上千倍的水时只会体积膨胀,却不会因加压挤出水来,为众多家庭带来方便;而且,这种高吸水性高分子材料还是很好的保鲜包装材料、人造皮肤的适宜选料,并有可能用于防止土地沙化;而以硅聚合物和聚氨酯为代表的医用高分子材料更因为可用于制造人造皮肤、人造肌肉、人造器官、人造骨骼等,为人类健康和长寿作出了突出贡献。
二、复合高分子材料

图8-7-4 日常生活中常用的高分子材料
新型复合高分子材料是由两种以上物理和化学性质不同的物质,经人工组合而得的性能优良的多材质材料。近代的橡胶轮胎、钢筋水泥、玻璃钢、磁带、书籍的塑纸封面、洗衣机的塑钢等都属于这种新型材料。
复合高分子材料改善和克服了单一材料的诸多缺点,具有更加优异的综合性能。例如,由玻璃纤维和聚酯类树脂复合而成的“玻璃钢”,不仅强度远远超过普通钢材和合金钢材,隔热效果比金属高出成百上千倍,而且耐腐蚀、易成型、易加工;由酚醛树脂、聚乙烯醇缩丁醛树脂和芳纶压制而成的复合材料,可做成头盔、防弹板、防弹背心等,其保护性能较钢质材料提高三分之一。
高性能化和复合化使新型复合高分子材料在汽车工业、机械工业、体育用品、人类健康特别是宇航工业领域得到了极其广泛的应用。例如,集合了强度高于合金、质量轻于合金,且耐高温、耐高压、耐腐蚀等诸多优点的新型树脂复合材料就在美国“阿波罗”登月飞船上多处采用。
目前,新型有机高分子材料的研究正在不断加强和深入,高性能化、高功能化、复合化、智能化、精细化正日益成为今后新型有机高分子材料的研发方向。有理由相信,既充分利用资源,又能节约能源的新型有机高分子材料,不仅应用前景会越来越广阔,并必将作为未来的常规材料对人们的生产和生活产生越来越大的影响。
知识梳理
一、有机化合物的共同性质
A.多数熔、沸点______ B.多数______溶于水,____溶于有机溶剂
C.多数_____燃烧,受热______分解 D.多数不电离或者难电离,不导电
二、甲烷
1.结构:
分子式:____结构式:______结构简式:____空间构型:______
2.物理性质:没有颜色,没有气味,难溶于水的气体,密度0.717g/L(标准状况下)。
3.甲烷的化学性质:
(1)稳定性:通常条件下CH4与强氧化剂(KMnO4酸性溶液等)、强酸、强碱均不反应
(2)氧化反应:可燃性![]()
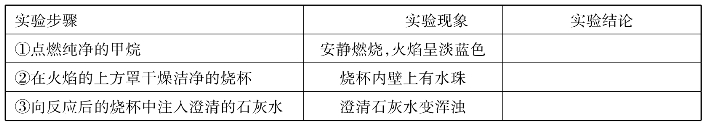
(3)取代反应:
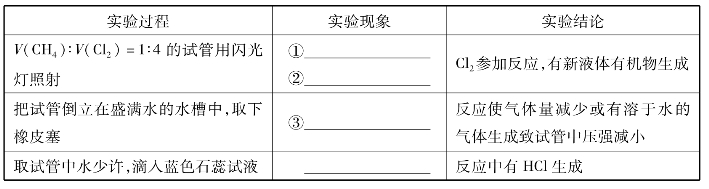
有机化合物分子中的某些原子(或原子团)被其他原子(或原子团)代替的反应。叫取代反应。
氯气与甲烷反应的说明:
A.反应条件:光照,在暗处不反应
B.反应物质:纯卤素单质,如甲烷与Cl2、溴蒸气光照条件下发生取代反应,与氯水、溴水不反应
C.反应产物:反应产物为多种有机物和无机物的混合物
D.有机产物的说明:四种氯代有机物均难溶于水,其中一氯甲烷气态,其余为油状液态,三氯甲烷曾被用作麻醉剂,三氯甲烷和四氯甲烷是重要的工业溶剂。
(4)分解反应:
①甲烷常温时很稳定,高温时可断键;
②甲烷的高温裂解反应方程式![]() 。
。
三、乙烯
(一)乙烯分子的组成和结构:
分子式:______ 结构式:______ 结构简式:_______
结构特点:碳原子间共价键是双键;乙烯分子属于平面型分子,即6个原子共面。
(二)乙烯的物理性质:
无色、稍有气味、______溶于水、密度比空气________的气体。
(三)乙烯的化学性质:
1.氧化反应:
(1)燃烧:________________________________
(2)乙烯能被KMnO4(H+)溶液氧化。
2.加成反应:有机化合物分子中双键上的碳原子与其他原子(或原子团)直接结合生成新的化合物分子的反应。
(1)与卤素单质加成:_______________________________
(2)与氯化氢加成:________________________________
(3)与氢气加成:________________________________
(4)与水加成:_______________________________
四、苯
(一)苯分子的结构
分子式:______ 结构式(凯库勒式):______ 结构简式:_______
结构特点:
①具有平面正六边形结构,所有原子均在同一平面上。
②苯环中所有碳碳键等同,是一种介于单键和双键之间的独特的键。
(二)苯的物理性质

(三)苯的化学性质和用途
1.稳定性:苯不能与溴的四氯化碳溶液发生加成反应而使其退色,也不能被酸性KMnO4溶液氧化而使其退色。
2.苯在空气里燃烧:_______________________________________
3.苯的取代反应:
(1)卤代反应(跟卤素单质):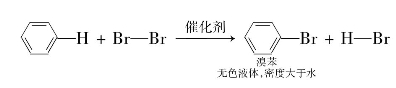
注意:①反应物:苯和液溴(不能用溴水)(https://www.xing528.com)
②反应条件:催化剂(FeBr3)
③除去溴苯中的溴,用NaOH溶液
(2)硝化反应:
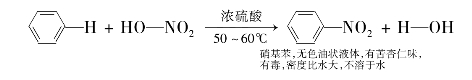
4.苯的加成反应:
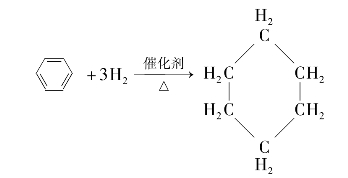
5.苯用途:
合成纤维、合成橡胶、塑料、农药、医药、染料、香料等。苯也常用于有机溶剂。
五、乙醇
1.乙醇的物理性质:
乙醇俗称_______,它是_______色透明、具有________的液体;沸点为78.5℃,易________;能与水以_______互溶,能溶解多种________,是优良的________。
2.乙醇的分子结构:
乙醇可看作是CH3CH3分子里的________被_______取代而形成的,也可看成是水分子中________被_______取代。分子式为_______,结构式为_______,结构简式为________或________,决定乙醇化学性质的原子团是________(名称是________)。
3.乙醇的应用:
(1)乙醇在空气中容易燃烧,发出________的火焰,放出大量的热,是一种很好的液体燃料。反应方程式为_________________________________________;乙醇与甲烷一样被称为“绿色能源”。
(2)乙醇可用作________、________、________、________等。医院里用________(体积分数)的乙醇溶液消毒。
4.工业酒精含有对人体有害的甲醇,结构简式为________________,甲醇会使人________、_______________,因此禁止用工业酒精配制饮用酒和调味用的料酒。
六、乙酸
1.乙酸的物理性质:
乙酸俗称_______,是食醋的主要成分,普通食醋中含有________(质量分数)的乙酸。乙酸是________色有强烈________气味的液体_______溶于水、乙醇等溶剂,沸点:117.9℃,熔点:16.6℃。当温度低于16.6℃时,无水乙酸易凝结成________的晶体,所以无水乙酸又称为________。
2.乙酸的分子结构:
化学式________,结构式________,结构简式_______,决定乙酸化学性质的原子团是_______,叫________。
3.油脂是一类特殊的___________,油脂分为____________和____________。油一般是从________里榨取出来的,呈________态;脂肪是________体内含有的,呈________态。油脂可看做由高级脂肪酸(硬脂酸_______、软脂酸_______、亚油酸________等)与甘油________经_______反应生成的酯,它在适当的条件下能发生 ________反应,生成相应的_______和________。油脂除可食用外,还可用于________和________等。
七、葡萄糖
葡萄糖的性质:
(1)在试管中加入2mL 5%NaOH溶液,滴加2%CuSO4溶液4~5滴,混匀(制得的物质称为新制的Cu(OH)2悬浊液),立即加入2mL 10%葡萄糖溶液,在酒精灯上加热,现象为________________________________葡萄糖这一性质的用途:
①_______________________________________________________________________
②_______________________________________________________________________
注意:NaOH溶液必须稍微过量。
八、蛋白质的性质
1.蛋白质的组成:
蛋白质是一类非常复杂的化合物,其分子中含有C、H、O、N、S等元素。蛋白质的相对分子质量很大,从几万到几千万,蛋白质属于天然高分子化合物。
2.蛋白质的化学性质:
(1)盐析——可逆过程——可分离提纯蛋白质
(2)变性——不可逆过程
(3)颜色反应——可鉴别蛋白质(特性)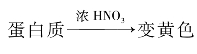 (严格地说,浓HNO3只能使含有苯环的蛋白质变黄色。)
(严格地说,浓HNO3只能使含有苯环的蛋白质变黄色。)
(4)灼烧时有烧焦羽毛的气味——可鉴别蛋白质
(5)蛋白质的水解:蛋白质的水解产物是氨基酸。

氨基酸分子中含有碱性基氨基(—NH2)和酸性基羧基(—COOH),氨基酸呈两性。天然蛋白质水解的最终产物都是α-氨基酸。
知识检测站
1.有机化学中的加成反应的原理类似于四种基本反应类型中的( )。
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
2.下列有机化合物中,既能使溴的四氯化碳溶液退色,又能使酸性高锰酸钾溶液退色的是( )。
A.甲烷 B.乙烯 C.甲苯 D.苯
3.石油炼制的方法较多,如:①分馏;②裂化;③裂解,其中属于化学变化的是( )。
A.只有② B.①② C.①③ D.②③
4.下列反应中,能说明乙烯的结构具有碳碳双键的是( )。
A.燃烧 B.加成反应 C.取代反应 D.能够催熟水果
5.下列有机化合物中含碳量最大的是( )。
A.甲烷 B.乙烷 C.乙烯 D.苯
6.下列物质能与镁反应生成氢气的是( )。
A.醋酸钠 B.醋酸溶液 C.苯 D.碳酸钠溶液
7.某有机物结构式为HO—CH2— =CH CHCH2—COOH,该有机物不可能发生的化学反应是( )。
A.水解 B.酯化 C.加成 D.氧化
8.下列说法中错误的是( )。
A.通常蔗糖和淀粉都不显还原性
B.油脂是热量最高的营养物质
C.纤维素分子是由葡萄糖单元组成的,可以表现出多元醇的某些性质
D.重金属的盐可以使蛋白质产生盐析现象
9.CH3COOH分别与CH3CH2OH和CH3CH218OH反应,生成的酯的相对分子质量大小关系为( )。
A.前者大于后者 B.前者小于后者 C.前者等于后者 D.无法确定
10.下列关于羟基和氢氧根的说法中,正确的是( )。
A.两者相同 B.羟基比氢氧根少一个电子
C.两者的组成元素相同 D.羟基比氢氧根性质稳定
11.下列说法正确的是( )。
A.凡符合Cn(H2O)m通式的化合物一定属于糖类,不符合此通式的不属于糖类
B.凡能溶于水且具有甜味的化合物都属于糖类
C.葡萄糖是一种单糖的主要原因是它是一种多羟基醛
D.葡萄糖分子中含有醛基,它具有还原性
12.为了促进脂的水解,可以采取的最有效的措施是( )。
A.增加酯的用量 B.增加水的用量
C.加热 D.加入氢氧化钠溶液并加热
13.下列叙述不正确的是( )。
A.天然蛋白质水解的最终产物是α-氨基酸
B.所有的蛋白质遇到浓硝酸都变黄
C.人工最早合成的具有生命活力的蛋白质——结晶牛胰岛素是中国科学家在1965年合成的
D.可以用灼烧法来鉴别蛋白质
14.下列变化属于取代反应的是( )。
A.硝酸银溶液与盐酸的反应 B.甲烷的燃烧
C.铝与氢氧化钠溶液的反应 D.由甲烷制取四氯化碳
15.根据表中A,B,C,D四种固体样品的性质推测,其中最可能是有机物的是( )。
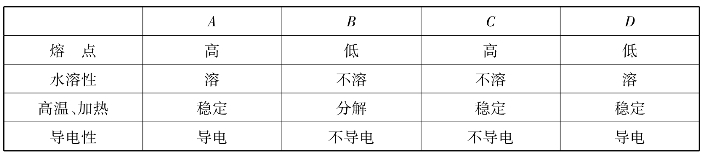
16.下列关于甲烷的说法正确的是( )。
A.甲烷分子中C、H间是离子键 B.甲烷分子是空间正方体结构
C.甲烷的结构式为CH4 D.甲烷分子中4个碳氢键是完全等同的
17.下列物质,常温下呈气态的是( )。
A.CH3Cl B.CH2Cl2 C.CHCl3 D.CCl4
18.下列说法中错误的是( )。
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
A.①②③④ B.只有②③ C.只有③④ D.只有①②③
19.在光照条件下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是( )。
A.CH3Cl B.CH2Cl2 C.CCl4 D.HCl
20.将下列气体通入酸性高锰酸钾,酸性高锰酸钾退色的是( )。
A.CH4 B.CO2 C.SO2 D.H2
21.同分异构体现象在有机化学中是非常普遍的,下列有机物互为同分异构体的是( )。
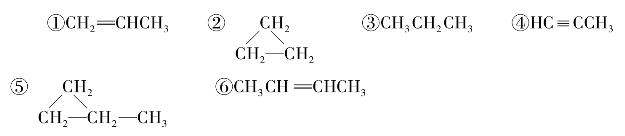
A.①和② B.①和③ C.①和④ D.⑤和⑥
22.关于取代反应和置换反应的下列说法中,正确的是( )。
A.取代反应和置换反应中一定都有单质生成
B.取代反应和置换反应一定都属于氧化还原反应
C.取代反应大多是可逆的,反应速率慢,而置换反应一般是单向进行、反应速率快
D.取代反应和置换反应的产物都是唯一的,不会有多种产物并存的现象
23.有下列几种物质的结构式:
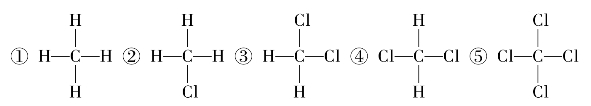
其中具有正四面体结构的有__________,属于同一种物质的是______和______。(填序号)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




