在化学实验中经常要用到溶液,我们有时用溶质的质量分数来表示溶液的组成。为了操作方便,一般取用溶液时并不是称量它的质量,而是量取它的体积。在化学反应中,反应物和生成物之间的比例关系是由化学方程式中的化学计量数所决定的。如果知道一定体积的溶液中溶质的物质的量,对于计算化学反应中各物质之间量的关系是非常便利的,对生产和科学研究也有重要的意义。
我们使用物质的量浓度这个物理量,来表示单位体积溶液里所含溶质B的物质的量,也称为B的物质的量浓度,符号为cB。物质的量浓度可表示为:


图2-3-1 几种规格的容量瓶
物质的量浓度常用的单位为mol/L,(或mol·L-1)。如果1L溶液中含有1mol溶质,这种溶液中溶质的物质的量浓度就是1mol/L。
我们知道了物质的量与质量之间的关系,以及用物质的量和溶液体积来表示溶液的组成,就可以在实验室配制一定物质的量浓度的溶液。
例 配制500mL 0.1mol/L NaOH溶液需要NaOH的质量为多少?
解 500mL 0.1mol/L NaOH溶液中NaOH的物质的量为:

0.05mol NaOH的质量为:
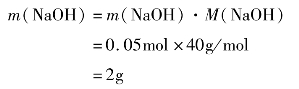
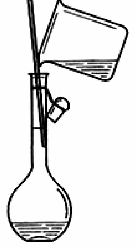
图2-3-2 向容量瓶中转移溶液
在实验室,我们可以直接用固体或液体试剂来配制一定物质的量浓度的溶液。如果要求比较精确,就需要使用容积精确的仪器,如容量瓶。容量瓶有不同的规格,常用的有100mL、250mL、500mL和1000mL。
【实验2-2】配制100mL 1mol/L NaCl溶液。
(1)计算需要NaCl固体的质量:_________g。
(2)根据计算结果,称量NaCl固体。(https://www.xing528.com)
(3)将称好的NaCl固体放入烧杯中,用适量的蒸馏水溶解。
(4)将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀。
(5)将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线相切。盖好瓶塞,反复上下颠倒。摇匀。

图2-3-3 配制一定物质的量浓度的溶液过程示意图
思考与交流
1.为什么要用蒸馏水洗涤烧杯,并将洗涤液也注入容量瓶?
2.如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求的大了还是小了?
3.你是用什么仪器称重NaCl固体的?如果是托盘天平,你称量的质量是多少?与计算量一致吗?为什么?
不同的物质具有不同的性质,同一物质的溶液浓度不同时,有时在某些性质上也会表现出差异。我们在实验室做化学实验或进行科学研究时,需要根据不同的情况选择不同浓度的溶液进行实验。所以,在实验室不仅用固体物质来配制溶液,还经常要将浓溶液稀释成不同浓度的稀溶液。
思考与交流
1.以硫酸为例,讨论不同浓度的溶液在性质上可能会出现什么差异。
2.如果将5mL浓硫酸稀释为20mL的稀硫酸,得到的稀硫酸与原浓硫酸中所含H2SO4的物质的量相等吗?能说出你的理由吗?
在用浓溶液配制稀溶液时,常用下面的式子计算有关的量:
c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液)
在稀释浓溶液时,溶液的体积发生了变化,但溶液中溶质的物质的量不变,即在溶液稀释前后,溶液中溶质的物质的量相等。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




