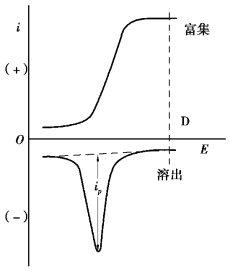
图15.1 阳极溶出伏安法极化曲线
溶出伏安法(stripping voltammetry)包含电解富集和电解溶出两个过程。首先是电解富集过程。它是将工作电极固定在产生极限电流电位(图15.1中D 点)上进行电解,使被测物质富集在电极上。为了提高富集效果,可同时使电极旋转或搅拌溶液,以加快被测物质输送到电极表面,富集物质的量则与电极电位、电极面积、电解时间和搅拌速度等因素有关。
其次是溶出过程。经过一定时间的富集后,停止搅拌,再逐渐改变工作电极电位,电位变化的方向应使电极反应与上述富集过程电极反应相反。记录所得的电流-电位曲线,称为溶出曲线,呈峰状,如图15.1所示,峰电流的大小与被测物质的浓度有关。
例如在盐酸介质中测定痕量铜、铅、镉时,首先将悬汞电极的电位固定在-0.8 V,电解一定的时间,此时溶液中的一部分Cu2+、Pb2+、Cd2+在电极上还原,并生成汞齐(汞合金),富集在悬汞电极上。电解完毕后,使悬汞电极的电位均匀地由负向正变化,首先达到可以使镉汞齐氧化的电位,这时,由于镉的氧化,产生氧化电流。当电位继续变正时,由于电极表面层中的镉已被氧化得差不多了,而电极内部的镉还来不及扩散出来,所以电流就迅速减小,这样就形成了峰状的溶出伏安曲线。同样,当悬汞电极的电位继续变正,达到铅汞齐和铜汞齐的氧化电位时,也得到相应的溶出峰。如图15.2所示。
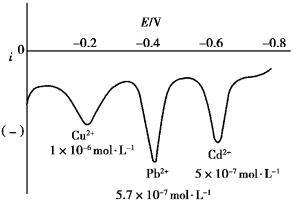
图15.2 盐酸底液中镉、铅、铜的溶出伏安曲线(https://www.xing528.com)
在这里,电解富集时,悬汞电极作为阴极,溶出时则作为阳极,称之为阳极溶出法。相反,悬汞电极也可作为阳极来电解富集,而作为阴极进行溶出,这样就称为阴极溶出法。
溶出伏安法的全部过程都可以在普通极谱仪上进行,也可与单扫描极谱法和脉冲极谱法结合使用,其方法灵敏度很高,可达到10-7~10-11 mol/L,特别适用于痕量分析。其主要原因是由于工作电极的表面积很小,通过电解富集,使得电极表面汞齐中金属的浓度相当大(100~1 000倍),起了浓缩的作用,所以溶出时产生的电流也就很大。已有30 多种元素可以通过阳极溶出伏安法测定。
传统的阳极溶出伏安法是以汞电极作为工作电极,需要采用悬汞或汞膜电极作为工作电极,汞是有毒重金属元素,分析操作过程对用户和环境存在潜在威胁,其在水质分析领域的应用受到很大的限制。
使用铋膜电极对仪器的最低检测限有影响,但完全能满足环境分析。采用镀铋膜方法,可以完全避免汞的使用。使用铋膜电极作为工作电极在重金属在线分析仪上运用有重要意义。除了铋膜电极,也有用铋合金电极作为工作电极用于阳极溶出伏安法进行检测。
检测砷、汞等元素时,不适合用汞电极和铋电极作为工作电极,通常使用金电极或金膜电极作为工作电极,在配套的电解质底液中,使用阳极溶出伏安法能较好地检测痕量的砷、汞元素。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




