尽管pH值可以通过多种方法测量得出,对于pH 电极而言,为了产生电势差,必须形成完整的电流回路。完整的电流回路是由插入同一溶液中的指示电极和参比电极构成,图3.2所示为参比电极和指示电极集成在一起的复合电极的结构,图3.3所示为pH 复合电极中玻璃膜电极的结构示意图。
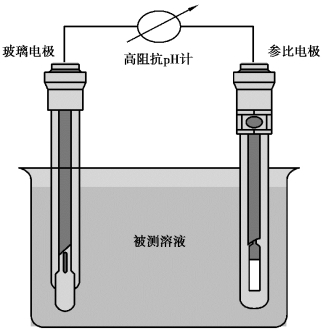
图3.2 pH 复合电极示意图
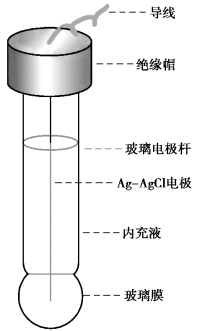
图3.3 玻璃膜电极结构示意图
无论待测溶液的组成如何,参比电极的功能主要是提供恒定电位;指示电极对氢离子敏感度高,主要功能是测量由于溶液中氢离子的存在而引起的电位变化。通过pH 和电位关系的校准曲线,可以将两个电极之间的电位差转化为溶液的pH值。
在能斯特公式中温度“T”作为变量,作用很大。随着温度的上升,电位值将随之增大。对于每1 ℃的温度变化,将引起电位0.2 mV/pH 变化。则每1 ℃每1pH 变化0.003 3pH值。这也就是说:对于20~30 ℃和pH=7 左右的测量来讲,不需要对温度变化进行补偿;而对于温度>30 ℃或>20 ℃和pH>8 或6 的应用场合则必须对温度变化进行补偿。
现代的pH值检测采用差分传感器技术,使用三个电极取代传统的PH 传感器中的双电极。测量电极和标准电极都与第三个地电极测量电位,最终测出的pH值是测量电极和标准电极之间电位差值。该技术大大提高了准确性,消除了参比电极的结点污染后造成的电位漂移,如图3.4所示pH 电极结构。
最常用的pH 电极称为复合电极,即参比电极和指示电极集成在一个电极上,其各个组成部分及作用如下。
(1)参比电极
参比电极包含一个浸入参比电解质溶液中的参比单元,这个参比单元与待测溶液中的电解质构成一个电路连接。
参比电解质溶液通过一个多孔介质或者隔膜(有时称为“盐桥”)与待测溶液构成电路连接,该多孔介质或“盐桥”可以从物理上将内部电解质溶液与外部待测溶液隔离开。
最常用的参比电极是表面涂有固体氯化银(AgCl)的银电极(Ag)。选用银作电极的金属材料,原因在于:在所有金属中,银的导电性能最佳,电阻最小;氯化银(AgCl)的作用是提供一个稳定的参比电压。
(2)盐桥或多孔介质(https://www.xing528.com)
多孔介质或盐桥为参比电解液和待测溶液接触提供了一个微小的通道,但是不允许参比电解液和待测溶液相互混合。多孔介质或盐桥的作用是为参比电解液和待测溶液创造一个理想的接触条件。
(3)参比电解液
参比电解液主要作用是连接待测样品和pH 计,其浓度必须非常高以减小电极电阻,保证在一定的温度范围内保持一个稳定的参比电极电位,从而不影响待测溶液的pH 测量。最常用的参比电解液为饱和氯化钾(KCl)溶液。
氯化钾在20 ℃的溶解度是34 g,故20 ℃下饱和氯化钾溶液浓度为25.37%。
(4)温度传感器
为获得准确的测量值,pH 传感器必须补偿因能斯特方程中温度变化的影响。
(5)指示电极
指示电极是一种由特殊的玻璃材料烧结而成,该玻璃材料对氢离子浓度响应敏感,这种玻璃的主要成分为非结晶态的二氧化硅,掺入了一些碱金属氧化物,主要是金属钠(Na)的氧化物,即氧化钠(Na2O)。
当玻璃表面与水接触后,玻璃中的碱金属离子(Na+)以及溶液中的氢离子(H+)之间发生离子交换反应。一层非常薄的水合凝胶层在玻璃外表面形成,同时在玻璃泡内侧与内部缓冲溶液接触的表面也形成薄薄的一层水合凝胶层。
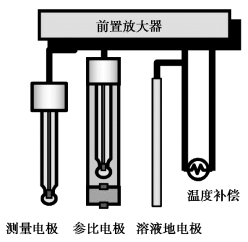
图3.4 pH 电极结构
氢离子迁出或迁入水合凝胶层取决于待测溶液中氢离子的浓度。在碱性待测溶液中,氢离子从水合硅凝胶层中迁出,因此在水和硅胶层的外层产生负电荷;在酸性待测溶液中,氢离子迁入水合硅胶层,因此,在水合硅胶层中的外表面产生正电荷。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




