在逆向合成分析中,只变更官能团的种类或位置而不改变碳架的变换称为逆向官能团变换。逆向官能团变换主要包括逆向官能团的互换和逆向官能团的添加。官能团变换的目的是:(1)为了便于逆向切断、逆向重接和逆向重排等变换,将目标分子上原有不合适的官能团变换成合适的官能团,或者添加必需的官能团;(2)为了提高区域选择性或立体选择性,在碳架适当的位置添加致活、导向、阻断等基团。
1.醛酮的逆向官能团变换
醛酮常逆向变换成醇,然后切断。脂肪族醛酮也可变换成硝基化合物,其正向反应是Nef反应,因此脂肪族化合物中的硝基是隐藏的羰基。酮也可变换成炔,其正向反应是炔的水合。
醛的逆向转换如下:
伯醇氧化生成生醛是醛的主要生成途径:
醇氧化生成醛,可选用三氧化铬—吡啶/二氯甲烷等特殊的氧化剂,从而使醛不进一步被氧化成酸而停留在醛。
烯和炔也是转换为醛一个主要途径,如下所示:
酮的逆向转换如下:
Nef反应如下所示:
烯烃还可以通过臭氧的氧化生成醛或酮及羧酸:
2.烯键的逆向官能团变换
醇、卤代烃、季铵盐、羧酸酯、黄原酸酯及氧化叔胺等通过消除反应生成烯烃。这里主要介绍前面三种常用方法。
卤代烃脱卤化氢具有反应条件温和、选择性好、新试剂易开发的优点,迄今仍是合成烯烃的常用方法之一:
卤代烃脱HX的消除方向一般来说是遵从Saytzeff(查依采夫)择向规则的,即优先生 成热力学稳定的多取代烯烃。
醇的脱水亦是合成烯烃的常用方法。常用的脱水剂有酸(如硫酸、磷酸、草酸等)、酸性氧化物(如P2O5)等。其中,酸催化脱水最为常见。易遵守Saytzeff规则:
季铵盐及其碱的热解:胺经彻底甲基化生成季铵盐,然后用碱处理(常用的碱有湿Ag2O、NaOH、C2H5ONa等)得到季铵碱,季铵碱加热进行热分解得到烯烃。该反应称为Hofmann消除反应。
炔烃通过催化加氢而生成烯烃:
3.羧酸的逆向官能团变换
羧酸主要途径是醛或伯醇的氧化,还有腈的水解。
4.醇的逆向官能团变换
烯烃在碱性高锰酸钾条件下氧化生成顺式邻二醇,在过氧酸作用下先生成环氧化物,再在碱性或酸性条件下生成反式邻二醇,如下例:(https://www.xing528.com)
在稀硫酸催化下水解下遵守马氏规则生成醇,但在硼氢化后,加碱性的双氧水生成反马式的醇:
醛酮在还原剂如硼氢化钠和四氢锂铝作用下被还原为醇:
羧酸在四氢锂铝作用下生成伯醇:
醚在HX作用下也生成醇,酯和酸酐等也能被还原生成醇。
5.卤代烃的逆向官能团转换
常见的形成C—X(Cl、Br、I)键的反应主要包括不饱和烃的亲电加成、芳烃的亲电取代、醇(醚)的亲核取代以及自由基反应等。
烃基在光照的情况下与卤素发生游离基的取代反应。下图C—H键有多种。给氢标上数字,处于不同环境下的H原子发生游离基取代的优先顺序为H1>H5>H2>H3>H4,结构发生游离基取代的为H1原子。
芳香苯在路易斯酸的催化下,卤素与芳香苯发生亲电取代反应,如下所示:
羰基边的α-碳原子上的氢可发生卤代反应,如下所示:
烯烃、炔烃和HX、X2发生亲电加成反应,溴化氢在双氧水条件下发生反马式加成。
醇(C—OH)中的羟基被卤素取代生成卤烃(C—X)键。将醇转变成卤代烃的卤化剂有HX、PX3、PX5、SOCl2等,这些试剂不适于对酸敏感的醇。将醇在温和条件下转变为卤代烃的方法是将醇先转变成烷氧基膦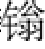 盐中间体。反应机理如下:
盐中间体。反应机理如下:
由于烷氧基膦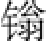 盐形成时烷氧键并不断裂,溴离子从手性醇背面进攻导致构型翻转。例如:
盐形成时烷氧键并不断裂,溴离子从手性醇背面进攻导致构型翻转。例如:
三苯基膦与四氯化碳、四溴化碳、六氯丙酮作用也生成卤代三苯基鏻盐,后者与醇反应也形成烷氧基三苯膦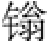 盐,因此也可以制备相应的卤代物:
盐,因此也可以制备相应的卤代物:
以上的卤代反应是SN2机理,反应产物产生构型翻转。反应具有化学选择性,除了酸性氢外,其他的官能团不受影响,同时也没有重排副反应发生。
将醇转为卤化剂的另一类重要试剂有磺酸酯类(由磺酰氯和醇在吡啶或三乙胺存在下反应)。常用的磺酸酯类有对甲苯磺酸酯、甲磺酸酯、三氟甲磺酸酯。
烯丙醇转变为卤代烃往往发生重排。克服这一缺点的方法是将醇先转变为磺酸酯,然后与卤素负离子发生亲核取代反应,例如:
【例】设计合成化合物:
分析:
合成:
或
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




