从消防观点来说,闪燃是可燃液体和某些固体可燃物发生火灾的危险信号,闪点是评价可燃液体火灾危险性的主要参数。液体的闪点越低,火灾危险性越大。几种易燃和可燃液体的闪点见表5-1。
表5-1 几种易燃和可燃液体的闪点 (单位:℃)
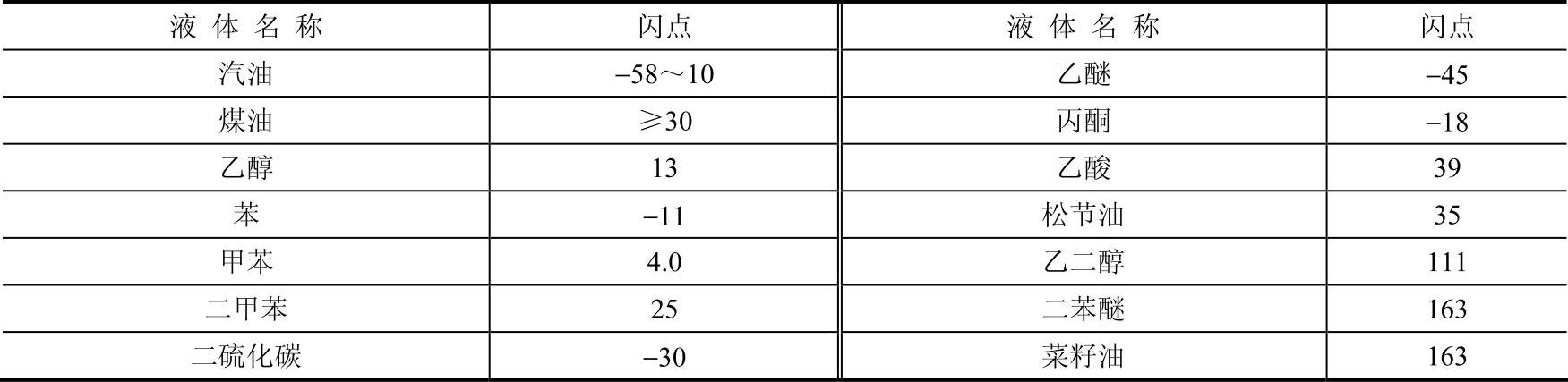
一般地说,可燃液体多数是有机化合物。根据其分子结构不同,有机化合物分成若干同系物。每类同系物中可燃液体的闪点都有一定的变化规律。
(一)同类(同系物)易燃和可燃液体的闪点
(1)同系物液体的闪点,随其分子量的增加而升高。
(2)同系物液体的闪点,随其沸点的增加而升高。
(3)同系物液体的闪点,随其密度的增加而升高。
(4)同系物液体的闪点,随其蒸气压的降低而升高。
例如,部分醇类和芳烃类的闪点与其摩尔质量、密度、沸点和蒸气压力的关系见表5-2。
表5-2 部分醇类和芳烃类的闪点与其摩尔质量、密度、沸点和蒸气压的关系
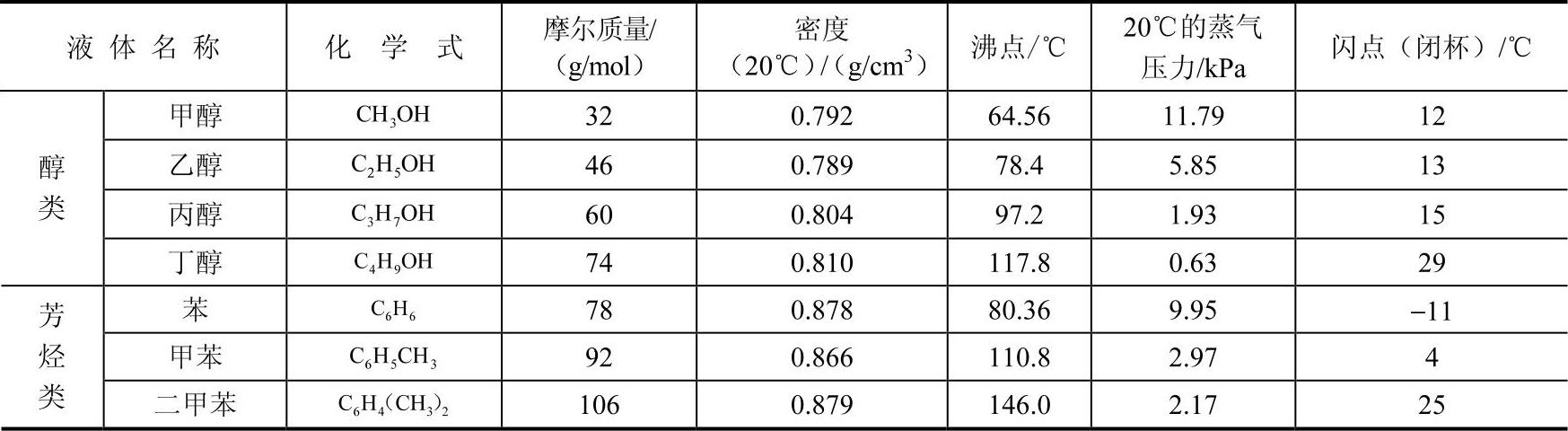
汽油的闪点随着馏分温度的提高而升高更为明显,见表5-3。
表5-3 汽油的闪点与馏分的关系 (单位:℃)
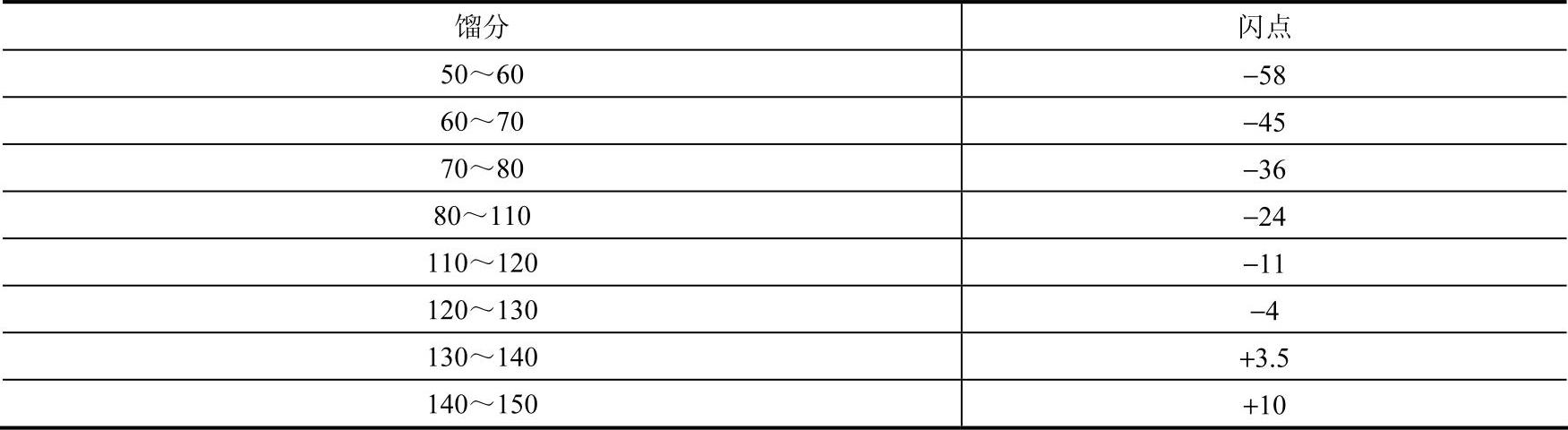
(5)同分异构体中,正构体比异构体闪点高,见表5-4。
表5-4 部分正构体与异构体的闪点比较 (单位:℃)(https://www.xing528.com)
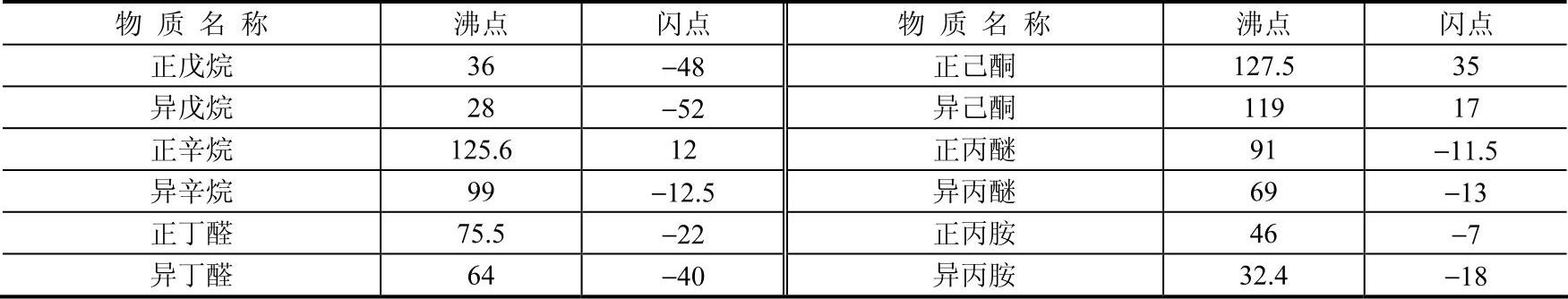
之所以同系物的闪点有这些变化规律,是由于分子间范德华力作用的不同造成的。摩尔质量的增大表明分子中原子数增加了,而原子数增多,分子间范德华力也就增大,结果造成液体的沸点增高,蒸气压降低,密度增大,闪点升高。相同碳原子数的异构体中,支链数增多,造成空间阻碍增大,使分子间距离变远,从而分子间的范德华力减弱,结果沸点降低,闪点下降。
(二)混和液体的闪点
1.完全互溶的两种可燃性液体的混合物
这类混合液体的闪点一般低于各组分闪点的平均值,并且接近于混合物中含量较大的组分的闪点。例如,甲醇和乙酸戊酯的混合物,纯甲醇的闪点为12℃,纯乙酸戊酯的闪点为28℃,当60%的甲醇与40%的乙酸戊酯混合时,其闪点并不等于(12×60%+28×40%)℃=18.4℃,而为10℃,如图5-1所示。甲醇和丁醇(闪点29℃)1:1的混合液的闪点不是(12+29)/2℃=20.5℃,而是13℃,要比平均值低,如图5-2所示。又如,车用汽油的闪点为-38℃,灯用煤油的闪点为40℃,如果将这两种液体按1:1比例混合时,其闪点低于(-38+40)/2℃=1℃。有人曾做实验发现,在煤油中加入1%的汽油,可使煤油的闪点降低10℃以上。可见,如果往可燃液体中添加闪点更低的可燃液体,即使加入的量不多,也能大大降低可燃液体的闪点,增大其火灾危险性。
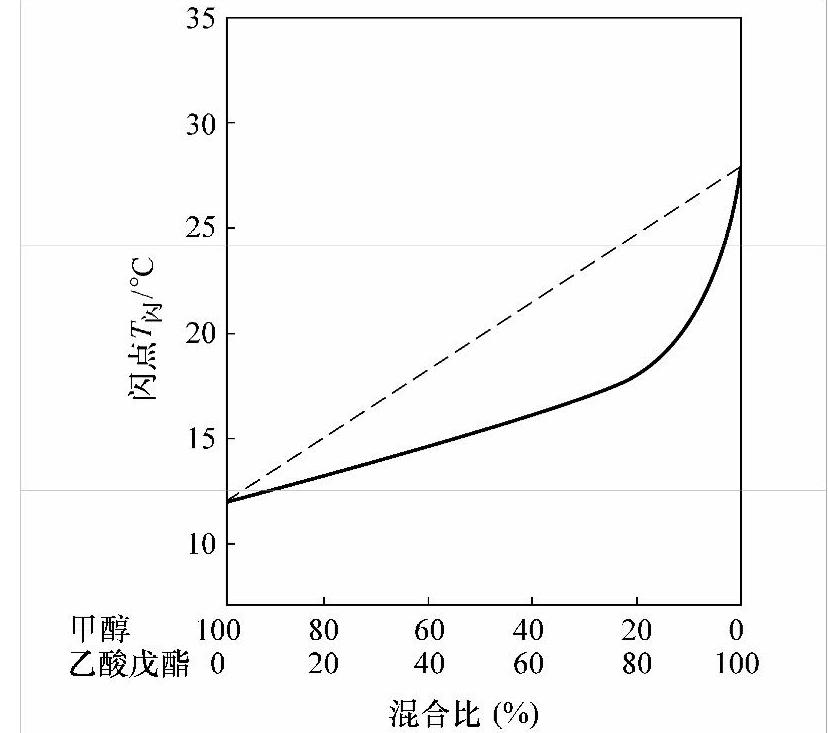
图5-1 甲醇与乙酸戊酯混合液的闪点
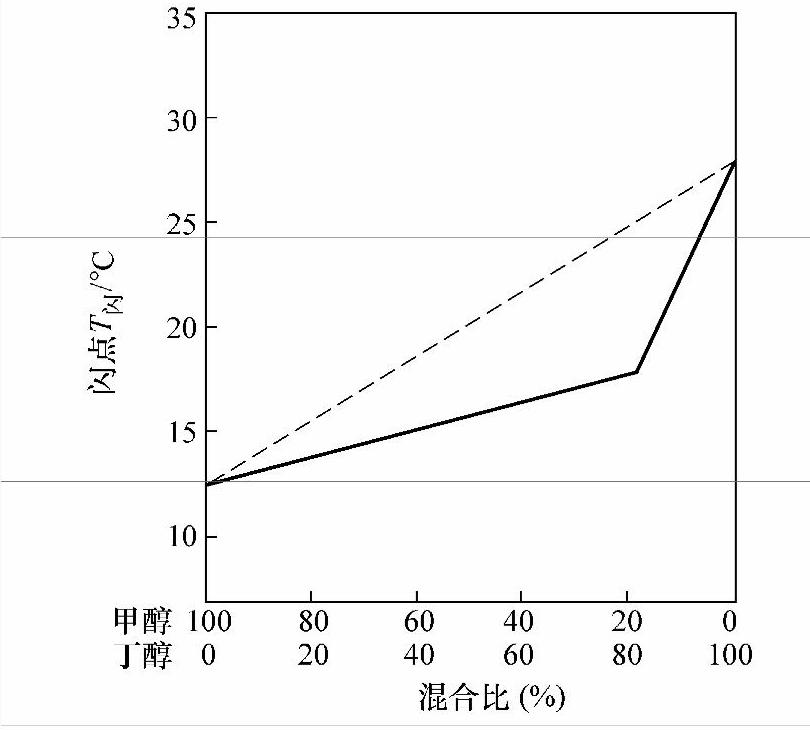
图5-2 甲醇和丁醇混合液的闪点
2.完全互溶的可燃液体与不燃液体的混合物
可燃液体与不燃液体的混合物,其闪点将随着不燃液体含量的增加而升高。当不燃组分含量达到一定值时,混合物不再发生闪燃。这类混合物常见的有甲醇与水、乙醇与水,丙酮与水以及甲醇与四氯化碳等。醇与水混合液体的闪点变化见表5-5。
表5-5 醇与水混合液体的闪点变化
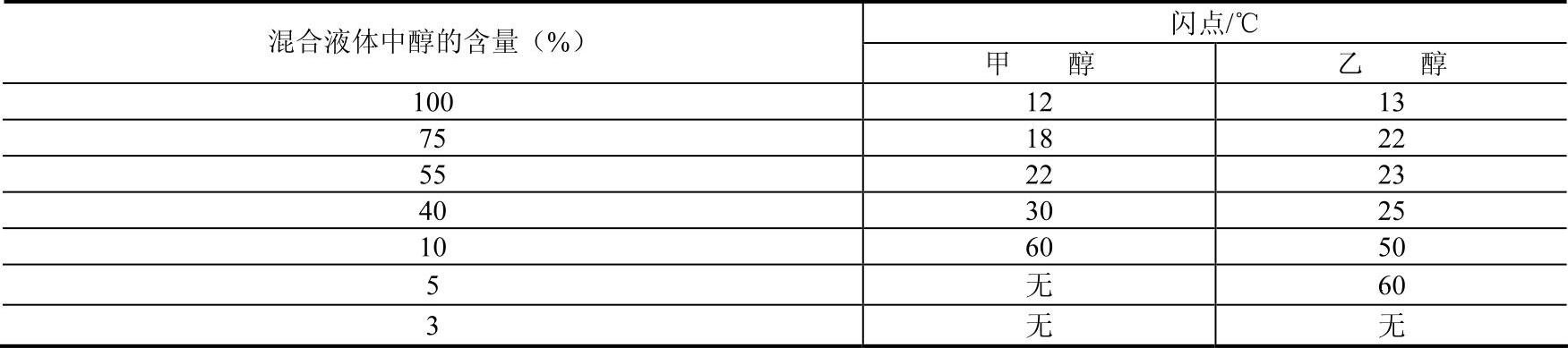
从表5-5中可以看出,能溶于水的醇闪点,随含水量的增加而提高。对于乙醇的水溶液,当醇的含量为40%时,其闪点将由纯乙醇时的13℃升至25℃;当醇的含量只占3%时,就不再发生闪燃。
所以,对于能溶于水的可燃液体的火灾,用水稀释,虽然能提高其闪点,但只有当溶液极稀时,才能使其不再发生闪燃。若可燃液体数量较多时,并不适宜用水稀释法来灭火,因为在这种情况下,不但可燃液体在火灭后不能再使用了,而且稀释需要大量的水,容易使液体溢出容器,造成火势蔓延扩大。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




