【摘要】:设有一个球形容器,体积为V,表面积为F,内部充满某种反应热为ΔH的可燃预混气体,现对其放热和散热进行分析。根据燃烧反应速度方程可知,化学反应速度Ws与混气温度T成指数关系,所以Q放是混气温度的指数函数,而Q散则与混气温度成正比例关系。将Q放和Q散分别对混气温度T作图即得到放热曲线和散热曲线,如图4-3所示。
设有一个球形容器,体积为V,表面积为F,内部充满某种反应热为ΔH的可燃预混气体,现对其放热和散热进行分析。为使问题简化,作如下假设:
1)环境温度为T0,反应开始时混气温度与环境温度相同,反应过程中混气的瞬间温度为T。
2)反应开始时容器的壁温与环境温度T0相同,反应过程中,壁温升高,与混气温度相同。
3)反应过程中,容器内既无自然对流,也无强迫对流,容器内各点的温度、浓度相同。
4)着火前反应物浓度变化很小,近似认为不变。
5)环境与容器之间有对流换热,表面传热系数为α,它不随温度变化。
该分析模型的简化示意图如图4-2所示。
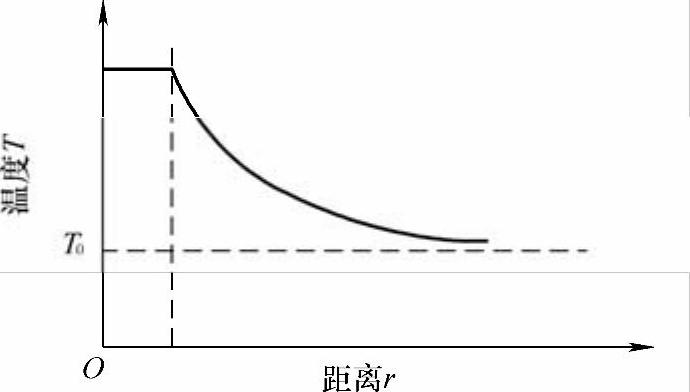
图4-2 热自燃理论分析模型的简化示意图
用Q放表示混气在单位时间内由化学反应放出的热量,即放热速度,用Q散表示混气在单位时间内向外界环境散发的热量,即散热速度,则(https://www.xing528.com)
Q放=VΔHWs (4-2)
Q散=αF(T-T0) (4-3)
式中 ΔH——可燃预混气体的化学反应热;
Ws——可燃预混气体的化学反应速度;
T——可燃预混气体温度。
根据燃烧反应速度方程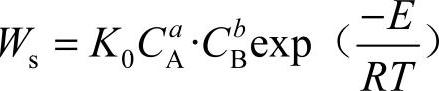 可知,化学反应速度Ws与混气温度T成指数关系,所以Q放是混气温度的指数函数,而Q散则与混气温度成正比例关系。将Q放和Q散分别对混气温度T作图即得到放热曲线和散热曲线,如图4-3所示。不难理解,当混气浓度不同时,反应速度Ws不同,因而可得到一组放热曲线;当环境温度T0不同时,可得到一组平行的散热曲线;当改变αF时,可得到一组斜率不同的散热曲线。
可知,化学反应速度Ws与混气温度T成指数关系,所以Q放是混气温度的指数函数,而Q散则与混气温度成正比例关系。将Q放和Q散分别对混气温度T作图即得到放热曲线和散热曲线,如图4-3所示。不难理解,当混气浓度不同时,反应速度Ws不同,因而可得到一组放热曲线;当环境温度T0不同时,可得到一组平行的散热曲线;当改变αF时,可得到一组斜率不同的散热曲线。
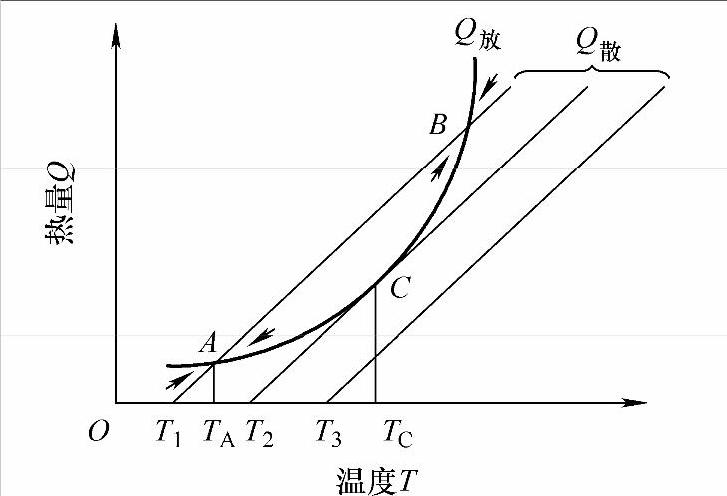
图4-3 放热曲线与散热曲线
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




