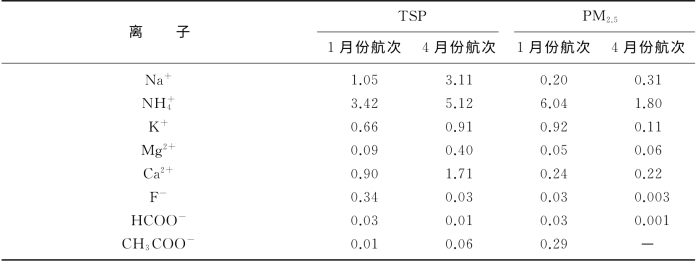
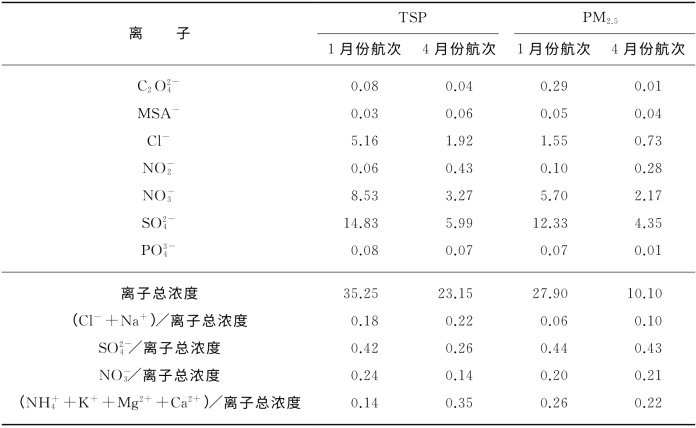
表6-4给出了2个航次中TSP和PM 2.5中的离子浓度。在1月份航次的TSP中,海盐(Cl-和Na+)占了总离子的18%,而SO24-和NO 3-分别占了42%和24%,NH 4+、K+、Mg2+和Ca2+一共占了14%。在4月份,则为海盐(Cl-和Na+)22%,而SO 24-和NO 3-分别占了26%和14%,NH 4+、K+、Mg2+和Ca2+一共占了35%。在PM 2.5中,1月份SO24-和NO 3-分别占总离子的44%和20%,4月份分别为43%和21%。离子在2个航次中有明显不同,无论在TSP还是PM 2.5中,大多是1月份高,4月份低。1月份干冷的气团控制和来自内陆的北风影响,给海洋地区带来大量的内陆污染,而4月份有比较湿润的天气,湿清除起到显著的作用,故1月份航次的离子浓度显著高于4月份。
表6-4 TSP和PM2.5中主要离子的浓度值(μg·m-3)
(续表)
1.海洋氮营养盐的主要组分NO 3-和NH 4+
海洋初级生产力增加的主要因素,是氮营养盐的注入[39 42]。大气中的NO 3-,是一系列氮氧化物(NO+NO2)的最终氧化产物,其主要来源是化石燃料的燃烧、机动车尾气的排放以及一些天然植物的固氮过程[43]。大气中的NH 4+主要来自NH 3的转化,而NH 3主要来源于动物排放的废弃物、施肥过程、土壤的释放和工业排放[44]。海洋大气中NO3-和NH 4+的沉降,是海洋氮营养盐的主要来源,对海洋生态的影响非常大。表6-5列出了2个航次测得的NO3-和NH 4+。在4月份航次中,NO3-和NH 4+的平均浓度分别为2.2μg·m-3(0.8~5.1μg·m-3)和2.0μg·m-3(0.8~3.6μg·m-3);在1月份航次中,NO3-和NH 4+的平均浓度分别为5.7μg·m-3(0.3~10.5μg·m-3)和6.0μg·m-3(0.8~8.7μg·m-3)。
表6-5 PM 2.5中NO3-和NH4+的浓度

NO-3的形成,可能是由于溶解的NO 2和HNO 3在碱性的海盐液滴中发生反应而产生的[45]。
![]()
NH 4+则是由于工农业污染排放出的挥发性NH 3通过气相反应而产生,然后凝结在细颗粒物中[46,47]。由于高浓度的NH 4+总是和SO 24-共存于颗粒物中,因此推测,一个可能的反应机理是:NH 3和一些酸性气体(如SO2)在颗粒物表面发生反应,形成稳定的(NH 4)2 SO 4。这是经由气相反应、异相反应和液相反应而产生的典型的二次污染物[43]。H.Zhuang等[48]对香港的一个海岸采样点的气溶胶进行研究,发现NH 4+和SO 24-都分布在粒径大约0.5~0.7μm范围内。而在美国的一个海岛,L.Zhuang等[49]对采集的污染气溶胶进行分析,发现NH 4+和SO24-都叠加在粒径大约0.3~0.4μm的范围内。可见,颗粒物中的NH 4+和SO24-是共生的,很可能是由NH 3和H 2 SO4发生反应产生的。从表6-4还可以发现,NH 4+在PM 2.5中的浓度,要高于在TSP中的浓度,主要是由于在粗颗粒物中,NH 4+容易挥发损失[50,51]。
2.海洋气溶胶中的非海盐硫酸盐和甲基磺酸
硫酸盐是酸沉降的主要贡献者之一,可以破坏建筑物和植物,导致生态系统p H的改变[52]。最近的研究表明,硫酸盐的干沉降占其总沉降(干和湿沉降)的70%[53]。根据非海盐硫酸盐(non-sea-salt-sulfate,nss-sulfate)的浓度计算公式nss-SO 24-=[SO 24-]-[Na+]×0.251 6[54],对于TSP样品,1月份航次中非海盐硫酸盐的平均值为14.6μg·m-3(3.9~29.8μg·m-3),占总硫酸盐的86%~99%;在4月份的航次中为5.2μg·m-3(1.0~15.7μg·m-3),占总硫酸盐的39%~98%。而在PM 2.5中,1月份的平均值为12.3μg·m-3(3~20.0μg·m-3),占总硫酸盐的96%~99%;4月份为4.3μg·m-3(0.3~8.3μg·m-3),占总硫酸盐的81%~99%。Q.Ma等[55]在南海北部地区3个航次调查结果的非海盐硫酸盐值为6.3μg·m-3,香港沿岸地区TSP样品中的年均值为8.04μg·m-3,两者的值均介于我们得到的1月份和4月份的均值之间。
二甲基硫(DMS)是海洋生物排放到大气中的含S气体,被认为是大洋地区云凝结核(CCN)的主要前体,从而影响地球的反照率和气候变化[56]。DMS一旦被释放到空气中,会发生一系列的气相和多相化学反应。在气相中,它白天会跟氢氧根自由基OH和卤素自由基等发生反应,夜间会跟硝酸根自由基发生反应[57,58]而生成硫酸盐或者甲基磺酸(MSA)。在北太平洋地区,海洋生物排放产生的非海盐硫酸盐和MSA的比值(非海盐硫酸盐/MSA)是18。到目前为止,还没有人调研过南海上空气溶胶中的MSA。在南海北部地区,PM2.5气溶胶中MSA的平均浓度为0.048μg·m-3(1月份)和0.043μg·m-3(4月份)。Y.Gao等(1996年)报道,青岛东海沿岸地区气溶胶中的MSA浓度为0.066μg·m-3,厦门南海沿岸地区气溶胶中的MSA浓度为0.036μg·m-3。很明显,MSA的浓度,在东海地区要高于南海地区。而在南海地区,1月份的MSA值略大于4月份。表6-6列举了世界各地海洋性气溶胶中的MSA值。我们调查研究所得到的值,跟其他研究者得到的,大都在同一个数量级范围。影响DMS转化成MSA的因素是多方面的,其中至少有3个方面是影响南海地区MSA浓度的显著因素。首先,哪个地区有比较高的初级生产力,哪儿就有比较多的营养输入。最近对不同海区的生态调查表明,中国东海的渤海[5]地区的初级生产力为112 g C m-2·yr-1(克碳每平方米每年)[59],这要比南海地区的(39 g C m-2·yr-1)[60]来得高。由于黄海和鸭绿江会输入营养成分到渤海地区,因此渤海的营养输入要高于南海。其次,能影响MSA浓度的因素是NO 3自由基的浓度,因为它是DMS的主要氧化剂之一,故污染气团中携带更多的NO 3自由基,也就能产生更多的MSA[57]。图6-7给出了MSA和NO3-浓度变化,两者呈现显著的正相关。从图中可以看出,在受污染严重的邻近码头的地区,MSA的浓度要显著高于远洋海域,那也是由于受内陆污染气团携带有更大量的NO3自由基的影响。其三,DMS的氧化过程也包括和氢氧自由基的反应,该反应与温度密切相关。有研究表明,低温有利于DMS的这种氧化[61-63],而南海的1月份气温要低于4月份,因此在1月份气溶胶中的MSA值,要略大于4月份。(https://www.xing528.com)
表6-6 世界各地区沿岸大气中MSA的浓度

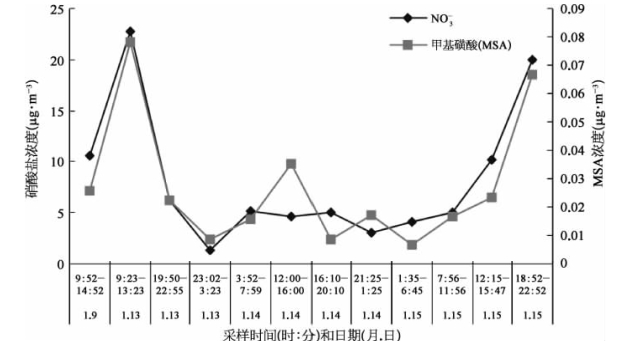
图6-7 南海北部MSA和NO3-的浓度变化(彩图见下载文件包,网址见14页脚注)
3.海洋气溶胶中的可溶性Fe(Ⅱ)
P和N等是海洋初级生产力的主要营养物质。J.H.Martin[13]根据对东北太平洋中Fe的分布以及Fe和其他营养元素如N、P在海水中的含量跟海水中浮游生物生产力之关系研究,提出Fe是这一海区海洋生产力之限制因素的假设,亦即铁限制假设。这一假设的提出,引起了全球科技同行的普遍重视。一般认为,只有可溶于水的Fe才能为浮游生物所吸收。某些海区海水中的Fe,可能99%以上来自大气气溶胶在海洋中的沉降[22]。许多大洋海区的人工加铁实验,证实了大气中的Fe对海洋初级生产力的限制和决定性作用[70]。庄国顺等人[27]于1992年在Nature上首次报道了远太平洋和大西洋地区海洋气溶胶中存在的Fe(Ⅱ),并提出Fe-S氧化还原耦合的全球循环模式,揭示了S和Fe的生物地球化学循环,及其可能的连锁循环反馈模式。我们利用新发展的高效液相色谱法[34],首次检测了中国气溶胶、雨水和雪中的Fe(Ⅱ)[71]。研究表明,海洋生物可利用的Fe,跟海洋吸收CO 2的能力进而跟全球温室效应直接有关[72-77]。Faust和Hoigne[78]认为,Fe(Ⅲ)的光还原反应是云层、雾水和雨水中OH·自由基的主要来源(见55页)。他们测定了此光解反应在波长为313 nm时的量子效率为0.14±0.04。此值是早先较为保守的估计值0.02的7倍。此光解反应可能就是远洋气溶胶中产生Fe(Ⅱ)的关键反应。
表6-7展示了不同地区和不同时期采集的气溶胶中Fe(Ⅱ)的浓度。可以看出,尽管在海洋地区气溶胶中Fe(Ⅱ)的绝对平均浓度,比陆地的沙尘及非沙尘时期都低,但是海洋气溶胶中Fe(Ⅱ)占总Fe的比例为22.6%±19.0%,这要比陆地气溶胶中的值大。可见,海洋气溶胶更有利于Fe(Ⅱ)的生成,因此在沙尘入侵期间,海洋气溶胶中Fe(Ⅱ)的绝对浓度要大大高于其他时期。因此,每年的沙尘暴时间虽短,但其输送至遥远地区的气溶胶量,可以占据全年输送量的绝大部分。G.Zhuang等[79]的研究表明,太平洋上空气溶胶的浓度及雨量时间分布,均具有极大的事件脉冲特性,气溶胶年沉降量的很大部分常常是在很短时间内由几个重大的沙尘事件所完成。这一结果表明,中国的沙尘暴虽然每年只是短短的几次或几天,但对海洋地区的沙尘沉降总量,以至对全球的生态变化,有着至关重要的影响。
表6-7 气溶胶中Fe(Ⅱ)的浓度(μg·m-3)
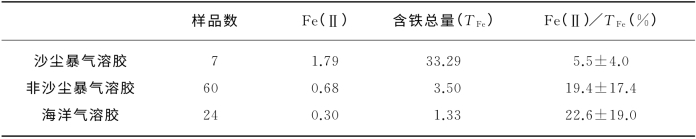
表6-8列出了2个航次中PM 10和PM 2.5样品中Fe(Ⅱ)浓度。可以看到,4月份Fe(Ⅱ)的平均浓度(0.205μg·m-3)要比1月份(0.387μg·m-3)来得小。但是,4月份样品中Fe(Ⅱ)占总Fe的比值(64%±18%),比1月份(36%±20%)要高。这一结果表明,在南海春季的气溶胶中比较容易产生Fe(Ⅱ)。图6-8展示了珠江口海域春季和冬季PM 10和PM 2.5中Fe(Ⅱ)的浓度。春季PM 10气溶胶中Fe(Ⅱ)的浓度为0.1~0.4μg·m-3,PM 2.5中Fe(Ⅱ)的浓度为0.12~0.37μg·m-3;冬季PM 10气溶胶中Fe(Ⅱ)的浓度为0.15~0.53μg·m-3,PM 2.5中Fe(Ⅱ)的浓度为0.12~0.92μg·m-3。Fe(Ⅱ)占总Fe的9%~63%。每年有大约8.50×102~5.95×103 t(吨)的可溶性Fe(Ⅱ)沉降在珠江口海区,为该海区浮游植物的生长提供微量营养元素。从图中可以看出,PM 2.5中Fe(Ⅱ)的检出率明显高于PM 10。这进一步证明了Fe(Ⅱ)在气溶胶中的产生机理,即是由于细颗粒物表面的复相化学变化的产物,因此在细颗粒物中Fe(Ⅱ)要多一些。同时,我们利用XPS对珠江口气溶胶颗粒物进行表面结果分析发现,这些颗粒物表面存在Fe3 O4、α-FeOOH、NaFeO2,同时也存在FeO,FeO占总Fe的比例为43.13%。这一发现从微观上进一步证实了在气溶胶中存在Fe(Ⅱ),其在海洋表层水中的沉降可为生物所吸收利用,这是影响全球生物地球化学循环的重要机制之一。
表6-8 2个航次中海洋气溶胶中的Fe(Ⅱ)浓度(μg·m-3)
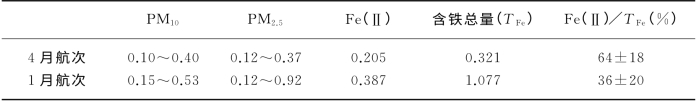
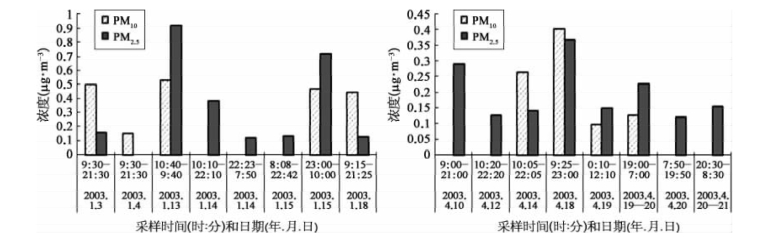
图6-8 春季和冬季PM10和PM2.5中的Fe(Ⅱ)浓度(彩图见下载文件包,网址见14页脚注)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




