煤层中煤层气的含量远远超过其自身孔隙的容积,是因为存在大量以吸附状态赋存的煤层气。煤层气吸附量与煤的比表面积、温度和压力有关。
通常固体的比表面积用单位体积内的总面积或单位重量总面积来表示。煤的比表面积相当大,采用CO2作介质测得煤的比表面积为50~200cm2/g,对气体有着强烈的吸附性。
(1)吸附理论
所谓吸附,就是物质在相界面上的过剩现象,是气体或液体分子在物质表面上的积聚,这是因为物质内部分子和周围分子之间有相互吸引作用,尤其是表面积很大的物质。吸附过程分为物理吸附和化学吸附两类。
物理吸附的作用力是分子间作用力,吸附的过程中物质不改变原来的性质,因此,吸附能很小,吸附热一般只有2.09~20.92J/mol,被吸附的物质容易解吸;化学吸附的过程中发生化学反应,作用力不仅有静电引力,还有化学键力,因此,吸附能较大,吸附热可达20.92~41.84J/mol,吸附过程一旦发生,则较难解吸。
多数研究者认为,煤层气是以物理吸附的方式赋存于煤储层之中,煤对煤层气的吸附是可逆的。甲烷与煤孔隙表面的相互作用具有各向异性特征,在-100~30℃范围内未发现化学吸附现象(陈昌国等,1995)。煤层气在煤的孔隙表面形成了吸附层,而且在范德华力的作用下,临界温度以下的所有气体都有吸附势,并会形成多层吸附。基于范德华力的物理吸附释放的热量与气体凝聚成液态释放的热量接近,所以,从本质上讲,物理吸附和凝聚作用相似,因此,吸附态甲烷与液态甲烷具有相似的物理性质和相近的密度。
煤对煤层气的吸附可用不同的吸附状态方程(吸附曲线)来表达:恒温条件下,测定不同压力时的吸附量,即吸附等温线;恒压条件下,测定不同温度时的吸附量,即吸附等压线;吸附物质的量(体积)一定的条件下,测定不同温度下的压力变化,即吸附等容线。
最直观的是吸附等温线,它反映了等温条件下吸附量与压力的关系。目前识别出的各种物质的吸附等温线大体归为5类。这种分类称吸附等温线的BET分类,气体在固体表面上吸附等温线的5种类型见图1-2。
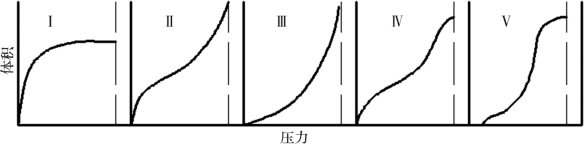
图1-2 气体在固体表面上吸附等温线的5种类型
煤对甲烷的吸附属于第Ⅰ类吸附等温线(Langmuir等温线),是单层可逆的窄孔吸附过程,煤样的外表面积比孔内表面积小很多,吸附容量受孔体积控制。
基于吸附相和游离相间的两相平衡,煤层气吸附行为常用Langmuir单分子层吸附模型和BET多分子层吸附模型来进行描述,此外还有基于统计势动力学理论的多相气体吸附模型以及吸附势理论模型。
①Langmuir单分子层吸附模型。Langmuir模型(I.Langmuir,1916)是根据汽化和凝聚动力学平衡原理建立的,广泛应用于煤和其他吸附剂对气体的吸附。Lang⁃muir模型的基本假设如下:
ⓐ固体表面之所以具有吸附能力,是由于其表面的原子力场没有饱和,有剩余力存在,当气体分子碰撞到未被吸附质覆盖的空白固体表面上时就可能被吸附并释放出热量,当固体表面布满气体分子后,这种力场达到饱和,因此,吸附是单分子层的;
ⓑ固体表面是均匀的,各处的吸附能力也是均匀的,吸附热不随覆盖度变化,是一个常数;
ⓒ吸附可逆,被吸附的气体分子热运动的动能足以克服吸附剂的引力场时,会重新回到气相,回到气相的可能性不受邻近其他被吸附气体分子的影响,即被吸附气体分子之间无作用力;
ⓓ吸附达到平衡时,吸附和解吸过程仍在进行,吸附平衡状态是吸附速度和解吸速度相等的动态平衡。
Langmuir吸附等温方程式:

式中:V——气体压力为p时的吸附量;
Vm——吸附剂表面覆盖满单分子层气体(覆盖度100%)的吸附量;
b——吸附作用平衡常数,也叫吸附常数,是温度和吸附热的函数。
吸附剂表面被气体分子覆盖的百分数为覆盖度:

Langmuir模型基于单分子层吸附理论,该理论认为被吸附气体和吸附剂之间的平衡是动态的,即分子在吸附剂表面空白区凝结的速率等于分子从已占领区域重新蒸发的速率。
②BET多分子层吸附模型。多分子层吸附理论是S.Brunauer、P.H.Emmet和E.Teller3人于1938年在单分子层吸附理论基础上提出的,该理论将Langmuir对单分子层假定的动态平衡状态用于各不连续的分子层,是单分子层吸附理论的扩展。BET多分子吸附模型在Langmuir单分子层吸附是动态平衡、固体表面各处吸附能力是均匀的、被吸附的气体分子间无相互作用3项假设的基础上,又假设第一层的吸附力是固体分子与气体分子间的范德华力,而第二层以上的吸附力是气体分子间的范德华力,第一吸附层的吸附热和其他各层不同,但第二层以上各层的吸附热相同。吸附是多分子层的,但不是第一层吸附满时再进行第二层吸附,而是每一层都可能有空吸附位,吸附层是不连续的,但只有直接暴露于气相的表面的分子发生解吸。这种吸附称为BET吸附,用BET方程进行描述。BET方程的二常数表达式为:
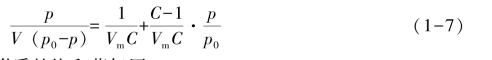
式中:p0——实验温度下吸附质的饱和蒸气压;
V——气体压力为p时的吸附量;
Vm——单分子层气体达到饱和时的吸附量;
C——与吸附热和吸附质液化热有关的系数。
BET方程可以描述所有类型的吸附等温线,它的一个重要用途就是测定固体比表面积。在较高的压力下,多分子层吸附存在的可能性更大。
③多相气体吸附模型。Langmuir模型和BET模型的建立,均是基于吸附相与游离相之间的两相平衡。J.J.Collins(1967)认为,煤孔隙中气体分析不是游离态,而是处于煤分子电磁场中,这种分子力改变了微孔中流体的性质。由此,Collins提出了煤层气分子的游离气相、单分子层吸附相、孔隙气相和类液相的四相平衡吸附理论,即统计势动力学理论,该理论认为,气体分子与固体分子间的作用力为伦敦分散力,气体分子间的作用力为范德华力,假设多孔介质为具有一定孔隙体积的固体,孔隙体积由所有具有同样半径的圆柱形孔隙的集合体组成,较高压力下的气体吸附等温线方程为:
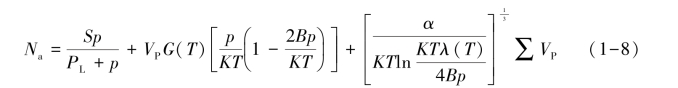
式中:Na——吸附剂中的气体分子数;
S——总吸附位数量;
PL——压力常数,在此压力下吸附量达最大吸附能力的50%;
VP——吸附剂孔隙体积;
G(T)——孔隙相气体密度温度校正因子;
K——玻尔兹曼常数;
T——绝对温度;
B——范德华因子;
α——常数;
∑——吸附剂比表面积。

式中:h——普朗克常数;
m——气体分子量。
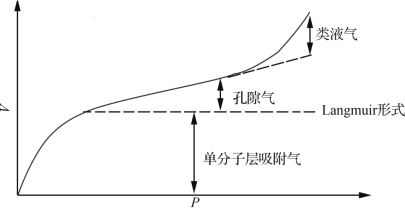
该吸附等温线方程中第一项为Langmuir等温吸附量,即单分子层吸附中的气体分子数;第二项为以孔隙气形式存在于孔隙体积中的气体分子数量;第三项为以压缩或类液层形式存在的分子数量,压力较低时为零。Collie认为吸附态的气体由以上3部分组成,游离态不属此范畴。等温吸附条件下多孔固体中的吸附态气体的3种相态见图1-3。
 (https://www.xing528.com)
(https://www.xing528.com)
图1-3 等温吸附条件下多孔固体中的3种相态
统计势动力学理论是动力学、热力学和位能理论的综合,其吸附等温线归为Ⅱ型吸附等温线。就目前获得的大量煤的吸附等温线来看,大多数属Ⅰ型,即可用Langmuir方程描述,但确有一些属Ⅱ型,见图1-4,在经除去游离态气体校正后,属Ⅱ型吸附等温线。
④吸附势理论。DeSaussure(1814)提出吸附剂对吸附质有吸引力,距离吸附剂表面越近,吸附引力越大,吸附质的密度也越高。Euken(1914)将这种引力引申为吸附势。吸附势理论认为,固体表面附近存在一个势能场,吸附是由势能引起的。就如同地球表面存在的引力场,距离固体表面越近,吸附势能越高,吸附质浓度越高。
M.Z.Polanyi对吸附势进行了定量描述,采用Dubinin⁃Radushkevich(R-D)方程来描述微孔吸附剂的等温吸附行为:
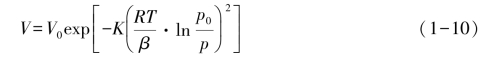
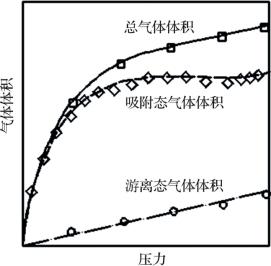
图1-4 黑勇士盆地煤的吸附等温线
式中:V——气体压力为p时的吸附量;
V0——极限吸附量,即微孔体积;
β——吸附质的亲和系数;
K——与孔结构有关的常数,微孔条件下,K=2;
p0——实验温度下吸附气体的饱和蒸气压。
吸附势理论不涉及固体表面的均匀性,认为吸附空间内各处都存在吸附势,距离固体表面越近,吸附势越大,吸附势相等的点构成吸附面,在任何温度下,吸附势和吸附量的关系都是相同的,即ε=f(Z),见图1-5。

图1-5 Polanyi吸附势理论
Polanyi吸附势理论认为,吸附温度T远低于吸附气体的临界温度Tc时,吸附膜是液态的;吸附温度T略低于吸附气体的临界温度Tc时,吸附膜是液态与压缩气体的混合体;吸附温度T高于吸附气体的临界温度Tc时,吸附膜为压缩气态。吸附势模型可描述Ⅰ、Ⅱ类吸附等温线,适合于孔径较小(一般孔径为0.6~0.7nm),并不易发生多层吸附或毛细凝结现象的物质,在对煤/单组分气体等温吸附模拟时较准确。
(2)煤对气体的吸附特性
煤层气是一种多组分混合气体,煤对多组分气体的吸附特性是煤层气赋存和开采的重要研究内容。二元气体的吸附等温线总是介于强吸附气体与弱吸附气体的吸附等温线之间。CH4+N2二元混合气体的吸附量总是小于纯CH4的吸附量,CH4+CO2二元混合气体的吸附量总是大于纯CH4的吸附量。CH4+CO2+N2三元气体的吸附等温线在较低压力下与混合气体中强吸附性双组分(CH4+CO2)等温吸附曲线接近;压力升高,其吸附性介于强吸附性双组分(CH4+CO2)与纯CH4之间,见图1-6。多元气体中各组分的比例或分压不同,吸附等温线也有差异。
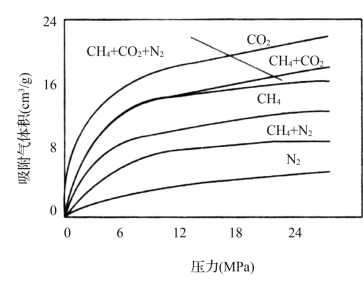
图1-6 不同气体的吸附特性(据何学秋,1995)
根据式(1-5),对于多组分气体,某组分i的吸附特征可用扩展的Langmuir方程描述:
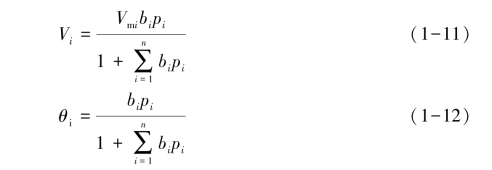
式中:Vi——气体组分i在压力为pi时的吸附量;
Vmi——气体组分i在压力为pi时的单分子层吸附量;
bi——吸附作用平衡常数,是温度和吸附热的函数;
θi——气体组分i的分子覆盖度。
解吸过程中,CH4的浓度随压力下降而下降,CO2在同一区间内的浓度则上升,见图1-7。
煤对不同纯气体组分的吸附能力取决于气体分子和煤分子之间的作用力,这种作用力与吸附质的沸点有关,沸点越高,吸附力越强,所以,间接与分子极性、分子量有关,相同条件下,煤对于煤层气中常见组分的吸附能力:
![]()
可见,煤层气中其他组分的存在对甲烷气体的吸附和解吸特性有一定影响。
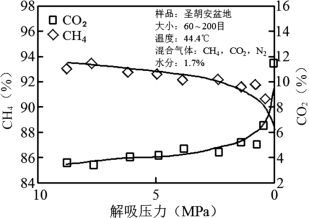
图1-7 CO2和CH4的解吸特性
向煤储层注入驱替气体A,则甲烷解吸动力学方程:
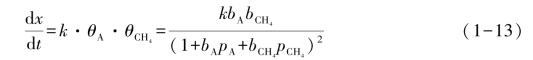
式中:A——注入的气体;
k——解吸速率常数;
θ——气体组分的分子覆盖度;
b——吸附作用平衡常数;
p——气体组分的压力。
(3)煤的等温吸附特性的测试
煤的吸附特性的测试有体积法、重量法和色谱法3种方法。
①体积法。以Boyle定律为依据,即测量同一温度不同压力下煤样的吸附、解吸气体体积,然后换算为标准状态下、单位重量无水无灰基煤样的吸附、解吸量,按前述的方法求取兰氏常数,得到吸附方程,绘制吸附等温线。
②重量法。通过测量吸附、解吸气体的重量随压力的变化而实现。目前常用的是灵敏恒定载荷天平和高压微量天平。后者的测试结果要进行浮力校正,即实测重量排除浮力影响后就是吸附、解吸气体重量。这种方法适合研究微量样品,如显微组分的吸附能力。
③色谱法。根据不同气体在吸附剂中流动速率不同来测试。对纯气体而言,简单的物质平衡就可计算吸附量;对混合气体而言,必须测定各种气体的成分和吸附量。
我国目前采用的是《煤的高压等温吸附试验方法》(GB/T19560—2008)标准。
(4)影响煤对气体吸附特性的地质因素
①煤储层压力。压力是影响气体吸附特性的重要因素,对于煤层气而言,煤储层压力影响显著。煤储层压力受煤层埋藏深度、构造应力、地下流体状况等因素的影响。煤储层压力增大,煤层气的吸附量随之增大,等温条件下,吸附量与压力的关系可以用Langmuir等温吸附方程式来描述;压力增大到某一极限压力后,吸附达到饱和,吸附量不再随压力的增大而增加。
②煤储层温度。温度提供的能量使吸附气活化,温度升高,会提高气体的活性,使解吸容易发生,同时,最大吸附能力减弱。根据山东煤样实验结果,在30~40℃区间,温度每升高1℃,吸附量减少0.11~0.29cm3/g;在40~50℃区间,温度每升高1℃,吸附量减少0.03~0.15cm3/g。
③煤质煤岩因素。煤的物质组成对煤层气的吸附有显著影响。矿物质对煤层气没有吸附能力,所以煤中矿物质含量越高,对煤层气的吸附能力就越差。如在中煤级煤阶段,惰质组的甲烷吸附能力高于镜质组;在高煤级煤阶段,二者差异不大。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




