循环伏安时,在H2SO4溶液中清洁Ru金属表面上表面氧化物膜形成的最初始阶段的一次或两次阳极和阴极扫描中,电流响应行为类似于Pt上发生的情况,即最初的H吸附和脱附出现在0~0.3 V之间(RHE),并能观察到亚单层OH或O开始沉积;在0.3 V以外,几乎与H氧化过程交叠在一起。这之后便形成宽阔的表面氧化物区域,直到阳极氧气在氧化物膜上析出,并伴随部分Ru的溶解。在约1.4 V处,每个Ru原子上近似沉积一个氧原子,但这可能只是一个重建层,即O/Ru的交换处,在1.4 V处的反向扫描不可逆地导致氧化物膜的还原峰。
与在Pt上的行为不同,由于H区的电荷依赖于扫描速率H沉积和脱附区包含电化学H吸收过程(阴极极化方向)和欠电势沉积(H吸附)。
Ru上存在氧化物膜随持续的循环累积性生长的现象。在0.05~1.40 V循环数百次至上千次,最终逐渐形成微米级厚度的厚膜。20~30次或稍少的循环会失去表征单层氧化物形成和还原的第一周循环伏安曲线的形状,随后产生了几乎矩形的循环伏安曲线,类似于大型电容器的充电和放电。在循环后形成IrO2的Ir上也观察到了类似的行为,但由于0.6 V以下转变成导电性差的氧化物膜(图4−12),所以观察到的可逆氧化和还原电流的电势区间仅为0.6~1.4 V(RHE)。
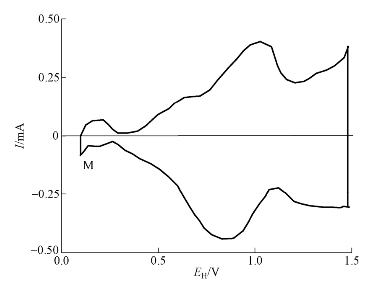
图4−12 Ir基体上几乎可逆生长和还原的IrO2氧化物膜的循环伏安曲线
同样地,在Pt和Rh上也可以形成厚氧化物膜(相当于40层O),相应方法如下:
①在接近0.7 V的受限电势范围内进行电势循环,在该电压范围内氧化物仅有部分还原。
②通过交流调制。(https://www.xing528.com)
③在2.0~2.4 V的高电极电势下恒电势极化。
但是这种膜与RuO2或IrO2循环时不同,未表现出可逆氧化还原行为。在某一负向循环时该厚氧化物膜也能完全还原为Pt金属,同时伴随H的欠电势沉积。
对于RuO2或IrO2而言,关键性的差异是一旦形成厚氧化物膜,在负向循环时从不还原成金属。因此,在降至H+/H2的可逆电势时,较低氧化态的氧化物膜仍能保持在金属表面。电解形成RuO2膜的循环伏安曲线所展示的可逆过程与交叠在一起的氧化还原过程有关,可能涉及Ru的三个或更多的氧化态,但不包括Ru0态。
在阳极极化的作用下,尽管在大部分金属(包括贵金属)上都会形成氧化物膜,但在电势循环下,只有在一定的阳极半循环中产生的氧化物能在接下来的阴极半循环中不完全被还原,或完全不被还原才能生长氧化物膜,因此在连续的循环中氧化物膜的厚度持续增加。当然,对阳极半循环来说需要对最小的正向电势进行限制,在相反的方向,即阴极半循环同样需要某种限制。在适当的阳极电势下,如在Pt上,当大于1.0 V时,对其持续进行直流极化,氧化物膜生长的速率直接取决于薄膜形成所用的极化时间的对数,即直接采用对数规律。
氧化物膜的生长定律与不同的氧化物生长机制和最终膜的不同离子和电子导电性相关。某些最初改造的氧化物膜形成后,生长机制随后会发生变化。例如,对于形式上相应于PtO2的程度,实际上在紧密膜中的状态是两层PtO。该膜之外进一步的生长则是以水合氧化物状态发生的,该水合氧化物可被还原且独立于紧密膜之外。但是,整个膜都没有表现出像RuO2或IrO2那样的可逆还原和再氧化性。循环时RuO2膜的形成还显示出有两个阶段,这种情况可通过两个依赖电势的区域进行辨别,如图4−13所示。
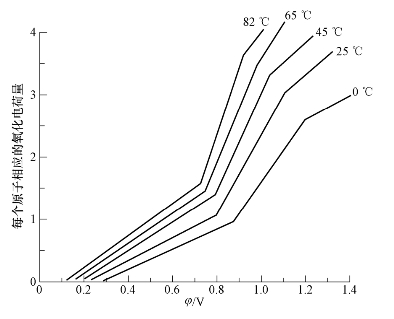
图4−13 H2SO4溶液中Ru的电极电势依赖于氧化电荷的两个区域
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




