燃料电池是燃料电池汽车的核心部件。燃料电池汽车的工作原理如图3-13所示,当汽车起动时,燃料电池中的氢与大气中的氧气发生化学反应,释放电能带动电动机工作,电动机驱动机械传动结构,进而带动汽车的前桥(或后桥)等行走机械结构工作,从而使电动汽车正常行驶。
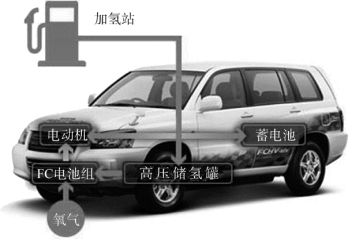
图3-13 燃料电池汽车的工作原理
1.制氢
由于燃料电池是以燃料氢气和氧气通过电化学反应产生电能,因此需要制造原材料氢气。化学反应制氢法包括水蒸气重整制氢、重油不完全氧化制氢、等离子体热裂解制氢、煤气化制氢、甲醇制氢、电解水制氢、热化学循环分解水制氢、光催化分解水制氢、微生物制氢等。我国现主要利用钢铁厂和氯碱化工厂的副产氢制取高纯氢气、利用煤炭生产高纯氢气、通过电解水和光解水制氢。
燃料电池涉及的化学反应的代谢产物是水和少许热量,化学反应过程如下:

输出的能量:ΔG(298K)=-273.2 kJ/mol
输入的能量:ΔH(298K)=-289.84 kJ/mol
输出电压:U=1.229 V
发电时生产的能量:Q=ΔH-ΔG=-16.64 kJ/mol
上式中,负号表示热量传出。燃料电池工作时,燃料供给负极,氧气供给正极。燃料电池内使用的电解质不同,正负极发生的反应也不同。根据化学特性,电解质可分为酸性介质、碱性介质和固体电解质。不同介质中的具体化学反应如下:(https://www.xing528.com)
(1)酸性介质时:负极H2+2OH-→2H2O+2e-
![]()
(2)碱性介质时:负极H2→2H++2e-
![]()
(3)固体电解质:负极H2+O2-→H2O+2e-
![]()
质子交换膜燃料电池的具体工作原理如下:氢气供给燃料电池的阳极板(负极)经过催化剂(铂)的作用,氢原子中的一个电子被分离出来,失去电子的氢离子(质子)穿过质子交换膜,到达燃料电池的阴极板(正极),而电子不能通过质子交换膜,只能经外部电路到达燃料电池阴极板,从而在外电路中产生电流,电子到达阴极后,与氧原子和氢离子重新结合成水。由于供给阴极板的氧可以从空气获得,因此只需给阳极板不间断供应氢,给阴极板供应空气,并及时处理水蒸气,就可以持续获得电能。燃料电池发出的电能经过逆变器、控制器等装置,给电动机供电,再经传动系统、驱动桥等带动车轮转动,就能够使汽车顺利行驶。
2.储氢
储氢法包括特高压气瓶、高压深冷液化氢瓶、可逆金属氢化物、物理吸附法和化合物储氢(纳米硼烷氨络合物)等,具体对比如表3-2所示。
表3-2 储氢方式对比

高压液化储氢消耗能量大且需要贵重隔热材料,推广难度较大,特高压气瓶、复合材料及无机化合物储氢能耗小,但安全技术还有待提高。氢气储存点应远离强氧化剂、高温区、有毒物质和高压电路。氢气密度小,车载储氢系统质量密度应大于5%。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




