由表3.4、表4.14、表4.16、表4.18及表4.19可知,平衡产物中浓度较高的物质为气态KOH 单体及其二聚体K2O2H2和K2(OH) 2、气态K 原子,其次是气态KO 单体,但浓度与气态K 原子相差至少一个数量级,并且灭火有效性排序与平衡产物中气态物质含量的多少相一致,说明钾盐灭火过程中的活性物质为气态KOH等含K化合物。因此,从动力学机理上推断,掺杂K元素的CH4/空气当量比火焰中,灭火活性自由基消除火焰自由基的催化循环反应至少应包含的物质为K、KOH和KO。
在之前的研究中,许多学者提出过碱金属盐抑制火焰的自由基消除反应机理,Jensen和Jones提出的两步反应机理为:

其中,X 代表任意碱金属元素;M 为参与链式反应的第三体。Williams 和Fleming 应用此两步反应机理对含钾和钠的碱金属进行计算,结果表明,大部分计算结果可以较为真实地反映实际的实验现象。
Hynes和Slack的研究成果认为,含碱金属抑制火焰的动力学机理中还应该包含物质XO及XO2,提出了可能的反应路径,并认为反应式(5.10)的重要性等同于反应式(5.9)。
 (https://www.xing528.com)
(https://www.xing528.com)
Williams 和Fleming 综合上述研究人员的成果,提出了含Na 物质抑制火焰的动力学模型为式(5.12)~式(5.14)。

相比于掺杂Na 的火焰化学机理,掺杂K 的火焰燃烧机理更少,目前还没有权威的、可直接使用的机理文件。Slack 参考Hynes 的17 步含Na 火焰动力学机理,将机理中的Na换成K,实验测试了正向和逆向反应速率,得到了被认可度相对较高的含K的燃烧动力学10步机理,见表5.2。
表5.2 含K的燃烧动力学10步机理
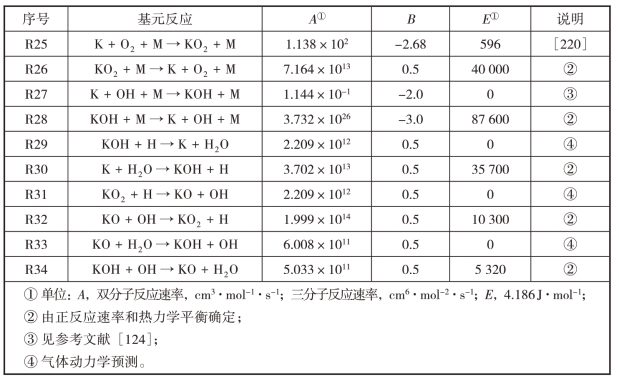
综上所述,含K 的CH4燃烧化学动力学简化机理模型应至少包括KOH、K、KO及反应R1~R34。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




