灭火过程是一个复杂的多元复相体系,通过热力学平衡计算手段可以预测反应结果,明确火焰温度如何影响化学反应的进行程度。
研究化学反应的热力学可行性及反应的平衡情况,首先需要建立反应标准吉布斯自由能变化(ΔGθ)与化学平衡常数(Kp)之间的数学关系,即通过化学反应的等温式(4.12)进行评估:
本章采用吉布斯自由能函数法推导化学反应的热力学参数。吉布斯自由能函数法是当今国际上通用的简化计算方法之一。该方法以经典计算为导出基础,并且未做任何的假设,因此所得结果与经典计算完全一致。
已知
由式(4.12)和式(4.13)得出:
或
对式(4.15)进行恒等变换,得到:
式中,T0为参照温度; 和
和 分别为化学反应在T及T0时刻的标准反应热效应;ΔSθT 为化学反应在温度为T时刻的标准反应熵差。
分别为化学反应在T及T0时刻的标准反应热效应;ΔSθT 为化学反应在温度为T时刻的标准反应熵差。
由基尔霍夫(Kirchhoff)式,得到标准反应热效应Δ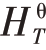 与温度的关系式:
与温度的关系式:
对式(4.17)在参照温度T0与T之间积分:
式中,![]() 是纯物质的标准摩尔相对焓;
是纯物质的标准摩尔相对焓;![]() 为化学反应的相对焓差,表示生成物的相对焓之和减去反应物的相对焓之和。式(4.18)将标准反应热效应之差转换为纯物质的相对焓差。(https://www.xing528.com)
为化学反应的相对焓差,表示生成物的相对焓之和减去反应物的相对焓之和。式(4.18)将标准反应热效应之差转换为纯物质的相对焓差。(https://www.xing528.com)
温度为T条件下的标准反应熵差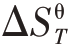 可表示为:
可表示为:
式(4.19)中的 为纯物质i 在温度为T 时刻的标准摩尔熵。由式(4.19)可知,标准反应熵差也可以转换为纯物质的标准摩尔熵差。
为纯物质i 在温度为T 时刻的标准摩尔熵。由式(4.19)可知,标准反应熵差也可以转换为纯物质的标准摩尔熵差。
取式(4.16)右端前两项,结合式(4.18)和式(4.19),得到:
定义 为物质的吉布斯自由能函数ϕT,有:
为物质的吉布斯自由能函数ϕT,有:
对任意化学反应的吉布斯自由能函数变化为:
式(4.22)中,ΔϕT为化学反应的吉布斯自由能函数,由式(4.18)及式(4.19),反应的吉布斯自由能函数Δϕ可由物质的吉布斯能函数ϕT得到:
将式(4.22)代入式(4.16),有:
或
由于大多数的热力学数据都是基于298 K 条件的,因此,参照温度T0取298 K,得出物质吉布斯自由能函数法的表达式为:
生成物和反应物在不同温度条件下的Hθ 和ϕ 值可由热力学数据手册提供,式(4.26)是一种热力学参数的简便计算方法,在保证精确的前提下,可以使化学反应的ΔGθ变得简单准确。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




