燃料电池是通过减少废气排放和能源消耗来改善全球气候环境的具有发展前景的方案。现在已经有很多种类的燃料电池相应问世,伴随着燃料电池系统制造成本、瞬态响应和低温性能等方面的改善,质子交换膜燃料电池(ProtonExchangeMembraneFuelCell,PEMFC)和固体氧化物燃料电池(SolidOxideFuelCell,SOFC)由于应用在混合动力电动汽车上也得到了一定程度的关注。
燃料电池是一种能够持续地将能源的化学能转化为电能的电化学装置,它的工作过程与电化学电池类似,主要区别在于:电化学电池将需要转化的化学能储存在电池内部,因此,一旦化学能被转化为电能,电池必须进行充电,否则就无法使用;而燃料电池所需要转化的化学能来自外部存储设备,因此只要燃料和氧气充足,获取电能的化学反应就能够持续进行。图2-56为德国ProtonMotor生产的燃料电池,图2-57为使用氢燃料电池的丰田第二代Mirai。

图2-56 德国ProtonMotor生产的燃料电池

图2-57 使用氢燃料电池的丰田第二代Mirai
图2-58是质子交换膜燃料电池的基本结构,包括阳极、阴极和电极之间的电解液,给阳极提供氢气,给阴极提供氧气(通常从空气中获取)。阳极位置的催化剂将氢气分解成电子和质子,电子经由外部线路/外负载前往阴极形成电流,而质子通过电解液到达阴极,一旦电子和质子都到达阴极,它们就会结合并与氧气发生反应形成反应产物——水。图2-59是25℃时标准质子交换膜燃料电池电压-电流密度关系曲线。
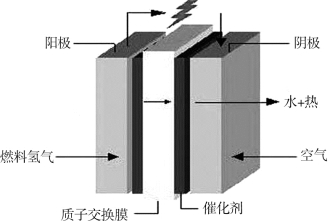
图2-58 质子交换膜燃料电池的基本结构
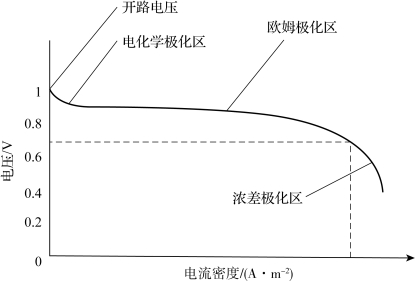
图2-59 25℃时标准质子交换膜燃料电池电压-电流密度关系曲线
此外,对于基于燃料电池的原动机来说,其子系统需要与DC/DC变换器、DC/AC逆变器和电动机进行集成。基于燃料电池的原动机由于包含很多子系统,因此具有复杂且详细的特征。从控制的角度分析,燃料电池系统的工作温度、压力和湿度都是影响其整体性能和效率的最为重要和关键的因素。采用基于燃料电池的原动机最大的优势在于它使所应用的汽车真正实现了零排放。
1.技术原理
燃料电池的电极材料是惰性的,在电池反应过程中不被消耗,但它具有催化特性。
日常生活中常见的电池通常使用金属负极(或阳极),而燃料电池中负极材料或燃料通常是注入负极(或阳极)的气态或液态物质,由于这些“燃料”与普通内燃机使用的燃料基本类同,“燃料电池”的名称因此而流行。
与传统的内燃机相比,燃料电池因为使用氢和碳或化石燃料发电,从而具有更高的效率和较少的污染。燃料电池典型的应用实例是氢-氧燃料电池,并在20世纪已经实际应用于航天领域。但陆地上的应用却进展缓慢,不过最近空气自呼吸式系统技术取得突破,重新为燃料电池赋予了活力。氢-氧燃料电池体系可应用在市政电源、调节电网负载平衡、分散或现场发电以及电动车辆等方面。
燃料电池技术可以分成两类:
1)直接燃料电池,燃料(如氢气、甲醇和水合肼等)直接参与反应;
2)间接燃料电池,首先通过重整将天然气或其他化石燃料转换成富氢的气体,然后提供给燃料电池。
按照燃料、氧化剂、电解质的类型、工作温度和应用等的不同,燃料电池可采取多种构造形式。近年来,燃料电池呈现出用作移动电源的趋势,并且功率水平从低到高不等。
燃料电池是名副其实地把化学能转化为电能的能量转换机器。电池工作时,燃料和氧化剂由外部供给。原则上只要反应物不断输入,反应产物不断排除,燃料电池就能连续地发电。下面以氢-氧燃料电池为例来说明燃料电池的原理。
氢-氧燃料电池反应是电解水的逆过程,其反应原理如图2-60所示。电极反应为
负极:![]()
正极:![]()
电池反应:![]()
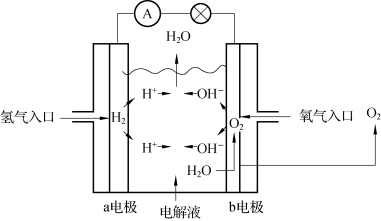
图2-60 氢-氧燃料电池反应原理
另外,只有燃料电池本体不能工作,还必须有一套相应的辅助系统,包括反应剂供给系统、排热系统、排水系统、电性能控制系统及安全装置等。燃料电池及其配套系统如图2-61所示。
燃料电池通常由形成离子导电体的电解质板、两侧配置的燃料极(阳极)和空气极(阴极)、两侧气体流路构成,气体流路的作用是通过燃料气体和空气(氧化剂气体)。
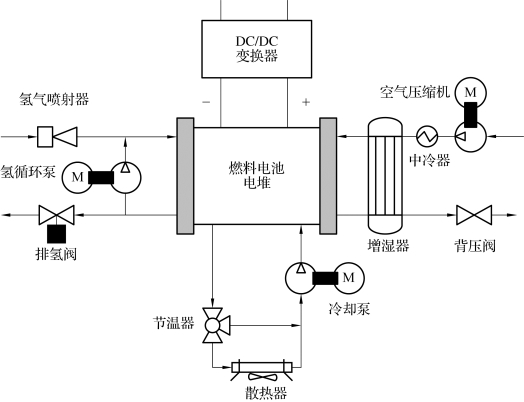
图2-61 燃料电池及其配套系统
在实用的燃料电池中因工作的电解质不同,经过电解质与反应相关的离子种类也不同。磷酸燃料电池(PhosphoricAcidFuelCell,PAFC)PAFC和PEMFC反应中与氢离子(H+)相关,发生的反应为
燃料极:(https://www.xing528.com)
![]()
空气极:
![]()
电池反应:
![]()
在燃料极中,供给的燃料气体中的H2分解成H+和e-,H+移动到电解质中与空气极侧供给的O2发生反应。e-经由外部的负荷回路,再返回到空气极侧,参与空气极侧的反应。一系列的反应促成了e-不间断地经由外部回路,就构成了发电。并且从反应式(3)可以看出,除H2和O2生成的H2O外没有其他的反应,似乎H2所具有的化学能全部转变成了电能。但实际上,由于存在一定的电阻,会引起部分热能产生,由此减少了转换成电能的比例。引起这些反应的一组电池称为组件,产生的电压通常低于1V。因此,为了获得大的输出功率需采用组件多层叠加的办法形成高电压堆。组件间的电气连接以及燃料气体和空气之间的分离,采用了称为隔板的、上下两面中备有气体流路的部件,PAFC和PEMFC的隔板均由碳材料组成。大的输出功率由总的电压和电流的乘积决定,电流与电池中的反应面积成正比。
PAFC的电解质为浓磷酸水溶液,而PEMFC的电解质为质子导电性聚合物系的膜。电极均采用碳的多孔体,为了促进反应,以Pt作为触媒。由于燃料气体中的CO将造成中毒,因此在PAFC和PEMFC应用中必须限制燃料气体中含有的CO量,特别是对于低温工作的PEMFC更应严格地加以限制,这就降低了电池性能。
PAFC的基本组成和反应原理是:燃料气体或城市煤气添加水蒸气后送到改质器,把燃料转化成H2、CO和水蒸气的混合物,CO和水进一步在移位反应器中经催化剂作用转化成H2和CO2。经过处理后的燃料气体进入燃料堆的负极(燃料极),同时将氧输送到燃料堆的正极(空气极)进行化学反应,借助催化剂的作用迅速产生电能和热能。
相对PAFC和PEMFC来说,熔融碳酸盐燃料电池(MoltenCarbonateFuelCell,MCFC)和SOFC则不要催化剂,以CO为主要成分的煤气化气体可以直接作为燃料应用,而且还具有易于利用高质量排气构成联合循环发电等特点。
MCFC主要由电极反应相关的电解质(通常为Li与K混合的碳酸盐)和上下与其相接的2块电极板(燃料极与空气极),以及两电极各自外侧流通燃料气体和氧化剂气体的气室、电极夹等构成,电极为镍系的多孔质体,气室的形成采用抗蚀金属。电解质在600~700℃的工作温度下呈现熔融状态,形成离子导电体。
MCFC的工作原理:空气极的O2(空气)和CO2与电解质接触,生成CO2-3(碳酸根离子),电解质将![]() 移到燃料极侧,与作为燃料供给的H+相结合,放出e-,同时生成H2O和CO2。发生的化学反应为
移到燃料极侧,与作为燃料供给的H+相结合,放出e-,同时生成H2O和CO2。发生的化学反应为
燃料极:
![]()
空气极:
![]()
电池反应:
![]()
与PAFC反应中的情况一样,e-从燃料极被放出,通过外部的回路返回到空气极,由其在外部回路中不间断的流动实现燃料电池发电。另外,MCFC的最大特点是,必须要有有助于反应的CO2-3,因此供给的氧化剂气体中必须含有碳酸气体。并且,在电池内部充填催化剂,将作为天然气主成分的CH4在电池内部改质,从而直接生成H2的方法也开发出来了。而在燃料是液化石油气的情况下,其主成分CO和H2O反应生成H2,因此可以等价地将CO作为燃料来利用。隔板通常采用Ni和不锈钢来制作。
SOFC主要以陶瓷材料构成,电解质通常采用ZrO2(氧化锆),它构成了O2-的导电体Y2O3(氧化钇)作为稳定化的YSZ(稳定化氧化锆)而采用。电极中燃料极采用Ni与YSZ复合多孔体构成金属陶瓷,空气极采用LaMnO3(氧化镧锰),隔板采用LaCrO3(氧化镧铬)。为了避免因电池的形状不同,导致电解质之间存在热膨胀差从而造成裂纹产生等,开发了在较低温度下工作的SOFC。电池形状除了有同其他燃料电池一样的平板型外,还有开发出了为避免应力集中的圆筒型。SOFC中发生的化学反应为
燃料极:![]()
空气极:![]()
电池反应:![]()
燃料极:H2经电解质而移动,与O2-反应生成H2O和e-。空气极:O2和e-生成O2-。电池反应同其他燃料电池一样,由H2和O2生成H2O。在SOFC中,因其属于高温工作型,因此,在无其他催化剂作用的情况下可直接在内部将天然气主成分CH4改质成H2加以利用,并且煤气的主要成分CO可以直接作为燃料利用。
2.组成结构
燃料电池的主要构成组件为:电极、电解质隔膜与集电器等。
(1)电极
燃料电池的电极是燃料发生氧化反应与氧化剂发生还原反应的电化学反应场所,其性能的好坏关键在于催化剂的性能、电极的材料与电极的制程等。
电极主要分为阳极和阴极两部分,厚度一般为200~500mm,其结构与一般电池的平板电极的不同之处在于,燃料电池的电极为多孔结构。燃料电池所使用的燃料及氧化剂大多为气体(如氧气、氢气等),而气体在电解质中的溶解度并不高,为了提高燃料电池的实际工作电流密度和降低极化作用,故发展出多孔结构的电极,以增加参与反应的电极表面积,而这也是燃料电池当初能从理论研究阶段步入实用化阶段的关键原因之一。
目前高温燃料电池的电极主要是以催化剂材料制成,如SOFC中的YSZ和MCFC的氧化镍电极等;而低温燃料电池则主要是由气体扩散层支撑一薄层触媒材料构成,如PAFC和PEMFC的白金电极等。
(2)电解质隔膜
电解质隔膜的主要功能是分隔氧化剂与还原剂,并传导离子,故电解质隔膜越薄越好,但亦需顾及强度,就现阶段的技术而言,其一般厚度约为数十毫米至数百毫米。至于电解质隔膜的材质,目前主要朝两个方向发展,一个方向是先以石棉膜、碳化硅(SiC)膜、铝酸锂(LiAlO3)膜等绝缘材料制成多孔隔膜,再浸入熔融锂-钾碳酸盐、氢氧化钾与磷酸等中,使其附着在隔膜孔内;另一个方向则是采用全氟磺酸树脂(如PEMFC)及YSZ(如SOFC)。
(3)集电器
集电器又称作双极板,具有收集电流、分隔氧化剂与还原剂、疏导反应气体等作用,集电器的性能主要取决于材料特性、流场设计及其加工技术。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




