【高考化学·考试大纲】了解乙醇、乙酸的结构和主要性质及重要应用。
【课程标准·学业要求】(1)能描述乙醇、乙酸的主要化学性质及相应性质实验的现象。(2)能书写相关的反应式,能利用这些物质的主要性质进行鉴别。
1.下列有关氢的活泼性判断正确的是[多选]( )
A.[16 全国Ⅱ,13]分别将少量钠投入到盛有水和乙醇的烧杯中,以比较水和乙醇中氢的活泼性
B.[17 全国Ⅱ,10]乙醇和水都可与金属钠反应产生可燃性气体,说明乙醇分子中的氢与水分子中的氢具有相同的活性
C.[17 全国Ⅱ,10]用乙酸浸泡水壶中的水垢,可将其清除,说明乙酸的酸性小于碳酸的酸性
2.[15 全国Ⅱ,8]某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
A.C14H18O5 B.C14H16O4 C.C16H22O5 D.C16H20O5
3.[18全国I,9]在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
一、烃的衍生物
概念:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物。
二、官能团
1.概念:决定有机化合物化学特性的原子或原子团
2.几种常见官能团的名称及符号。
注意:苯环不属于官能团。
三、乙醇和乙酸
1.分子组成和结构
2.物理性质
3.化学性质
(1)乙醇
①与钠反应:2CH3CH2OH+2Na—→2CH3CH2ONa+H2↑
置换反应,反应较水与钠反应平缓,说明乙醇羟基中的氢不如水分子中的氢原子活泼,常用于处理废钠,乙醇不与氢氧化钠溶液反应。
②在空气中燃烧:氧化反应,常用作燃料。
③催化氧化(Cu或Ag作催化剂):
CH3CHO能发生银镜反应,能被酸性高锰酸钾氧化。④CH3CH2OH![]() 使酸性高锰酸钾溶液褪色:
使酸性高锰酸钾溶液褪色:
乙醇用途:燃料、饮料、化工原料;常用的溶剂;体积分数为75%时可作医用酒精消毒(浓度过大或过小都不能很好的杀菌消毒)。
(2)乙酸
①一元弱酸:CH3COOH CH3COO-+H+
CH3COO-+H+
2CH3COOH+Na2CO3—→2CH3COONa+H2O+CO2↑
酸性强弱:CH3COOH>H2CO3。
②酯化反应:
酯在碱性条件下水解:(https://www.xing528.com)
乙酸用途:化工原料,用于生产醋酸纤维、香料、染料、医药和农药等。
【考型1】乙醇、乙酸的性质
1.[15 山东,9]下列关于分枝酸( )的叙述正确的是( )
)的叙述正确的是( )
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
【考型2】乙醇与乙酸的酯化反应
2.[18 海南,11]实验室常用乙酸与过量乙醇在浓硫酸催化下合成乙酸乙酯,下列说法正确的是( )
A.该反应的类型为加成反应
B.乙酸乙酯的同分异构体共有三种
C.可用饱和碳酸氢钠溶液鉴定体系中是否有未反应的乙酸
D.该反应为可逆反应,加大乙醇的用量可提高乙酸的转化率
【考型3】乙醇、乙酸的活性氢的比较
3.下列有关物质的活性氢判断正确的是( )
A.用Na2CO3溶液不能区分CH3COOH和CH3COOC2H5
B.1mol苹果酸(![]() )与3molNaOH发生中和反应
)与3molNaOH发生中和反应
C.1mol苹果酸(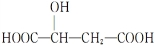 )与足量金属Na反应生成1molH2
)与足量金属Na反应生成1molH2
D.[17.11 浙江,学14]乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
E.[17 江苏测试,14]在苯、乙酸、乙醇中,只有乙酸溶液的pH小于7
一、★乙酸乙酯的制取实验
1.试剂
(1)向试管内加入化学试剂的顺序:先加入乙醇,然后边振荡试管边慢慢加入浓硫酸,最后加入乙酸,注意不能向浓硫酸中加入乙醇或乙酸,防止液体溅出伤人。(2)浓硫酸的作用:催化剂和吸水剂。(3)饱和Na2CO3溶液的作用:①吸收挥发出来的乙醇;②与挥发出来的乙酸反应生成乙酸钠,除去乙酸;③降低乙酸乙酯的溶解度,使溶液分层,便于分离得到酯(注意不能用氢氧化钠)。
2.装置
(1)长导管的作用:导出乙酸乙酯和冷凝回流乙酸和乙醇。(2)碎瓷片的作用:防止暴沸。(3)长导管位置:不能插入溶液中,防止倒吸,若插入液面以下,应使用防倒吸装置,如干燥管等。
3.反应条件
(1)刚开始小火均匀加热,防止乙醇、乙酸过度挥发,并使二者充分反应。(2)反应末大火加热,将生成的乙酸乙酯挥发出来。
4.产物分离
分液法分离,上层油状物为产物乙酸乙酯。
二、乙酸、水、乙醇、碳酸分子中羟基氢的活泼性比较
NaOH与酯能反应。在常温下,Na2CO3不与低级酯反应(例如:用饱和Na2CO3溶液作实验室制取乙酸乙酯的吸收剂),但在加热条件下,Na2CO3与油脂能反应,常用于去油污。(Na2CO3水解生成NaOH,促使油脂发生脂化反应)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




