【高考化学·考试大纲】(1)了解甲烷、乙烯、苯等有机化合物的主要性质及应用。(2)了解氯乙烯、苯的衍生物等在化工生产中的重要作用。(3)掌握常见有机反应类型。
【课程标准·学业要求】(1)能描述甲烷、乙烯、乙炔的分子结构特征,并能搭建甲烷和乙烷的立体模型。能写出丁烷和戊烷的同分异构体。(2)能描述乙烯的主要化学性质及相应性质实验的现象,能书写相关的反应方程式,能利用这些物质的主要性质进行鉴别。
1.下列判断正确的是( )
A.[16 全国Ⅲ,8]乙烷室温下能与浓盐酸发生取代反应
B.[17 全国Ⅲ,8]环己烷与苯可用酸性KMnO4溶液鉴别
C.[17 全国Ⅱ,10]将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明,说明生成的1,2-二溴乙烷无色、可溶于四氯化碳
D.[17 全国Ⅱ,10]甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红,说明生成的氯甲烷具有酸性
E.[18 全国I,10]1.0molCH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA
2.[18 全国Ⅱ,9]实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
●反应类型
3.下列叙述不正确的是( )
A.[16 全国Ⅰ,9]由乙烯生成乙醇属于加成反应
B.[17 全国Ⅲ,8]植物油氢化过程中发生了加成反应
C.[全国高考Ⅰ]香叶醇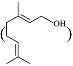 能发生加成反应不能发生取代反应
能发生加成反应不能发生取代反应
4.[16 全国Ⅱ,8]下列各组中的物质均能发生加成反应的是( )
A.乙烯和乙醇 B.苯和氯乙烯
C.乙酸和溴乙烷 D.丙烯和丙烷
一、几种重要的烃
1.甲烷、乙烯、苯的组成结构和物理性质
二、几种烃的化学性质及反应类型
1.甲烷和烷烃
(1)取代反应:![]()
(进一步取代,可生成CH2Cl2、CHCl3和CCl4等一系列混合物)
(2)稳定性:与强酸、强碱和强氧化剂等一般不发生化学反应。
(3)氧化反应:![]()
(在空气中燃烧)
2.乙烯
(1)氧化反应:①在空气中燃烧;
②乙烯能使酸性高锰酸钾溶液褪色:
用于鉴别烯烃和烷烃,但不能于除去烷烃中的乙烯。
(2)与H2、Br2、H2O、HCl等在一定条件下发生加成反应:
乙烯能使溴水或溴的CCl4溶液褪色,用于鉴别烯烃和烷烃,或用于除去烷烃中的烯烃。
(乙烯水化制乙醇)
(3)聚合反应:![]()
(聚乙烯,用作食品袋)
(聚氯乙烯,用作塑料,不能用作食品袋)
3.苯
(1)稳定性:不与酸性KMnO4溶液反应,不与溴水(或溴的四氯化碳溶液)反应。
空气中燃烧:![]()
(火焰明亮,带浓烟)
(2)取代反应:
①卤代反应:苯与液溴反应(需要Fe或FeBr3作催化剂):
②硝化反应(水浴加热):
(3)加成反应:![]()
(4)甲苯在侧链上的反应
①取代反应:
(苯无此反应)
②被酸性高锰酸钾溶液氧化:
6.煤和石油的加工
三、化学反应的基本类型
(1)取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。(https://www.xing528.com)
(2)加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应叫加成反应。
(3)聚合反应:由单体合成高分子化合物的过程。聚合反应分为加聚反应和缩聚反应。
【考型1】有关烃的结构
1.下列判断正确的是( )
A.[15 福建,7]聚氯乙烯分子中含碳碳双键
B.[18.4 浙江,学15]乙烯和苯分子中均含独立的碳碳双键,都能与H2发生加成反应
C.[15 广东,7]对二甲苯属于饱和烃
D.[17.11 浙江,学22]任意条件下,1mol苯中含有C-H键的数目一定为6NA
【考型2】有关烃的性质
2.[17.4 浙江,学15]下列说法不正确的是( )
A.1mol乙烷在光照条件下最多能与3molCl2发生取代反应
B.石油裂解气能使溴的四氯化碳溶液、酸性KMnO4溶液褪色
C.水煤气可用来合成液态烃及甲醇等含氧有机物
D.苯可通过取代反应制得硝基苯、氯苯
【考型3】有机反应的反应类型
3.下列有关反应类型的判断正确的是[多选]( )
A.[15 海南,9]石油裂解制丙烯不属于取代反应
B.[14 山东,7]![]() 与CH2==CH2+HCl—→CH3CH2Cl,均为取代反应
与CH2==CH2+HCl—→CH3CH2Cl,均为取代反应
C.[18 浙江,学15]光照下,1molCH4最多能与4molCl2发生取代反应,产物中物质的量最多的是CCl4
D.[17 浙江,学14]乙烯和苯都能与H2发生加成反应,说明二者的分子中均含有碳碳双键
【考型4】有机分子的空间构型
4.下列有关分析构型的判断中,正确的是( )
A.[16 江苏,11]如下左图分子中两个苯环一定处于同一平面
B.[16 浙江,10]CH3CH==CHCH3分子中的四个碳原子在同一直线上
C.[15 安徽,26]TPE(如下右图)中所有原子可能在同一平面上
一、几种烃的典型性质
1.甲烷与氯气的取代反应
(1)试剂与反应条件:甲烷与氯气混合,光照下。
(2)实验装置
(3)实验现象与解释:①气体的颜色逐渐变浅,证明氯
气参与了反应;②试管内壁有油状液滴出现,证明生成的氯代烃中有油状液体;③试管中有少量白雾,证明有氯化氢生成;④试管内液面上升,证明气体体积减小;⑤水槽中有固体析 出,原因为HCl溶于水,降低了NaCl的溶解度,从而析出。
(4)结论:①反应生成了多种卤代烃(CH3Cl+CH2Cl2+CHCl3+CCl4)和HCl的混合物。因此,制备卤代烃一般不采用取代反应。
②定量关系:![]() molCl2取代1molH原子,生成1molHCl。Cl2中有一半Cl进入有机物中,一半生成了HCl,产物最多的是HCl。
molCl2取代1molH原子,生成1molHCl。Cl2中有一半Cl进入有机物中,一半生成了HCl,产物最多的是HCl。
2.甲烷、乙烯、苯典型化学性质的比较
(1)烷烃最典型的性质是发生卤代反应;卤代反应会生成一系列多卤代物,因此,常不能得到纯净的产物;在卤代反应中,卤原子只有一半形成有机物,另一半生成HCl。
(2)烯烃最典型的性质是发生加成反应。
(3)苯环含有一种介于双键和单键之间的特殊的化学键(或大π键)。注意对苯环的认识,有三不能:①不能认为含有碳碳双键或单键;②不能认为六元环都是苯环;③不能认为C6H6就一定是苯。
(4)芳香族、芳香烃和苯是三个不同的概念,苯或苯的同系物<芳香烃(可能含有多个苯环)<芳香族(可能有O、N等元素),其包含关系如右图。
二、有机反应类型的判断方法
1.取代反应
取代反应的特点是“有上有下”,反应中一般有副产物生成;卤代、水解、硝化、酯化均属于取代反应。一般说来,有机物均能发生取代反应。
2.加成反应
加成反应的特点是“只上不下,变双为单”,反应物中一般含碳碳双键、碳碳三键、苯环等。加成反应包括加H2(只能发生加成)、X2(卤素)、HX、HCN、H2O等小分子加成,以及信息题中的双烯加成。
3.聚合反应(加聚反应)
反应中的三个概念
加聚反应的单体必须是含有双键、三键等不饱和键结构的化合物。
4.氧化反应
主要包括有机物的燃烧、碳碳不饱和键被酸性KMnO4溶液氧化、葡萄糖(含醛基)与新制Cu(OH)2悬浊液、银氨溶液的反应、醇的催化氧化等。
一般有机物都能发生氧化反应和取代反应。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




