【高考化学·考试大纲】理解质量守恒定律。
【课程标准·学业要求】(1)运用物质的量、摩尔质量、气体摩尔体积、物质的量浓度之间的相互关系进行简单计算。(2)了解定量研究方法是化学发展为一门科学的重要标志。
1.[15 全国Ⅰ,9]乌洛托品的结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比应为( )
A.1∶1 B.2∶3 C.3∶2 D.2∶1
2.[15 全国Ⅱ,8]某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
A.C14H18O5 B.C14H16O4 C.C16H22O5 D.C16H20O5
3.[16 全国Ⅰ,36]将K2MnO4转化为KMnO4的生产有两种工艺。
CO2歧化法:3K2MnO4+4CO2+2H2O==2KMnO4+MnO2+KHCO3
电解法:2K2MnO4+2H2O![]() 2KMnO4+2H2↑+2KOH
2KMnO4+2H2↑+2KOH
在“电解法”和“CO2歧化法”中,K2MnO4的理论利用率之比为。
4.[14 全国Ⅰ,36]下图为目前国际上磷矿石利用的大致情况:
(1)世界上磷矿石最主要的用途是生产含磷肥,由图可知约占磷矿石使用量的________%。
(2)现有1t折合含有P2O5约30%的磷灰石,最多可制得85%的商品磷酸________t。
在化学反应中,守恒包括原子守恒、电荷守恒、得失电子守恒等。任何化学反应在反应前后都遵守此规律。
1.原子守恒(或称质量守恒)
即化学反应前后各元素原子个数相等,是配平化学反应方程式的基础。
2.电荷守恒
即反应前后阴阳离子所带电荷总数必须相等,是配平离子反应的基础,另一种情况是指电中性原则,即在任何电解质溶液中,阳离子所带的正电荷总数和阴离子所带的负电荷总数相等。
3.得失电子守恒
在氧化还原反应中,失电子总数一定等于得电子总数,是配平氧化还原反应的基础。即得失电子数目相等。
【考型1】得失电子守恒法
1.[16 全国Ⅰ,28]“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为_______。(计算结果保留两位小数)
【考型2】电荷守恒法
2.[天津高考]对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5的酸碱性为_________,试样的pH值=__________。
【考型3】平均值法
3.20g由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2L氢气(标准状况),这种金属混合物的组成可能是( )
A.Mg和Al B.Al和Fe C.Fe和Zn D.Zn和Cu(https://www.xing528.com)
【考型4】极值法
4.[14 全国,13]已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且![]() 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
A.若某温度下,反应后![]() 则溶液中
则溶液中![]()
B.参加反应的氯气的物质的量等于![]()
C.改变温度,反应中转移电子的物质的量ne的范围:![]()
D.改变温度,产物中KClO3的最大理论产量为![]()
一、守恒法
是一种整合的思维方法,运用守恒定律,不纠缠过程细节,只考虑反应体系中研究对象化学量的始态和终态(如反应中的原子守恒、电子守恒、电荷守恒、化合价升降守恒、能量守恒等),或相互间的关系(如化合物中的化合价规则,电解质溶液中的电中性原则等),从而达到速解、巧解化学试题的目的。
1.反应前后的守恒
(1)元素守恒:反应前后各原子的种类和数目保持不变。
(2)得失电子守恒:氧化还原反应中,氧化剂得电子的总数 =还原剂失电子的总数。
(3)化合价升降守恒:氧化还原反应中,元素化合价升高的总价数=元素化合价降低的总价数。
(4)电荷守恒:在离子反应方程式中,反应前后的阴、阳离子所带的电荷总数相等。
注意:不能混淆“守恒法”与“关系式法”,如H2与O2反应生成H2O;由关系式可得:O2~2H2O;以此列比例式:![]() 变形为:n(H2O)=2n(O2);由氧元素守恒也可以直接得出同样关系:n(O)=n(H2O)=2n(O2);但一些同学会把“关系式”与“守恒法”混淆而出现下列的错误等式:n(O2)=2n(H2O)。在解题中要特别注意区分,“关系式法是列比例(用~)求解,守恒法是建立等式(用=)求解”。
变形为:n(H2O)=2n(O2);由氧元素守恒也可以直接得出同样关系:n(O)=n(H2O)=2n(O2);但一些同学会把“关系式”与“守恒法”混淆而出现下列的错误等式:n(O2)=2n(H2O)。在解题中要特别注意区分,“关系式法是列比例(用~)求解,守恒法是建立等式(用=)求解”。
2.体系中的守恒
(1)化合物中的化合价规则:在化合物中,正、负化合价的代数和为0;化合物中微粒之间存在确定的组成比,这个组成比在考试中常由化合价规则确定。
(2)电荷守恒:电解质溶液(或离子化合物)中,阴、阳离子所带的电荷总数相等。
(3)溶液中的物料守恒:溶液中某一组分的原始浓度应该等于它在溶液中各种存在形式的浓度之和。这是元素守恒的一种表示形式。
二、平均值法
平均值法是一种用于确定范围的方法。它所依据的数学原理是:设两个物理量M1和M2(M1>M2)的混合后的平均值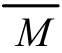 ,则平均值有下列关系:M1>
,则平均值有下列关系:M1>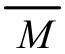 >M2。(如:M1=M2,则
>M2。(如:M1=M2,则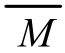 =M1=M2),所以,只要求出平均值
=M1=M2),所以,只要求出平均值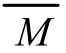 ,就可以判断出M1和M2的取值范围,再结合题给条件即可迅速求出正确答案。
,就可以判断出M1和M2的取值范围,再结合题给条件即可迅速求出正确答案。
常见的平均值有:求平均相对原子质量、平均相对分子质量、平均摩尔电子质量、平均浓度、平均含量、平均组成等。
三、极值法
极值法也是一种用于确定可能范围的思想方法,当两种或多种物质混合无法确定其某种物理量时,可将混合物全部假设为纯物质(极端情况)进行分析,确定最大值、最小值,混合物的这种物理量界于最大值和最小值之间。
常用极值法解决的问题有:(1)把混合物假设成纯净物。(2)把可逆反应假设成向左或向右的完全反应。(3)把平行反应分别假设成单一反应。
极值法与平均值法是分析问题的两个方面:
如:极值法:已知FeCl2和FeCl3混合物,则混合后的平均化学式表示为:FeClx,则2<x<3;
平均值法:已知某混合物的平均化学式为:PbO1.2,其中含有PbO2和另一种PbOx,则x<1.2。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




