一场大飓风释放的能量足够让全世界的人们使用数年,如果能想办法利用和储存这种能量,你就等于找到了一种廉价、可再生、无污染的动力源泉.
知能概述
用元素符号和数字的组合表示物质组成的式子叫化学式.每种纯净物的组成固定不变,所以每种物质的化学式只有一个.混合物没有对应的化学式.
化学式的意义:(1)表示某种物质.(2)表示某种物质的1个分子.(3)表示物质组成元素的种类.(4)表示物质中各元素的原子个数比.
元素之间化合时,其原子个数比都有确定的数值.一种元素一定数目的原子与其他元素一定数目的原子相互化合的性质叫作化合价,化合价有正价与负价.写法:![]() .化合物中元素化合价代数和为零,单质化合价为零.
.化合物中元素化合价代数和为零,单质化合价为零.
问题解决
例1 类推的思维方法在化学学习中应用广泛,例如:水![]() 过氧化氢(H2O2),氧化钠
过氧化氢(H2O2),氧化钠![]() 过氧化钠(Na2O2).由此可推断,过氧化钡的化学式为( ).
过氧化钠(Na2O2).由此可推断,过氧化钡的化学式为( ).
A.Ba2O B.BaO2 C.Ba2O2 D.BaO3
(湖南省竞赛题)
物质由分子构成时,化学式也叫分子式.
(1)(3)为宏观意义,
(2)(4)为微观意义.
注意与离子符号写法比较.
解题思路 从化学式中可以看到氧化物(H2O,Na2O)与过氧化物(H2O2,Na2O2)在粒子构成上的区别,即每一个粒子中过氧化物比氧化物的氧原子个数多1,但这只是表观现象.在过氧化物中,氧元素的化合价为-1价,可由两知识点共同推断.
例2 化肥尿素的化学式为CO(NH2)2,关于尿素的下列说法中错误的是( ).
A.一个尿素分子中含有8个原子
B.尿素由碳、氢、氧、氮四种元素组成
C.尿素中氮元素的质量分数为46.67%
D.尿素中碳、氧、氮、氢原子个数比为1∶1∶1∶2
(重庆市竞赛题)
解题思路 尿素中氮元素的质量分数为:![]() ,计算结果如C选项所示,从尿素的化学式中可以看到有2个NH2(氨基),故尿素中碳、氧、氮、氢原子个数比为1∶1∶2∶4.
,计算结果如C选项所示,从尿素的化学式中可以看到有2个NH2(氨基),故尿素中碳、氧、氮、氢原子个数比为1∶1∶2∶4.
例3 科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如右图,其中每个 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子.下列说法中不正确的是( ).
代表一个氢原子.下列说法中不正确的是( ).
A.该分子的分子式为C5H4
B.该分子中碳元素的质量分数是93.75%
C.该分子中的氢原子与碳原子的个数比是4∶5
D.等质量的该物质与甲烷相比,燃烧时消耗的氧气更多
例3图
(广东省竞赛题)
解题思路 CH4与C5H4完全燃烧均生成CO2与H2O.化合物X(C5H4)的相对分子质量为12×5+1×4=64,甲烷的相对分子质量为16,等质量时C5H4所含分子个数少于CH4,燃烧时消耗氧气的质量取决于物质中所含碳原子个数与氢原子个数的多少.
例4 在元素周期表中,横行叫作“周期”,其周期数与该原子的电子层数相同;纵行叫作“族”,其数值与该原子的最外层电子数相同,且元素的原子序数等于该元素原子的质子数.请将第三周期第二族元素的有关内容填入下表:
(广东省竞赛题)
解题思路 离子所带电荷的多少与得失电子的数目有关,与最外层电子数目有关,化合价与离子所带电荷的数目与“正、负”有关.通常,Mg原子最外层有2个电子,易失去,形成带2个单位正电荷的阳离子Mg2+,Mg元素的化合价为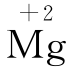 .
.
A.+4 B.+5 C.+6 D.+7
(全国复赛题)
解题思路 根据信息知,化学反应前后电荷守恒.设反应前原子团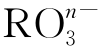 所带电荷数值为x,则有x+(-2)=(-1)+(-2),x=-1,化合价数值与离子所带电荷数值相等,故n=1,在
所带电荷数值为x,则有x+(-2)=(-1)+(-2),x=-1,化合价数值与离子所带电荷数值相等,故n=1,在 中R元素的化合价为+5时,其离子的化合价为-1价.
中R元素的化合价为+5时,其离子的化合价为-1价.
例6 成语是我国的文化瑰宝,请用恰当的化学用语表示下列成语相关内容中带点的字:
(1)如胶似漆:胶中含有碳、氢、钙等元素,写出其中一种非金属的元素符号___________.
(2)争风吃醋:醋溶液中含有氢离子___________.
(3)大浪淘沙:沙的主要成分二氧化硅的化学式:___________.
(4)信口雌黄:雌黄即三硫化二砷,三硫化二砷中砷元素的化合价为+3价___________.
(江西省南昌市中考题)
解题思路 可以根据一定规律、规则,再依照化合价来书写化学式,比如:两种元素所形成的化学物,金属元素写在前,非金属元素写在后,若是氧化物则其他元素写在前,氧元素写在后.另外再根据化合物中元素化合价代数和为零,通常H元素为+1价,O元素为-2价,Cl元素为-1价等规律,依规守律,就可以写出正确的化学式,也可以判断化学式书写的正误.
1.下列化学用语与意义对应不相符的是( ).
A.O2:一个氧分子
B.4Ne:4个氖原子
C.SiO2:二氧化硅
D.2Mg2+:两个镁离子带两个单位的正电荷
(甘肃省兰州市中考题)
离子所带电荷为1时,1可省略不写.
O2既有微观意义,又有宏观意义.
微观:1个氧分子,每个氧分子由两个氧原子构成.
宏观:氧气,氧气由氧元素组成.
2.合成纳米材料氮化镓是我国1998年十大科技成果之一.已知氮的原子结构示意图为![]() ,镓(Ga)的原子结构示意图为
,镓(Ga)的原子结构示意图为 ,则氮化镓的化学式为( ).
,则氮化镓的化学式为( ).
A.GaN B.Ca3N2 C.Ga5N3 D.Ga3N4
(山西省竞赛题)
3.对以下反应归纳正确的是( ).
A.都是分解反应
B.生成物中氧元素的化合价都相同
C.都是实验室制取O2的常用方法
D.①③中的MnO2都是反应的催化剂
(2019年陕西省中考题)
4.已知Na的化合价为+1,则在化合物Na2O2中,O的化合价为( ).
A.-1 B.-2 C.-3 D.0
5.在消毒剂家族中,臭氧和过氧乙酸的贡献并驾齐驱.O3可以看成是一个O2分子携带一个O原子,利用其自身的强氧化性杀灭病菌,反应后放出无污染的O2.下列关于O3的说法中正确的是( ).
A.O3与O2化学性质完全相同
B.等质量的O3与O2所含的原子个数相同
C.使用时浓度大小对人体无害
D.O3遇氟氯代烷不会分解
(甘肃省兰州市竞赛题)
6.元素化合价发生改变的反应都是氧化还原反应.例如![]()
![]() ,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( ).
,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列判断错误的是( ).
A.分解反应都属于氧化还原反应
B.置换反应都属于氧化还原反应
C.复分解反应都不属于氧化还原反应
D.有单质参加的化合反应属于氧化还原反应
(山东省潍坊市中考题)
根据原子结构示意图可判断氮化镓中氮元素呈负价,化合价数值=-(8-5),镓元素化合价为正价,数值等于最外层电子数.
化合物中元素正负化合价总数的代数和为零.
第3题中化学反应对应的文字表达式:
①过氧双氢![]() 水+氧气
水+氧气
②水![]() 氢气+氧气
氢气+氧气
③高锰酸钾![]() 锰酸钾+二氧化锰+氧气
锰酸钾+二氧化锰+氧气
氧元素通常为-2价,但在Na2O2,K2O2,Li2O2,H2O2中为-1价.(https://www.xing528.com)
7.从地沟油中提炼生物柴油是垃圾资源化的方法之一.生物柴油的主要成分是硬脂酸甲酯(C19H38O2),下列有关硬脂酸甲酯的说法正确的是( ).
A.C,H,O三种元素的质量比为19∶38∶2
B.相对分子质量为(12×19+1×38+16×2)
C.C,H,O三种原子的个数比为12∶1∶16
D.氧元素的质量分数为![]()
(2019年广东省广州市中考题)
8.正确理解和使用化学用语是重要的学科素养.下列说法正确的是( ).
A.H2O,H2CO3中均含有氢分子
B.KClO3,KCl中氯元素的化合价不相同
C.Na+,Mg2+,Al3+原子核内质子数均为10
D. 表示的粒子都是阴离子
表示的粒子都是阴离子
(陕西省中考题)
9.如右图所示是某元素的原子结构示意图,该原子在化学反应中容易_________电子(填“得”或“失”),所形成粒子的符号是________,该粒子与镁离子形成化合物的化学式为________.
第9题图
(广东省竞赛题)
10.请按CH4,NH3,H2O,HF,HCl排列顺序,列出五种物质之间存在的规律:____________、_____________.
这五种物质中除_____________(填化学式)外,各分子所含核外电子总数均为_________个.
(全国复赛题)
11.![]() 分别表示氢元素的三种原子,可简写成1H,2H,3H.制造燃料电池常用1H,制造氢弹要用2H,3H.请据图回答:
分别表示氢元素的三种原子,可简写成1H,2H,3H.制造燃料电池常用1H,制造氢弹要用2H,3H.请据图回答:
第11题图
(1)1H,2H,3H三种原子中,_________(填“质子”“中子”或“电子”)数目不等.
(2)2H2与O2反应生成的重水可表示为2H2O,写出3H2在O2中燃烧的化学方程式:____________________________,在图乙的小方框中,把3H2与O2恰好完全反应的反应物微观粒子补画齐全.
(2019年广东省中考题)
注意:重氢与重水的化学式与氢气和水的化学式不同.
重氢:2H2,重水:2H2O.
以此类推:3H2,3H2O.
解题技巧:
1.将物质的微观示意图改写为对应的化学式.
2.对比反应前后微观示意图,去除未反应分子的微观示意图,从而确定参加反应的两种物质分子个数比.
12.近日央视报道:科学家成功研制出一种合成甲醇的新工艺,其反应过程的微观示意图如下.
第12题图
(1)有关说法正确的是( ).
A.反应前后共有四种分子
B.反应前后氧元素化合价发生了改变
C.反应前后原子、分子数目不变
(2)参加反应的两种物质分子个数比为_________.
(2019年江西省中考题)
13.现有X,Y,Z三种元素,其中X原子核内只有一个质子;Y原子L层电子数是K层电子数的2倍;X与Z形成的化合物的分子式为ZX3,每个分子内有10个电子.请回答下列问题:
(1)写出Z元素的原子结构示意图_________________;X分别与Y,Z形成的化合物中,具有5个原子核的微粒的化学式为_______________.
(2)某些常见物质可用来合成新材料,如利用高温高压法使石墨转变为人造金刚石.科学家认为Y,Z元素可形成一种比金刚石更硬的化合物,后来人们在实验室成功合成了含有这些元素的化合物(制作晶体薄膜材料),这种化合物的化学式是_________________;试推测合成这种化合物所需的条件是_______________.
(全国复赛题)
14.龙海实验学校初三兴趣小组利用如下装置(部分固定装置略)制备氮化钙,并探究其化学式(实验式).
第14题图
(1)按图连接好实验装置.检查装置的气密性,方法是________________.
(2)反应过程中末端导管必须插入试管A的水中,目的是____________.
(3)制备氮化钙的操作步骤是:①打开活塞k并通入N2;②点燃酒精灯,进行反应;③反应结束后,______________________________;④拆除装置,取出产物.
(4)数据记录如下:
①计算得到化学式(实验式)CaxN2,其中x=_________.
②若通入的N2中混有少量O2,如上计算x_________3(选填“>”“=”或“<”),并给出判断依据:________________________________.
(全国复赛题)
15.据济南市疾病预防控制中心2007年5月11日发布的消息,目前济南市除商河、济阳两县外,其他八个县(市、区)均为缺碘地区.专家提醒,成人每天吃6g加碘盐就可满足人的生理需要.生产加碘盐通常是在食盐中加入碘酸钾(KIO3).试回答下列问题:
(1)碘酸钾由_________种元素组成.
(2)在KIO3中碘元素的化合价是________价.
(3)为检验某食用盐试样中是否含有碘元素,某同学确定采用以下反应进行实验:
![]() 要达到实验目的,除了KI、稀硫酸外,他还应选用的一种试剂是下列中的_________(填序号).
要达到实验目的,除了KI、稀硫酸外,他还应选用的一种试剂是下列中的_________(填序号).
①淀粉溶液 ②NaCl溶液 ③K2SO4溶液 ④NaOH溶液
(山东省竞赛题)
16.为确定氨的组成,在一定温度、压强下进行如下实验.取20mL氨,设法使它完全分解为N2和H2,体积为40mL.加入20mLO2,当H2和O2完全化合成水,剩余气体体积为15mL(已知一定温度、压强下一定体积各种气体中的分子数相同).请根据以上数据确定氨的化学式.
(全国复赛题)
17.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律.下表列出的是1-18号元素的部分最高正化合价和最低负化合价.请阅读并回答下列问题:
(1)11号元素属于________元素(填“金属”或“非金属”),它在化学反应中形成的离子与_________(写元素符号)原子具有相同的核外电子排布.
(2)16号元素的原子核外电子数为________,推测该元素最低负化合价为________,最高正化合价的氧化物的化学式为________.
(3)从化合价角度分析,我们可以发现一些规律.请写出其中的一个:________________________________________________________________.
(全国复赛题)
碘(I2)遇淀粉变为蓝色.
例1 B 例2 D 例3 D 例4 12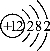 Mg2+ +2 MgO 例5 B
Mg2+ +2 MgO 例5 B
例6 (1)C (2)H+ (3)SiO2 (4)![]()
1.D 2.A 3.A 4.A 5.B 6.A 7.B 8.B
9.得 Cl- MgCl2
10.相对分子质量依次增大 除氢以外元素的质子数依次增大 HCl 10
11.(1)中子 (2)![]()
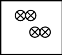
12.(1)B (2)1∶2(或2∶1)
13.(1)![]() CH4(或
CH4(或 ) (2)C3N4 高温高压
) (2)C3N4 高温高压
14.(1)关闭活塞k,将末端导管插入试管A的水中,用酒精灯微热硬玻璃管,若导管末端有气泡冒出,撤去酒精灯冷却后,在导管内形成一段水柱,则证明装置的气密性良好 (2)防止空气中的氧气通过末端导管进入实验装置,生成氧化钙,引入杂质 (3)将末端导管从试管A中撤出水面,再熄灭酒精灯,然后停止通入氮气 (4)①3 ②< 因为钙的总量不变,若通入的N2中混有少量O2,所得产物中会混有氧化钙,因为氮的相对原子质量小于氧的相对原子质量,结果m2偏大,n(N)会偏大,所以x值会减小
15.(1)3 (2)+5 (3)①
16.N2,H2,O2体积一共为60mL,H2和O2化合成水剩余气体体积为15mL,消耗45mL气体.
由![]() 知:消耗30mLH2,15mLO2,剩余气体中O2为5mL、N2为10mL.
知:消耗30mLH2,15mLO2,剩余气体中O2为5mL、N2为10mL.
则20mL氨完全分解为10mLN2和30mLH2,即1mL氨由1/2mLN2和3/2mLH2组成,所以氨的化学式为NH3.
17.(1)金属 Ne (2)16 -2 SO3
(3)元素最低负化合价数值=-(8-最外层电子数)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




