上科版高中一年级第一学期化学教材第11页上列出了一个氧原子![]() 的相对原子质量的算式:
的相对原子质量的算式:
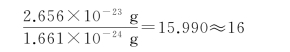
其中,2.656×10-23g是一个氧原子![]() 的质量;1.661×10-24g是一个
的质量;1.661×10-24g是一个![]() 原子质量的
原子质量的![]() 是该氧原子
是该氧原子![]() )的质量数。
)的质量数。
上科版高中化学拓展教材第4页上列有氯元素两种同位素![]() 和
和![]() 的相对原子质量分别为:34.969和36.966,34.969≈35,36.966≈37。
的相对原子质量分别为:34.969和36.966,34.969≈35,36.966≈37。
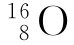 、
、![]() 的相对原子质量近似等于其质量数,但都略小于其质量数,这其中的原因是什么呢?
的相对原子质量近似等于其质量数,但都略小于其质量数,这其中的原因是什么呢?
* * *
我们知道,原子是由原子核和核外电子构成的,原子核又是由质子和中子构成的。忽略电子的质量,将原子核内所有的质子和中子相对质量取近似整数值,加起来所得的数值,称为质量数。
若按上科版高中一年级第一学期化学教材第8页表1.1列出的质子、中子相对质量为1.007、1.008,忽略电子的质量(电子的相对质量为0.00055),则:
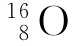 的相对原子质量约为:8×1.007+8×1.008=16.12
的相对原子质量约为:8×1.007+8×1.008=16.12
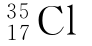 的相对原子质量约为:17×1.007+18×1.008=35.263(https://www.xing528.com)
的相对原子质量约为:17×1.007+18×1.008=35.263(https://www.xing528.com)
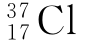 的相对原子质量约为:17×1.007+20×1.008=37.279
的相对原子质量约为:17×1.007+20×1.008=37.279
可见,![]() 的相对原子质量应比其质量数16大才合理
的相对原子质量应比其质量数16大才合理![]()
![]() 的相对原子质量也应比其质量数35、37大才合理,为什么其实际的相对原子质量比计算出来的相对原子质量和质量数数值要小呢?
的相对原子质量也应比其质量数35、37大才合理,为什么其实际的相对原子质量比计算出来的相对原子质量和质量数数值要小呢?
由于质子和中子结合成原子核时要放出巨大的能量(核聚变),根据爱因斯坦质能方程:E=m c2(E 表示能量,m 表示质量,c表示光速2.998×108m·s-1),物质的能量与它的质量呈正比,如果物质的能量增加了ΔE,物质的质量也相应地增加Δm,反之亦然,即ΔE=Δm c2。由此可知,质子和中子若结合成原子核就有质量亏损。例如,1 mol D(氘21H)的质量比1 mol质子和1 mol中子的质量和小约0.004 312 g,这一差值就是质量亏损。当然质量的亏损不是质量的消灭,因为核反应时,能量以辐射形式释放出来,辐射场有质量也有能量,核反应后核子的质量再加上辐射场的质量,其反应前后的总质量是守恒的。
因此,一个原子核的质量不等于构成它的单个核子(质子、中子)质量的简单加和,一个原子的质量也不等于构成它的质子、中子和电子质量的简单加和。上述![]() 的数据就证明这一点。高一年级化学教材中质子、中子的质量是指质子、中子的静止质量。
的数据就证明这一点。高一年级化学教材中质子、中子的质量是指质子、中子的静止质量。
那么,是否所有原子的相对原子质量都比其质量数小呢?
查阅相关资料后得到的数据如表2所示。
表2 常见元素的质量数和相对原子质量
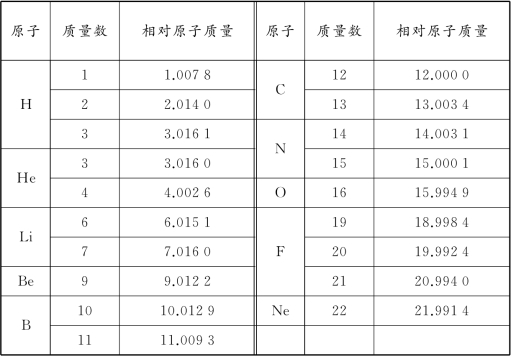
从表2中可以看出,只有质子数大于8(包括8)的元素的同位素的相对原子质量才小于它的质量数,而质子数小于8的元素的同位素,其相对原子质量是大于质量数的。其原因是质子数小于8的元素核子数较少,聚变为核时“亏损”质量也较少;质子数大于8的元素核子数较多,聚变为核时“亏损”的质量也较多。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




