长期以来,医药界一直希望能找到一种方法,可以在需要的时候将需要的药物量投入至需要的人体器官。利用智能型高分子可以实现对病灶周围的温度、化学环境等异常变化自动感知,自动释放所需量的药物。当身体正常时,药物控释系统恢复原来的状态,重新抑制释放。图12-20为智能膜材的药物渗透和释放模型示意图。A中药物在智能膜的一侧,通过外界环境的改变,膜孔道可以由“关”的状态到“开”的状态,从而使药物从膜的一侧渗透到另一侧;B中药物被智能膜包裹在中间,通过调节外界环境使膜的孔道打开,药物则从膜的内侧释放到膜的外侧。
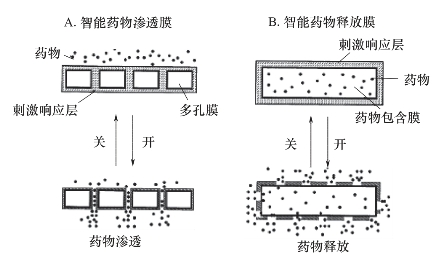
图12-20 智能膜材的药物渗透和释放模型示意图
将电解质单体如丙烯酸、交联剂及光引发剂的混合溶液通过喷射法或浸渍法浇铸在PET或聚碳酸酯多孔膜上,经紫外光照射可制成pH敏感膜。这种pH敏感膜对甲基蓝(methylene blue)的控制释放能力如图12-21所示。甲基蓝只在酸性介质中能够透过膜,而在中性及碱性介质中则不透过。这是由于在酸性条件下,聚丙烯酸分子链由于离子亲和而产生收缩,从而使浇铸膜孔道开放,甲基蓝得以通过。相反,在中性或碱性条件下,聚丙烯酸发生解离,离子间产生相互排斥而使分子链变成伸展状态,从而将膜的孔道堵塞,而拒绝甲基蓝通过。
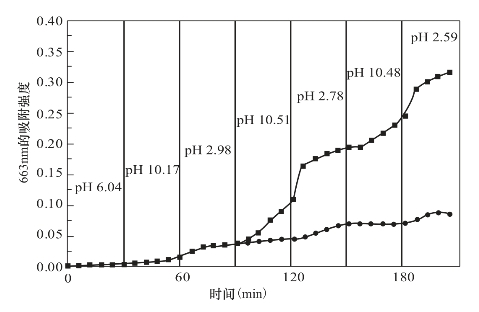
图12-21 甲基蓝(0.1g/l)通过复合膜(含25%PAA)的pH响应性
孔径:■,10μm;●,2.0μm(https://www.xing528.com)
采用等离子诱导填孔接枝聚合法将PNIPAAm开关接枝到PVDF膜孔上,同自由基聚合法制备的PNIPAAm交联水凝胶结合,可组成一种温度感应复合型控制释放膜系统。在该膜系统中,PNIPAAm接枝PVDF膜作为控制释放开关,PNIPAAm交联水凝胶作为药物载体该复合膜系统对NaCl有较好的正相控制释放效果,即在环境温度高于LCST时,NaCl的释放速率显著大于低于LCST时的释放速率,表现出良好的温度感应特性,并且通过降低水凝胶的交联程度以及开关膜的接枝率可以加强NaCl的释放,从而达到有温度感应控制释放的目的。
四乙基原硅酸盐/壳聚糖IPN膜是一种可以用于药物释放体系的pH敏感膜。该膜在pH=2.5时溶胀,在pH=7.5时收缩,而与四乙基原硅酸盐和壳聚糖的配比无关。当环境pH改变时,四乙基原硅酸盐/壳聚糖IPN膜的药物渗透性能会迅速发生变化,当pH从2.5变至7.5时,该膜的药物渗透速度增大。图12-22为药物通过该膜的机理示意图,即药物同时从壳聚糖分子内部和四乙基原硅酸盐与壳聚糖的孔隙中透过。四乙基原硅酸盐作为膜的刚架,并不随pH改变而溶胀,但IPN膜内部的壳聚糖却随着外界pH的改变而溶胀或收缩。当pH低时,壳聚糖被离子化而溶胀,像关闭阀门一样阻塞了膜的孔隙。这种pH敏感膜在药物载体和生物分离方面有很好的应用前景。

图12-22 药物同时在TEOS IPN和壳聚糖孔径渗透和仅在壳聚糖膜孔径渗透机理的示意图
●:![]() ; ○:NH2
; ○:NH2
聚(乙烯-co-乙烯醇)(EVAL)和氨基乙酸改性的EVAL敏感膜,可用于特种克隆药物的释放。EVAL膜和改性EVAL膜的结构都较为紧密,几乎不存在孔隙。环境温度为37℃,无论EVAL膜或是改性EVAL膜,在pH=2.0时,对5-对氨基水杨酸(5-ASA)的渗透性都非常小,而这一特征刚好符合在酸性条件下阻碍特种克隆药物释放的要求。24h后5-ASA在pH=2.0和pH=7.4条件下的渗透相对值(relativevalues)分别为6倍和41倍。很显然,与EVAL膜相比,改性EVAL膜对5-ASA渗透能力的显著提高非常适合于溃疡性结肠炎的定位治疗。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




