1.电位-pH值图及表示方法
金属的电化学腐蚀绝大多数是金属与水溶液相接触时发生的腐蚀过程。水溶液中总有H+和OH-,这两种离子含量的多少由溶液的pH值表示。而金属在水溶液中的稳定性不但与它的电极电位有关,还与水溶液的pH值有关。若将金属腐蚀体系的电极电位与溶液pH值的关系绘制成图,就能直接从图上判断给定条件下发生腐蚀反应的可能性,这种图称为电位-pH值图。电位-pH值图是基于化学热力学原理建立起来的一种电化学平衡图,以直观的图形表达了与金属腐蚀有关的各种化学平衡和电化学平衡。这种图指示人们通过控制电位或改变pH值来达到防止金属腐蚀的目的。
电位-pH值图上的线段有三种类型,如图1-23所示。现就以Fe-H2O系统所涉及的化学反应为例加以说明。
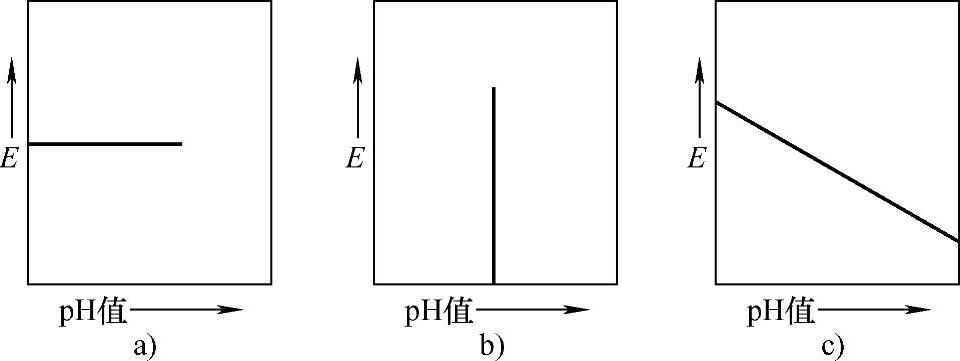
图1-23 三种电位-pH值图
a)水平 b)垂直 c)倾斜
(1)水平线段(图1-23a) 电极反应可以是均相反应,即
Fe2+→Fe3++e-
也可以是多相反应,即
Fe→Fe2++2e-
这个电极反应的特点是只出现电子,而没有氢离子或氢氧根离子出现,即整个反应与pH值无关。根据能斯特方程[式(1-59)]其平衡电极电位E(Fe2+/Fe)可写为
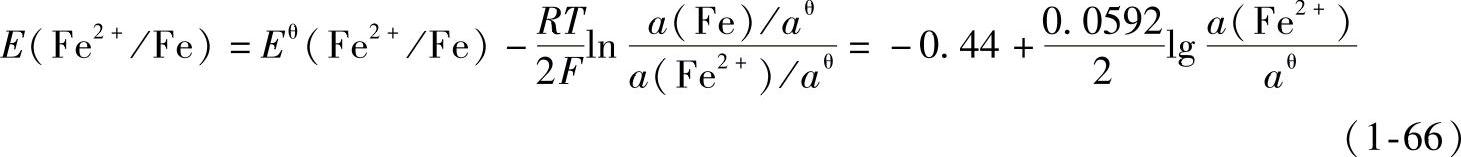
此类电极反应的电极电位与pH值无关,在电位-pH值图上为一水平线段。
(2)垂直线段(图1-23b)元素在水系中发生的反应可分为有电子得失的氧化还原反应和无电子得失的非氧化还原反应两类。如:
均相反应
Fe3++H2O→FeOH2++H+
多相反应
Fe2++2H2O→Fe(OH)2+2H+
这些反应的特点是只有氢离子(或氢氧根离子)出现,而无电子转移(或得失),属于非氧化还原反应,不构成电极反应,不能用能斯特方程表示电极电位与pH值的关系。可以从反应的平衡常数表达式得到表示电位-pH值图相应曲线的方程。
在一定温度下,反应Fe2++2H2O→Fe(OH)2+2H+的标准平衡常数为

对上式两边取对数得
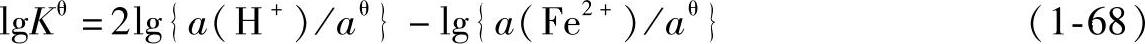
查表得lgKθ值为-13.29,所以有
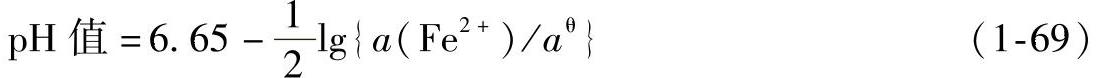
此类反应的通式可写为
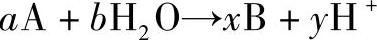
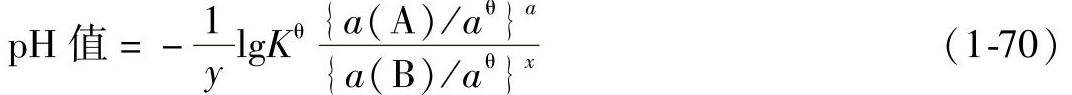
可见此类反应的pH值与电极电位无关,在一定温度下(Kθ一定),A、B的活度一定,则pH值为定值。在电位-pH值图上此类反应表示为一垂直线段。
(3)斜线段(图1-23c)有电子得失的氧化还原反应,如:
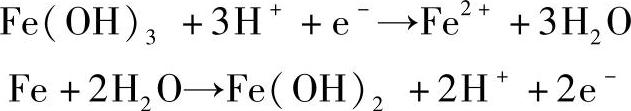
这些反应的特点是既有氢离子(或氢氧根离子)出现,又有电子出现,以Fe(OH)3+3H++e-→Fe2++3H2O为例,其平衡电极电位为(https://www.xing528.com)
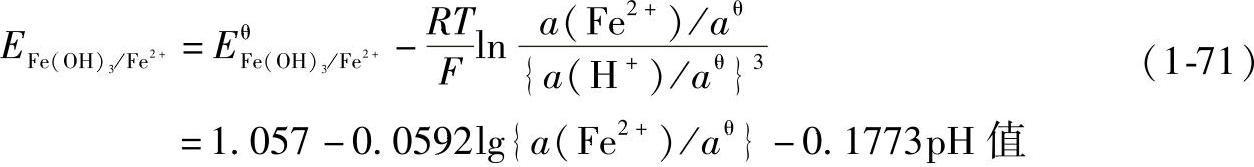
若以下标R、O分别表示物质的还原态(如Fe2+)和氧化态[如Fe(OH)3],则这类电极平衡电极电位的普遍形式可写为
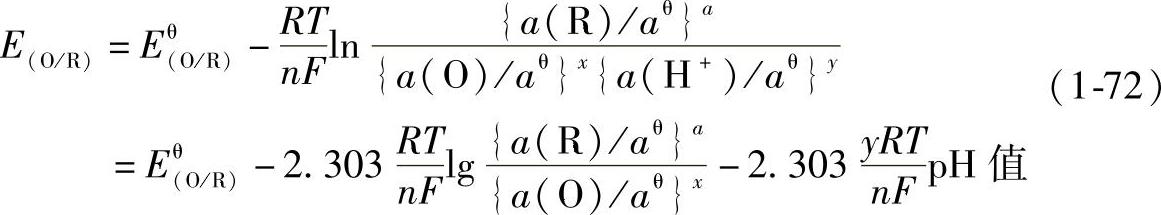
此式表明,在一定温度下,给定氧化还原物质的活度,平衡电极电位随pH值升高而降低,在电位-pH值图上为一斜线段,其斜率为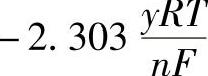 。
。
2.电位-pH值图的主要应用
电位-pH值图主要有以下三方面用途:预测反应的自发方向,从热力学上判断金属腐蚀趋势;估计腐蚀产物的成分;预测减缓或防止腐蚀的环境因素,选择控制腐蚀的途径。
以Fe-H2O体系的简化电位-pH值图为例。如果假定以平衡金属离子浓度为10-6mol·L-1作为金属是否腐蚀的界限,即溶液中金属离子的浓度小于此值时就认为未发生腐蚀。那么,对于Fe-H2O体系可得到如图1-24所示的简化电位-pH值图,图中有三个区域:
1)腐蚀区。在该区域内处于热力学稳定状态的是可溶性的Fe2+、Fe3+、FeO42-和HFeO2-等离子。因此,金属处于不稳定状态,可能发生腐蚀。
2)稳定区。在此区域内金属处于热力学稳定状态,因此金属不发生腐蚀。
3)钝化区。在此区域内的电位和pH值条件下,生成稳定的固态氧化物、氧氧化物或盐膜。因此,在此区域内金属是否遭受腐蚀,取决于所生成的固态膜是否有保护性,即它能否进一步阻止金属的溶解。
例如,从图1-24中A、B、C、D、E各点对应的电位和pH值条件,可判断金属的腐蚀情况。若Fe在A点位置,则因该区是Fe和H2的稳定区,Fe不会发生腐蚀;若Fe在B点位置,则因该区是Fe2+和H2的稳定区,Fe出现析氢型的腐蚀;若Fe在C点位置,则因该区对Fe2+和水是稳定的,因此Fe仍将发生腐蚀,但由于Fe处于C点的电位E位于@线之上,因此将不发生H+还原,而是发生电位比E更正的氧还原过程;若铁在D点位置,则因该区处于Fe2+和H2O稳定区,Fe在该区发生腐蚀,并在酸性介质中发生有氧的还原反应;若Fe在E点位置,则因该区处于Fe2O3和H2O稳定区,Fe在该区发生溶解的同时伴有在碱性介质中氧的还原反应,因为Fe表面生成保护性的Fe2O3膜,故Fe处于钝化状态。
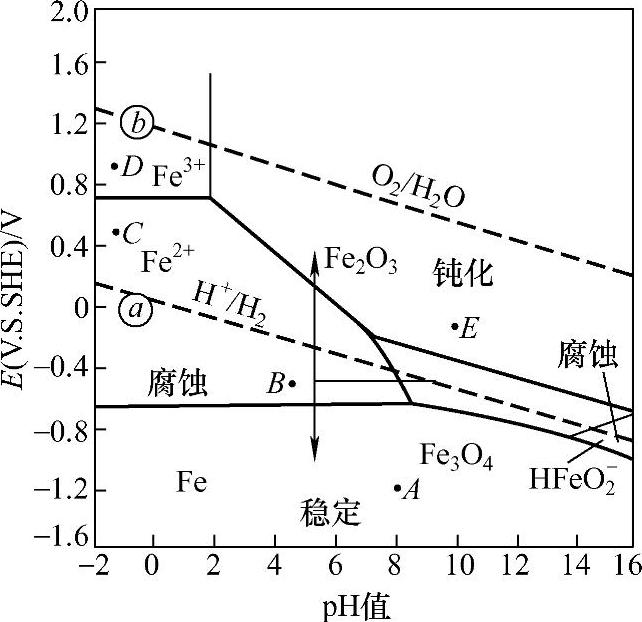
图1-24 Fe-H2O体系的简化电位-pH值图
由此可见,上述五个点的位置(电位、pH值)不同,Fe的腐蚀倾向和腐蚀产物也不同。
通过金属-H2O体系的电位-pH值图,还可以从理论上选择控制腐蚀的有效途径。例如,在Fe-H2O体系的电位-pH值图(图1-24)中,将铁从B点移出腐蚀区,防止或降低Fe的腐蚀有三种可能的途径。
1)阴极保护。当溶液pH值较低时,设法使Fe的电极电位移向负方向(-0.6V以下),铁处于稳定区,不受腐蚀,这就是通常采用的阴极保护方法。用牺牲阳极法即用电极电位为负的锌或铝合金与铁连接,构成腐蚀电偶,或用外加直流电源的负端与铁相连,而正端与辅助阳极连接,构成回路,都可保护铁免遭腐蚀。
2)阳极保护。当溶液pH值较高时,可将铁的电极电位移向正方向,使铁进入钝化区,减少腐蚀,此所谓阳极保护。可通过外加电流阳极保护或在溶液中添加阳极型缓蚀剂或钝化剂来实现。这种方法应用十分有限,它主要适用于强氧化性介质,且这个系统中金属趋向钝化。有时由于钝化剂加入量不足,或者阳极保护参数控制不当,金属表面保护膜不完整,反而会引起严重的局部腐蚀。当溶液中有Cl-存在时,还需要注意防止点蚀的出现。
3)调整溶液pH值。调整溶液pH值=9~13,也可使铁进入钝化区而不受腐蚀。应注意,如果由于某种原因(如溶液中含有一定量的Cl-)不能生成氧化膜,铁将不能钝化而继续腐蚀。
常用金属的电位-pH值图如图1-25所示。
3.电位-pH值图应用的局限性
借助电位-pH值图可以预测金属在给定条件下的腐蚀倾向,为解释各种腐蚀现象和作用机理提供热力学依据,也可为防止腐蚀提供可能的途径。因此,电位-pH值图已成为研究金属在水溶液介质中腐蚀行为的主要工具。但其应用存在以下一些局限性:
1)由于金属的理论电位-pH值图是根据热力学数据绘制的电化学平衡图,所以它只能用来预测金属腐蚀倾向的大小,而无法预测金属的腐蚀速度。
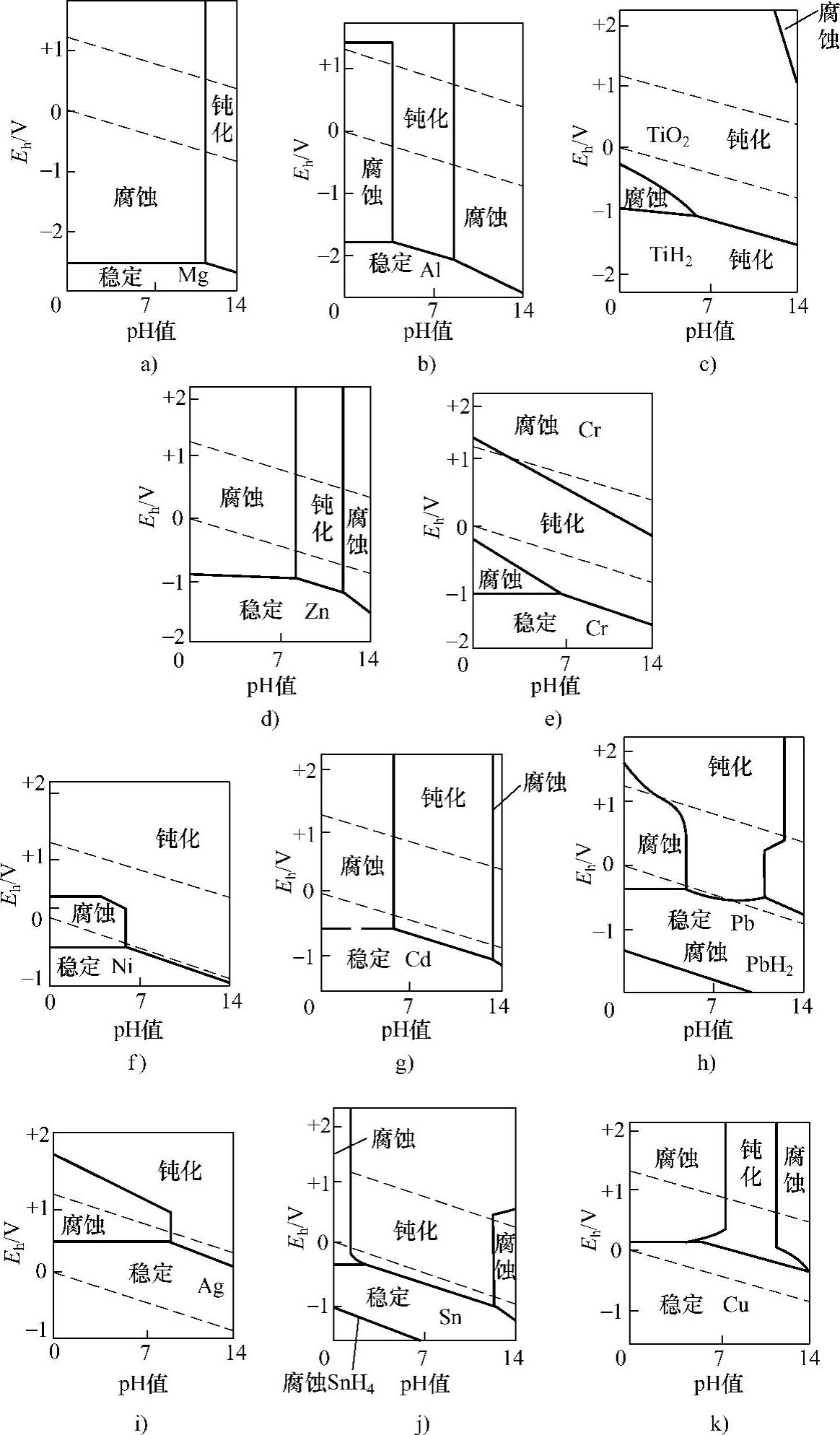
图1-25 常用金属的电位-pH值图
a)Mg b)Al c)Ti d)Zn e)Cr f)Ni g)Cd h)Pb i)Ag j)Sn k)Cu
2)由于它是热力学平衡图,它表示的都是平衡状态的情况,而实际腐蚀体系往往又是偏离平衡状态的,因此,利用表示平衡状态的热力学平衡图来分析非平衡状态的情况,必然存在一定的误差。
3)电位-pH值图只考虑了OH-对平衡产生的影响,但在实际腐蚀环境中,却往往存在着Cl-、SO42-、PO34-等阴离子,这些阴离子对平衡的影响未加考虑,同样也会引起误差。
4)电位-pH值图中溶液的浓度是溶液的平均浓度,而不能代表金属反应界面的真实浓度和局部反应浓度。
5)电位-pH值图上的钝化区,指出金属表面生成了固体产物膜,如氧化物或氢氧化物等,至于这些固体产物膜对金属基体的保护性能如何并未涉及,相当于只提供了基体金属受保护的必要条件,并不能确保满足充分条件。固体产物膜是否具有保护金属的作用,还需要根据实际情况来定。
虽然理论电位-pH值图有如上所述的局限性,但补充一些金属钝化方面的试验或试验数据,就可以得到实用电位-pH值图,如再综合考虑有关动力学因素,那么它将在金属腐蚀研究中发挥更广泛的作用。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




