第一步 药液的配制与滤过
1.称 量
(1)配料前核对原辅料名称、批号、生产厂家、规格及数量应与检验报告单相符,如发现原辅料包装、外观、色泽、形态有差异应及时与生产与质量部门联系。
(2)按批生产指令要求,一人称量,另一人复核。无复核不得称量投料。操作人、复核人均应在称量原始记录上签名。
(3)剩余的原辅料应密封储存,在容器外标明品名、批号、日期、剩余量及使用人签名。
(4)天平、磅秤每次使用前应校正,并定期由专人校验,做好标贴及记录(表4-1)。
表4-1 称量岗位生产记录

2.配 制
(1)配料前先用注射用水冲洗配料罐内外、标尺,用滤过的合格注射用水冲洗管道、罐内用纯蒸汽消毒。
(2)检查电机、减速器,接通电源后,试转一下,看运转是否可靠。如发现减速器有异声,电机不转,应请维修工检查,排除故障。有蒸汽加温的配料罐,接通蒸汽时,先开排汽阀门,再开进汽阀门,进汽应先小后大,压力一般不要超过0.1 MPa,以免损坏管路,造成事故。
(3)查看配料水化验合格单,水质合格方可投料。使用的注射用水应在80 °C以上保温,储存时间不得超过12 h。
(4)开启阀门,将注射用水注入配液罐中至总体积的80%(冷却至约30 °C),关闭进水阀门,通入惰性气体(CO2),饱和后加入维生素C,搅拌,缓缓加入碳酸氢钠,边加边搅拌使之中和作用完全,气泡不再产生为止,再将已溶于注射用水的依地酸二钠、半胱氨酸盐及焦亚硫酸钠溶液加入,搅匀,用惰性气体(CO2)饱和的注射用水加至全量。
(5)待药物全部溶解后,取样测定含量、pH、查看色泽,并同时通CO2气体封液面。填写生产记录(表4-2)。
表4-2 配液岗位生产记录

3.过 滤
待半成品检验合格后用砂滤棒或钛棒粗滤,0.45 μm精密滤芯精滤至澄明。
4.清 场
(1)每天(或每批)生产结束后必须严格清场。连续生产时配料缸、容器、滤器管道及下道工序灌封机药液管应用热注射用水冲洗干净(特殊品种例外),并用注射用水灌满浸泡过夜。更换产品必须全部拆除清洗。
(2)清场结束后,应及时、认真填写清场记录。
理论链接1 注射用油
注射用油指精制的植物油。除应符合《中国药典》各项规定外,应精制使其符合下列规定。
(1)注射用油应无异臭,无酸败味,色泽不得深于黄色6号标准比色液;在10 °C时应保持澄明。
(2)碘值应为79~128,酸值不大于0.56,皂化值应为185~200,并不得检出矿物油,含水量及杂质均不得超过0.2%。
碘值反映油中不饱和键的多少,过高表示含不饱和键多,油易氧化酸败;过低表示含有较多的蜡类杂质。酸值表示游离脂肪酸的多少,过高表示油脂酸败严重,可影响某些药物的稳定性,且有刺激性。皂化值表示油中游离脂肪酸和结合成酯的脂肪酸总量。过低表明油中脂肪酸相对分子质量较大或含不皂化的杂质较多;过高表明脂肪酸相对分子质量较小,亲水性较强,
已精制的注射用油采用150~160 °C进行1~2 h的干热灭菌,注射用油应贮于避光密闭洁净容器中,避免与日光、空气接触。
理论链接2 其他注射用溶剂
对于不溶或难溶于水或在水溶液中不稳定的药物常用非水溶剂制备注射液。常用的非水溶剂有以下几种。
(1)水溶性非水溶剂有乙醇、甘油、1, 2-丙二醇、聚乙二醇300、聚乙二醇400等,其中丙二醇必须用1, 2-丙二醇。一般使用浓度均在50%以下,特别是乙醇,10%肌内注射时已产生疼痛。而甘油与丙二醇浓度为50%时,黏稠度已使生产与使用感到不便。
(2)常用的油溶性非水溶剂有苯甲酸苄酯,与注射用油制成复合溶剂可增加二巯基丙醇在油中的溶解度及稳定性。油酸乙酯可被组织迅速吸收,常在激素类药物中使用。其他油溶性非水溶剂有乳酸乙酯等。
以上各种非水溶剂均应符合注射用或药用规格,不能用化学试剂代替。
理论链接3 防止主药氧化的附加剂
常用的有抗氧剂、惰性气体及金属离子络合剂等。
抗氧剂是一些比药物更易氧化的还原性物质,当抗氧剂与易氧化药物共存时,空气中的氧气先与抗氧剂发生作用,消耗氧气,从而使主药保持稳定。常用的水溶性抗氧剂有亚硫酸氢钠、焦亚硫酸钠、亚硫酸钠、硫代硫酸钠等,其中前两种适用于偏酸性药液,后两种适用于偏碱性药液。
通入惰性气体可驱除安瓿与药液中的氧气,生产上常用的高纯度的惰性气体有氮气和二氧化碳,从除氧的效果看,二氧化碳优于氮气;但二氧化碳在水中呈酸性,故不宜用于磺胺嘧啶钠等强碱弱酸盐或钙盐等注射剂,否则易析出沉淀。
原料、辅料、溶媒或制药器械等可能携带微量金属离子,可催化氧化反应的进行。常用一些金属螯合剂,来消除金属离子对药液的影响,常用的有EDTA-Na2(依地酸二钠)和EDTA-CaNa。
第二步 安瓿搬运、清洁、理瓶
1.安瓿的领取、转运与整理
(1)安瓿应有专人验收,对规格、批号、生产厂家、数量、内外包装质量进行核对,并检查检验合格单,核对无误后,领发料双方在领料单上签字。
(2)将安瓿箱送至清包间拆包,拆包前用微湿毛巾擦去箱外灰尘,打开纸箱,将纸箱内安瓿小盒依次取出,顺序放到小车上运到装盘处。
(3)将安瓿不锈钢盘经纯水洗净烘干后(若潮湿可用干毛巾擦干),将不锈钢盘送到装盘处。
2.安瓿装盘
(1)将小盒内安瓿逐盒装入不锈钢盘中,直至盘装满。
(2)在装盘过程中,挑出破裂、炸底等废损安瓿,置规定容器中。
(3)将安瓿盘放在车上,盘之间不能相互叠压。
3.安瓿搬运
应小心搬运,将安瓿送至洗、灌、封岗位。
4.工作完毕
(1)将安瓿盘放置一边,经适当清洁后,供下次使用。
(2)将安瓿纸箱、小盒整理好送到规定存放处,空盘依次放好,整齐堆放。
(3)将破损安瓿送入规定场所堆弃,清理作业现场至符合要求。
(4)按规定填写生产记录。
理论链接4 抑制微生物生长的附加剂
大多数注射剂均经过灭菌,无需使用抑菌剂。但某些采用低温间歇灭菌、滤过除菌、无菌操作法制备和多剂量包装的注射剂均须加入抑菌剂。但供静脉注射、脊椎注射的注射剂及一次用量超过5 mL的注射液不能加抑菌剂。常用的抑菌剂为苯甲醇、三氯叔丁醇等。
第三步 安瓿的洗、烘、灌封
1.准备工作
(1)冲洗精密滤芯,检查滤芯安装是否严密。
(2)启动干燥机,使机器升温。
(3)开动超声波清洗机检查设备各部位运转是否正常,检查喷针位置是否对正瓶口,不正时及时调整。
(4)往水槽内加注射用水并调节水槽水温在50~60 °C。打开并调节各阀门,使压缩空气压力 > 0.15 MPa,循环水压力 > 0.2 MPa,喷淋水压力 > 0.06 MPa。
(5)循环冲洗清洗机管路10 min后,由QA检查员取样检查新鲜注射用水、循环水可见异物,确认水质合格。
(6)待干燥机高温段温度达到设置的300 °C时,方可进行联动线的生产操作。
2.安瓿清洗
(1)将待洗安瓿整齐堆码在清洗机进瓶盘上,同时将破瓶及不合格的安瓿(不规则口、破口、瓶壁有麻点、长短不齐、细口等)剔除。
(2)启动清洗机,进行洗瓶操作。
(3)安瓿的内部清洗程序为超声波清洗—循环水—循环水—压缩空气—新鲜注射用水—压缩空气—压缩空气—压缩空气。安瓿的外洗是通过安瓿在水池内的浸泡和当安瓿在滚筒上转位时由喷射水流及圆弧滑道上反弹回来的水流进行冲洗。
(4)开机后应随时观察水、气压力表压力值是否符合要求。安瓿进入烘箱处是否排列整齐。机器运行过程中是否有断针,碎瓶、浮瓶等异常情况。发现问题应及时处理。
(5)严格检查精洗后的安瓿质量,遇安瓿没洗干净或有破损应立即挑出,不得流入烘箱。
3.安瓿烘干灭菌
(1)设定烘干杀菌温度为300 °C,设定温控停机温度为100 °C。
(2)启动工作按钮,各层流风机开始运转。此时各层流指示灯亮,加热管正在加热,温度记录仪开始记录。如果有任一指示灯不亮,说明有故障,机器会自动停机。
(3)检查电热管加热情况,转动电流开关,观察电流指示表显示的电流情况。
(4)开启按钮,与清洗机联锁,安瓿进入干燥机。
(5)开启按钮,与灌封机联锁,安瓿进入灌封机,当三机连线正常工作时,全线安瓿进行自动平衡。
4.灌 封
(1)同送气岗位联系,确认送气生产符合要求。
(2)与配制岗位操作人员联系好用注射用水冲洗管道、灌封机至少10 min,排尽残水。(https://www.xing528.com)
(3)用药液冲洗管道、针头。检查药液色泽、可见异物,合格后方可试装。
(4)缓慢打开火源阀,立即点火、调整好火焰强度打开主机开关,调整针头与装量。要求针头插入安瓿的深度和位置适中,装量符合该品种半成品控制要求。
(5)开启灌封机,开始进行正式生产操作。
(6)在灌封机出瓶斗处将灌封后的安瓿装满洁净周转盒,上好挡板,逐盘放入标签并标明:品名、批号、规格、机台号,将周转盒及时传至下一工序灭菌。
(7)在操作过程中要随时检查从烘干机出来的安瓿,用镊子将不合格品(包括掉底、裂纹、破口、长短不齐、细口等)剔除,保证供瓶连续。
(8)灌封过程中要随时检查装量和封口质量,及时剔除炭化,漏封、封口不好、装量不合格等不合格品,生产结束后集中销毁。
(9)在灌封操作过程中要注意惰性气体的压力变化,保证充填足够的惰性气体。惰性气体冲入量以液面微动为宜。
(10)灌封结束后,关闭火源、电源;将设备上剩余的未灌装的安瓿通过传递窗返至安瓿清洗间,第二天使用前重新清洗、灭菌。
填写生产记录(表4-3)
表4-3 洗烘瓶岗位生产记录

续表

理论链接5 pH调整剂
常用的pH调整剂有盐酸、硫酸、枸橼酸及其盐类和氢氧化钠、氢氧化钾、碳酸氢钠等。缓冲剂有磷酸二氢钠和磷酸氢二钠等。在选择pH调整剂时一般采用与主药同离子的酸或作用后能产生水的碱。
第四步 灭菌检漏
1.灭菌前准备
必须严格检查灭菌柜、烘房、工作场地有无前批药品遗漏,以免混药、混批及重复灭菌。
2.灭 菌
(1)按灌封好的产品顺序检查车号盘数,按产品品种要求掌握灭菌温度、时间(本产品的灭菌条件是100 °C、15 min),灌封到灭菌时间越短越好,从配料至灭菌结束时间不超过6 h。
(2)按产品工艺要求控制产品灭菌温度。升温时间一般为15 min,特殊品种要求为10 min以内。锅内最高气压不超过0.12 MPa,温度升到工艺规定时,开始计算保温时间,其间要求温度恒定,适时补充蒸汽。
3.检 漏
(1)保温结束关闭蒸汽阀,开排气阀直至柜表压为零,开进水阀和排水阀至产品冷却后关闭。
(2)开进色液阀,根据产品将配制的色液泵入柜内至灭菌产品全部浸在色液中(一般白瓶用红色液,棕瓶用蓝色液)。
(3)开真空阀检漏,真空度达到0.08 MPa的时间不少于10 min,然后关闭真空阀,开放空阀至常压,待20 min后开排液阀排尽色液,用纯化水清洗后开柜门,拉出灭菌车,逐盘挑出漏头破瓶,挂上已灭菌的状态牌。
(4)认真填写原始记录,详细记录灭菌柜号、产品、温度,时间、漏头和爆头等数据(表4-4)。
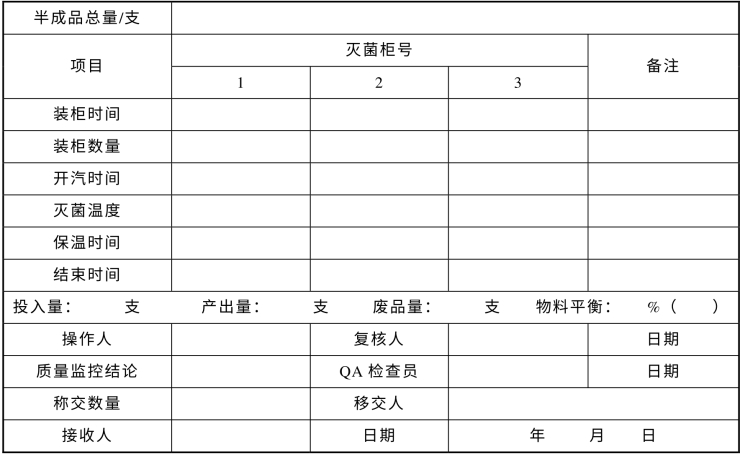
表4-4 灭菌、检漏生产记录

续表
第五步 灯检
1.生产前准备
(1)核对本批产品的品名、规格、批号、生产数量。
(2)检查是否有前次“清场合格证”副本。
(3)检查灯检室、容器具、灯检架是否有“已清洁”状态标识,且在有效期内。
(4)检查合格后,班长根据生产指令取下现场状态标识牌,换上“生产运行中”状态标识,标明本岗位需要生产的药品品名、批号、规格、生产批量、生产岗位、生产日期、操作人以及复核人。
(5)领取中间产品。
2.生产操作过程
(1)接通澄明度检测仪电源,打开荧光灯。
(2)启动照度开关,测定照度,同时旋转仪器上部的照度调节旋钮至所需照度为止。
(3)灯检岗位操作工从物料架上取一装有中间产品的周转盘,开口端朝上,斜靠于灯检架的左前方,撤下挡板。
(4)复核周转盘中中间产品的数量。
(5)从另一操作架上取一个贴标印字用空周转盘,开口端靠在灯检架的内壁上。
(6)灯检岗位操作工右手拿起夹子,用力使夹子张开后伸到周转盘中,夹起10~15支灭菌后的中间产品,拿到灯检架前面的荧光灯旁边。
(7)将夹子从上向下振动一次后迅速返回原位置,轻轻振动夹子,使药液下流,眼睛距离安瓿25 cm,逐支检查药液中有无异物和碳化点,药液装量是否合格,重复操作3遍。
(8)检查合格的中间产品摆放于正前方的空周转盘中。
(9)不合格的中间产品剔出,分类放于特制的周转盘中,待灯检操作结束后统一销毁,并记录。
(10)反复操作直至灯检结束,将不合格品数清,倒入套有塑料袋的废弃物桶中进行处理。
3.生产结束后的操作
(1)灯检岗位操作工填写中间产品递交单,进行中间产品的交接,中间产品转入外包装岗位,中间产品递交单自留一份贴于批生产记录上,交给外包装岗位操作工一份。
(2)按照《一般生产区容器具及工器具清洁规程》《一般生产区厂房清洁规程》和《一般生产区周转车清洁规程》进行各项清洁。
(3)质量保证部监控员检查合格,在“清场记录”上签字,并签发“清场合格证”正副本。
(4)灯检工序班长将正本“清场合格证”“清洁记录”“清场记录”纳入本批批生产记录,副本“清场合格证”插入灯检室“已清洁”标识牌上,作为下次生产前检查的凭证,纳入下批批生产记录中。
(5)灯检工序班长将填写好的批生产记录(表4-5)整理后交给车间主任。
表4-5 灯检批生产记录

理论链接6 渗透压调节方法之冰点降低数据法
冰点降低数据法:调节渗透压的依据是冰点相同的稀溶液具有相同的渗透压。一般情况下,血浆的冰点为-0.52 °C,因此任何溶液,只要其冰点降低为0.52 °C,即与血浆等渗。药物水溶液的冰点降低数据:根据这些数据可以计算该药物配成等渗溶液的浓度。等渗调节的用量可用下式进行计算。
![]()
式中 W——配成等渗溶液所需加入药物的百分含量,g/100 mL;
a——未经调整的药物溶液的冰点下降度数;
b——用以调整等渗的药物1% (g/mL)溶液的冰点下降度数。
例:配制100 mL 1%盐酸普鲁卡因溶液,需要加多少氯化钠,使之成等渗溶液?
查表得a=0.12 °C,b=0.58 °C代入上式得:
![]()
即100 mL盐酸普鲁卡因溶液需增加0.69 g氯化钠,可使1%的盐酸普鲁卡因溶液成为等渗溶液。
理论链接7 渗透压调节方法之氯化钠等渗当量法
氯化钠等渗当量法:药物的氯化钠等渗当量指与1 g药物呈等渗效应的氯化钠的量。从表中查出药物的氯化钠等渗当量后,可计算出等渗调节剂的用量,计算方法如下式:
![]()
式中 X——配成V mL等渗溶液所需加入氯化钠的质量,g;
V——配制溶液的体积,mL;
E——药物的氯化钠等渗当量;
W——V mL溶液中所含药物的质量,g;
0.009——每1 mL等渗氯化钠溶液中所含氯化钠的质量,g。
例:若配制2%的盐酸麻黄碱溶液1 000 mL,欲使其等渗,需加入氯化钠多少克?
查表可知,盐酸麻黄碱的氯化钠等渗当量E为0.28,2%的盐酸麻黄碱溶液l 000 mL含主药的量为2%×1 000=20 g。则
![]()
配制2%的盐酸麻黄碱溶液1 000 mL,应加入氯化钠的量为3.4 g,使其成等渗溶液。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




