骨类疾病是危害身体健康的一类严重疾病,如何解决骨类疾病带来的困扰已经成为医学界的一大难题[40]。经过人们在材料学和医学上的不断探索,骨水泥的发明和改进为骨类疾病患者在减轻痛苦、提高生活质量等方面做出了重要贡献。但传统骨水泥材料仍面临很多困难和挑战[37-39]。针对传统骨水泥目前存在的问题,并结合生物医学金属材料的特点,笔者实验室提出了一种全新概念、基于固液相转换的可注射式低熔点合金骨水泥[41]。
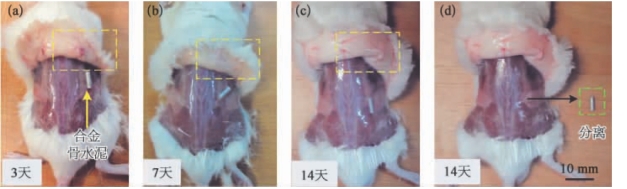
图12.5 小鼠皮下骨水泥的植入状况[41]
骨水泥植入小鼠背部皮下3d(a)、7d(b)和14 d(c)后,合金骨水泥的植入状况;d.合金骨水泥样品从小鼠背部剥离。
低熔点金属采用的是熔点为57.5℃的Bi35 In48.6 Sn16 Zn0.4,并采用BALB/c小鼠的活体实验来研究这种合金的生物相容性。选取9只8周龄雄鼠来进行合金骨水泥的皮下植入实验,分别在合金骨水泥皮下植入3d、7d和14 d后,对小鼠背部进行解剖。结果发现,几组植入皮下的合金样品,均能稳定地处于起初植入的原位皮下(图12.5),并没有由于小鼠的运动,造成空间上的移位,或者由于合金样品对组织的破坏而游移他处。因针头穿刺对皮肤造成的伤口在第3d时已经有了愈合的趋势(图12.5a),在第7d和第14 d的时候,完全看不出穿刺的位置,皮肤伤口已经愈合,其上的一些毛细血管也重新长出并恢复正常(图12.5b和c)。与合金接触的皮肤组织和肌肉组织无肉眼可见变化,移走合金样品后,合金下面接触的组织依然保持光滑完整(图12.5d)。移除的合金样品被黏膜包裹,结构完整,表面未有变色和腐蚀等变化。(https://www.xing528.com)
进一步研究证明,合金骨水泥样品植入后,周围组织会发生缓和的炎症反应,这些现象处于生物体对外来异物正常反应的合理范围之内。除此之外,组织未见剧烈炎症反应和细胞变异行为。在体实验的结果表明,合金骨水泥在相当长的一段时间内与组织具有良好的生物相容性。
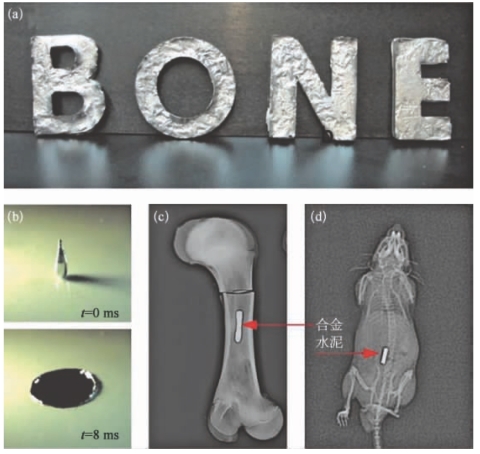
图12.6 合金骨水泥的注射式3D打印[41]
a.用合金骨水泥注模的“BONE”字样;b.高速摄像机所拍摄的液态合金液滴的液-固相变过程;c.骨腔内填充有合金骨水泥的X射线影像;d.对小鼠皮下植入合金水泥的X射线影像。
在合金骨水泥模具成型实验中,液态金属从离开注射器到冷却成型的整个过程大概经历10 min,表明了合金骨水泥材料注射性好、固化速度较快。在可塑性方面,如图12.6a所示,由于液态合金可以适形地填充于模型的边、角、曲、折等部位,所以液态合金凝固后形成的合金字母“B”、“O”、“N”、“E”组成的单词“BONE”轮廓清晰,说明液态金属的充型能力较强,能够根据模具的不同形状,实现多种特殊的造型。液态合金骨水泥被缓缓地从注射器中推出后,具有典型的液滴形态,并且有明亮的金属光泽,液滴在下降的过程中保持形态并竖直地落到平面上,结果如图12.6b所示。当液滴与平面撞击时,其形态开始发生变化,逐渐形成液膜,在经过多次往复振荡波动后趋于静止,这体现了其良好的流变性。与传统商业丙烯酸树脂骨水泥相比,合金骨水泥与骨组织的对比度更明显,在放射成像方面更具有优越性,图像效果更好(图12.6c和12.6d)。合金骨水泥优良的成像能力是自身具备的,所以免除了因添加其他成分而导致骨水泥改性的担忧。由于传统骨水泥是单向不可逆的液固转换过程,翻修时不得不切除一部分骨组织来实现对骨水泥及假体的移除。而且操作过程比较复杂,需要特殊的手术器械和熟练的手术技巧。对于合金骨水泥来说,因其固液相能够可逆地相互转换,即使变成了固体,也可以通过加热的方法令其熔化成为液态,便于移除。在加热探针和热电偶的配合下,既能实现合金骨水泥的固液转换,又可以监控界面骨组织的温度,降低骨组织发生热损伤的可能性。总的来说,通过选择合适的墨水,注射式3D打印可以用于合金骨水泥的医学应用。上面所介绍的合金骨水泥即是一个典型的在体3D植入式打印例子,体现出适形化打印的特点,同样,我们也可以用注射式3D打印快速制作一些微纳米生物电子器件。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




