将两极之间的液态金属小球增加至同时接触两极壁面而形成一个肾状体,在电极通电时可观察到与前述金属小球不同的运动现象。实验装置如图4.24所示,1 mL的NaOH溶液填充在两电极(尺寸为D=30 mm,d=4 mm)之间。NaOH溶液为液态金属提供一个推动力,并可及时去除液态金属表面的氧化物,使之转变为GaOOH,降低了氧化层的强度。另外,在液态金属、石墨电极、培养皿底部之间形成界面滑动层[49],滑动层会大大降低液态金属的摩擦力,同时也避免了电极之间的短路现象。当电极通电时,液态金属受洛仑兹力的驱动而环绕中心电极转动,其电流时间和电压时间测量曲线如图4.25所示,从图中可以看出,正负极的电压几乎保持常数(1.63 V),而电流则呈周期变化,拟合曲线的表达式为
![]()

图4.24 同心圆环形电极(D=30mm,d=4mm)之间的肾状体液态金属[45]
其中,I和t分别代表电流和时间,从拟合的电流时间曲线中算得频率为2.16s-1,这与实验测量值2.18rp(srevolutions per second)十分接近,表明通过液态金属的电流为正弦周期性变化。电流、电阻、功率和转速随电压的变化关系如图4.26所示。当电压小于1.82 V时,液态金属呈匀速圆周运动,在NaOH溶液中几乎没有气泡,通过金属的电流和消耗功率随电压的增大而增大,两极间电阻主要为接触电阻,阻值范围是2~2.6 Ω;当电压为1.63 V时,转速达到峰值,电压1.82 V是电流、功率变化趋势发生反转的转折点,电阻也由平稳变化开始急剧升高;当电压范围是1.82~3.63 V时,液态金属转速减缓,NaOH溶液中的气泡逐渐增多,电阻迅速变大,而电流迅速变小,功率的波动范围是0.95~1.41 W,转速电压曲线呈现下降趋势;当电压大于3.63 V时,NaOH溶液变得越来越浑浊,液态金属的转速越来越小并伴随着严重变形和剧烈碰撞,由于液态金属的铺展缩短了与电极板的间距,极板间电阻迅速下降,电流及功率相应变大。极板间较高的电压会导致NaOH溶液的电解度增大,这是不希望看到的,所以实现液态金属转速可控的理想电压范围是0~1.82 V,在该范围内NaOH溶液的电解度非常微弱,溶液中几乎没有气泡,这可由图4.27验证,图中显示了极间电压为0.6 V,时间分别在0s、0.6s、1.0s和1.48 s时的液态金属及电解液变化。
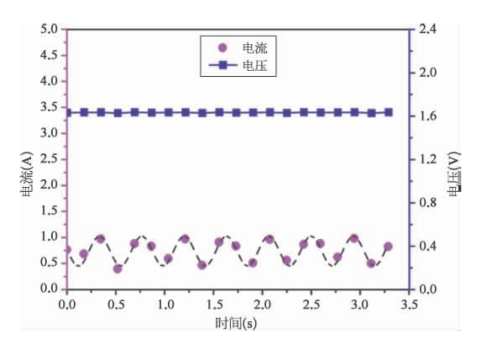
图4.25 肾状体液态金属匀速圆周运动时的电压-时间和电流-时间关系曲线图(短划线曲线是对电流测量值的拟合)[45]
NaOH溶液的浓度也是影响液态金属转速的一个重要因素,不同浓度下液态金属转速的测量结果如图4.28所示。金属的质量为9.8 g,电压调整为1.83 V,当溶液为去离子水(相当于NaOH溶液浓度为0 mol/L)或低浓度(0.2 mol/L)的NaOH溶液时,液态金属表面的氧化物不能被完全去除,施加在金属上的洛伦兹力不能克服运动摩擦力,这主要是由于金属和基底之间存在较大的黏附力,在电极通电时液态金属将发生变形和铺展,即电毛细效应[50];当NaOH溶液浓度大于0.4 mol/L时,液态金属将围绕中心电极旋转。(https://www.xing528.com)
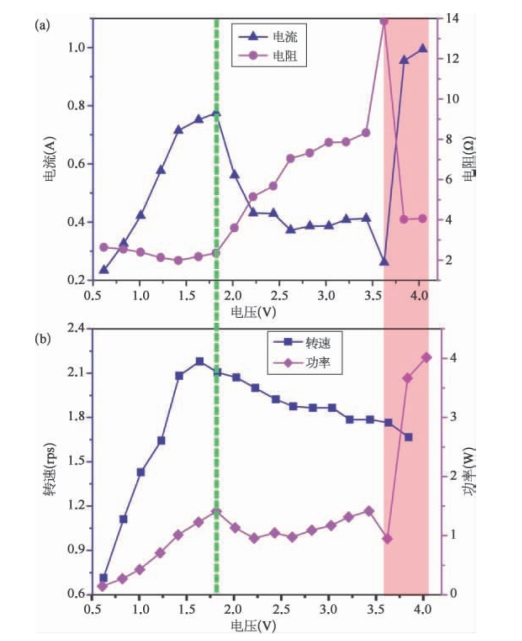
图4.26 液态金属匀速圆周运动时的关系曲线图[45]
a.平均电流-电压和平均电阻-电压关系曲线;b.转速-电压和平均功率-电压关系曲线。绿色短划线代表液态金属不同运动状态的分界线,当极间电压处于阴影区域时,液态金属将严重变形并不断碰撞极板壁。

图4.27 两极间电压为0.6 V,时间在0s、0.6s、1.0s和1.48s时的液态金属和NaOH电解液变化图[45]
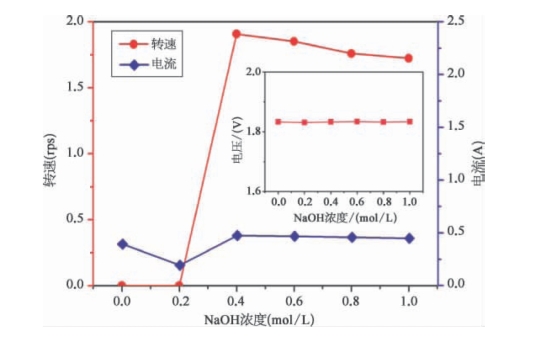
图4.28 不同NaOH溶液浓度下肾状体液态金属的转速和电流变化图(插图表示电压和NaOH溶液浓度的关系)[45]
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




