当铁碳合金中的含碳量超过铁的固溶度时,将形成碳化物。铁和碳可以形成一系列碳化物,表1-1[1]列举了铁碳化合物的类型及其晶体学参数。从Fe-Fe3C相图来看,在临界点A1以下,平衡相只有F和θ-Fe3C,但是在非平衡相变中,可能形成χ-Fe5C2、ε-Fe2.4C等碳化物,它们是不稳定的,是θ-Fe3C的过渡相。
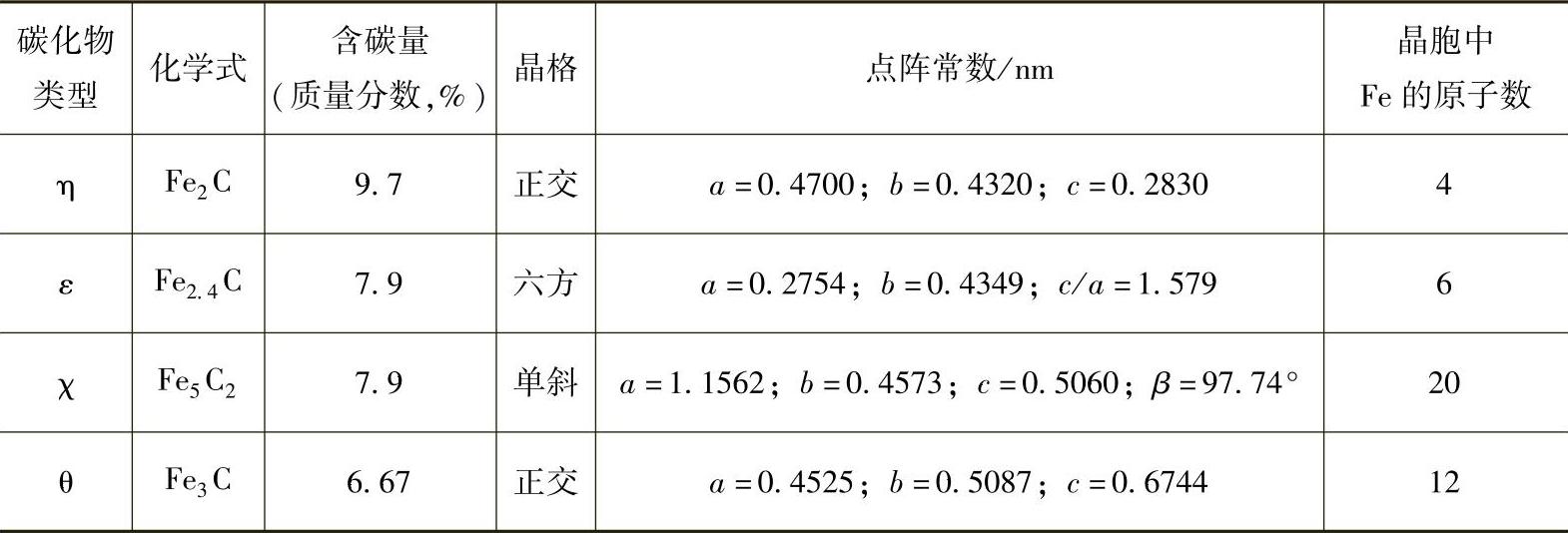
表1-1 铁碳化合物的类型及其晶体学参数
1.η-Fe2C
η-Fe2C的晶胞结构如图1-3所示,它以碳原子体心正交结构作为构架,铁原子以类似八面体的形状处于碳原子周围。片状的η-Fe2C在α相基体上常沿着位错线析出,与基体存在晶体学位向关系,片厚仅为3~5nm。
2.θ-Fe3C和χ-Fe5C2
铁在碳素钢中形成θ-Fe3C,而在合金钢中,有些碳化物形成元素在渗碳体中具有一定溶解度,故形成合金渗碳体θ-(Fe,M)3C。渗碳体是一种具有复杂晶体点阵的间隙化合物,属于正交晶系,是铁碳相图中的基本相。在渗碳体每个晶胞中有12个铁原子,碳的质量分数为6.67%,其晶体结构如图1-4a所示,每个碳原子由六个紧邻铁原子围绕。
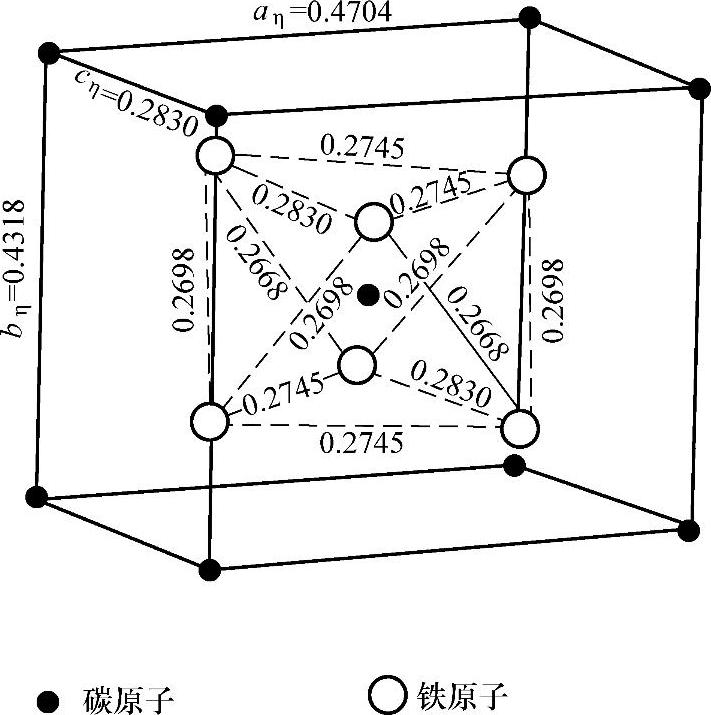
图1-3 η-Fe2C的晶胞结构
渗碳体的各个铁原子之间以金属键结合。铁原子和碳原子之间键的性质以金属键为主,存在共价键。渗碳体具有金属特性,如导电性、金属光泽等。渗碳体中能溶解其他元素形成固溶体,在形成固溶体时小原子(如氮)处于碳原子的位置,金属原子(如锰、铬等)处于铁原子的位置。这种以渗碳体为基的固溶体称为合金渗碳体,记为(Fe、Me)3C。
渗碳体(θ-Fe3C)并不是真正的平衡相,在较高温度回火时,长时间保温最终会转变为铁素体+石墨。(https://www.xing528.com)
渗碳体的硬度很高(≈800HBW),但塑性很差,特别是在游离状态下,其塑性几乎等于零。渗碳体在低温时略有铁磁性,此铁磁性在230℃以上消失。在铁碳相图中渗碳体的磁性转变温度标注为A0(230℃),渗碳体的熔点为1227℃。
χ碳化物一般用化学式χ-Fe5C2表示,具有底心单斜点阵。χ-Fe5C2的晶体结构与θ-Fe3C相似,同属于所谓三棱柱型的间隙化合物,其晶体结构如图1-4b所示。铁原子构成三棱柱的六个顶点,碳原子位于中间的间隙位置。这类间隙化合物复杂的晶胞是由三棱柱堆垛而成的,所以三棱柱是其结构的最小单元。
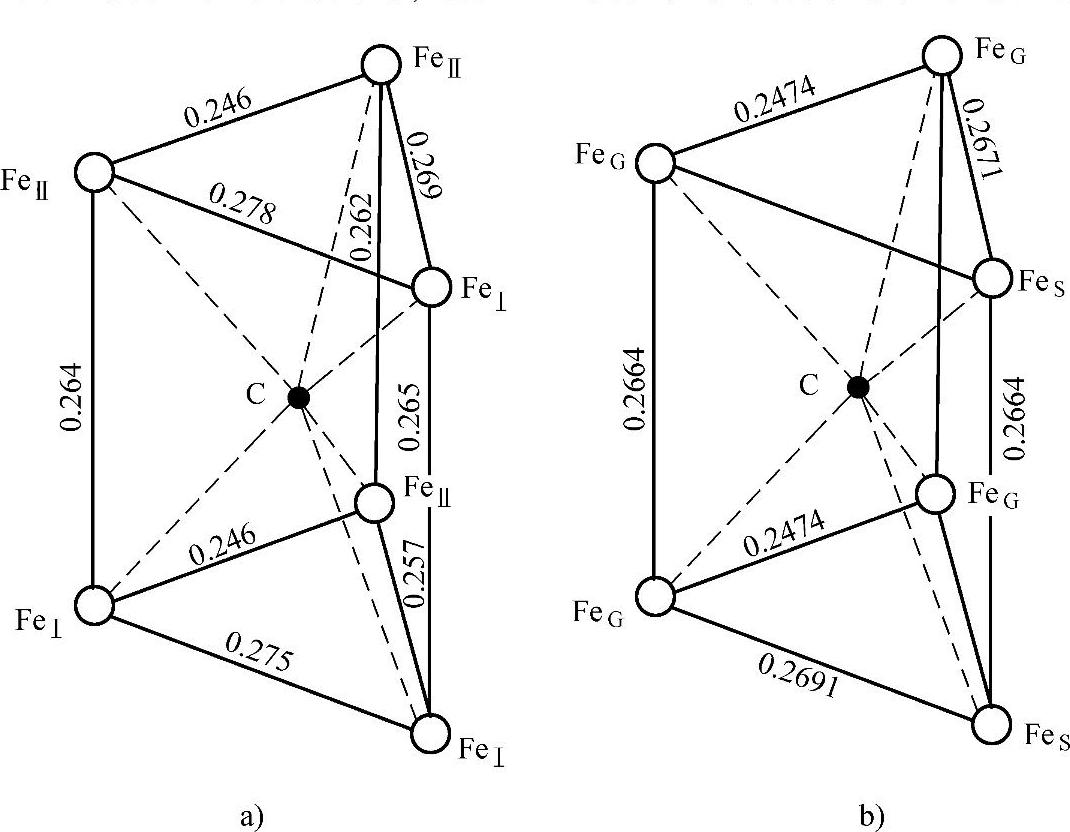
图1-4 θ-Fe3C、χ-Fe5C2晶格的三棱柱单元及其特征参数
a)θ-Fe3C b)χ-Fe5C2
θ-Fe3C的热力学稳定性比χ-Fe5C2和ε-Fe2.4C的都要高,所以在温度和时间许可的条件下,χ-Fe5C2和ε-Fe2.4C都将转变为θ-Fe3C。
从热力学上讲,θ-Fe3C也非充分稳定,在较高温度长时间保温的条件下,θ-Fe3C终将分解,转变为铁和石墨,即θ-Fe3C→3Fe+G(石墨)。可见,相对于石墨而言,θ-Fe3C也是一个亚稳相。
3.ε-碳化物
ε-Fe2.4C也是钢中经常出现的碳化物。ε-Fe2.4C于20世纪50年代初测定,直到20世纪70年代人们也未加怀疑。以后有人测定出η-Fe2C,认为ε-Fe2.4C就是η-Fe2C,因而出现六方和正交之争。目前,人们还在不同钢中进行逐一测定,尚不能得出确切的结论。
ε-碳化物的成分约在ε-Fe2.4C附近变化,是亚稳相,当温度升高时,或经过较长时间等温时,将转变为热力学上较为稳定的θ-Fe3C和χ-Fe5C2。在ε-碳化物中也能够溶入某些合金元素。ε-碳化物的居里点为370℃。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




