1.镁合金熔炼中的化学反应
(1)镁与氧的化学反应 金属镁是极活泼的元素,在固态时就可以氧化。在大气下熔炼时,镁熔体与空气中的氧直接接触,将产生强烈的氧化作用,生成氧化镁,其反应式为
2Mg+O2=2MgO (2-1)
一般当熔炼镁合金的温度超过350℃时就应通入保护气体,以减少固态的氧化。镁一经氧化,就变成氧化物,通常称为氧化烧损。镁与氧的化学亲和力很大,而且生成的氧化膜是疏松的(致密度系数α=0.79)。虽然在较低温度下镁的氧化速度不大,但当温度超过熔点,镁处于液态时,其氧化速度大大加快,镁液遇氧时即发生氧化而燃烧,放出大量的热,而生成的MgO层绝热性又很好,使反应生成的热量不能很好地散出去,因而提高了反应界面的温度,温度的提高又反过来加速了镁的氧化,使燃烧加剧。如此循环,将使反应界面的温度越来越高,最高可达2850℃,此时已引起镁的大量汽化,使燃烧更加剧烈,引起爆炸。
若在镁液中添加少量的铍[0.002%~0.01%(质量分数)]可以提高镁熔体的抗氧化能力。这是因为铍是镁的表面活性元素,富集于镁熔体表面,致使熔体表面含铍量为合金的10倍,并优先氧化。氧化铍的致密度系数α=1.71,故氧化铍充填于氧化膜孔隙中形成致密的复合氧化膜。但铍的加入量不宜过多,过多会引起晶粒粗化,恶化力学性能,并加剧热裂倾向,当温度大于750℃时,铍对提高镁的抗氧化作用大为降低。
(2)镁与水蒸气的反应 镁无论是固态还是液态均能与水发生反应,其反应方程式为
Mg+H2O=MgO+H2↑+Q (2-2)
Mg+2H2O=Mg(OH)2+H2↑+Q (2-3)
式中Q——热量。
在室温下,Mg和H2O的反应按式(2-3)进行,反应速度缓慢。随着温度升高,反应速度加快,并且Mg(OH)2会分解为H2O及MgO,在高温时只生成MgO。在其他条件相同时,镁与水蒸气间的反应将较Mg和O间的反应更为激烈。当熔融的镁液与水接触时,不仅由于发生上述反应而放出大量的热,而且还因为反应产生的氢与周围大气中的氧迅速发生反应以及液态的水受热而迅速汽化导致猛烈的爆炸,引起镁液的剧烈飞溅。因此熔炼镁合金时,与熔液相接触的炉料、工具、熔剂等均应干燥。镁与水的反应也是镁熔体中氢的主要来源,这将导致镁合金铸件出现缩松等缺陷。
(3)镁与氮的作用 镁与氮的反应方程式为
3Mg+N2=Mg3N2 (2-4)
式(2-4)的反应在室温下速度极慢,但当镁处于液态时,反应速度加快,生成多孔性Mg3N2膜,该膜既不能阻止反应的继续进行,也不能防止镁的进一步蒸发,因此氮气不能阻止镁熔体的氧化和燃烧。Mg与N2反应的激烈程度比Mg—O、Mg—H2O间的反应要弱得多。
氮还能与镁合金中的元素反应,生成氮化物,形成非金属夹渣,影响金属的纯度,并直接影响合金的耐蚀性和组织的稳定性,这是由于氮化物不稳定,遇水时氮化镁会发生分解,反应方程式如下:
Mg3N2+6H2O=3Mg(OH)2+2NH3↑ (2-5)
(4)镁与CO2、CO间的反应 镁与CO2、CO反应生成Mg2C+MgO复合物。在低温下,反应进行十分缓慢,因此可以认为,这两种气体对固态镁是惰性气体。但是在高温下,镁与CO2、CO气体间的反应将会加速,不过,其剧烈程度远较Mg—H2O及Mg—O间反应小。反应生成的表面膜有一定的防护作用。实验研究表明,在700℃下采用密封坩埚熔炼镁合金,CO2的防护性尚好。
一般认为CO2与镁在高温下产生如下反应:
2Mg+CO2=2MgO+C(无定型) (2-6)
实验证明:处于各种温度下的镁在干燥、纯净的CO2中,其氧化速度均很低,这与表面膜中出现了无定型碳有密切关系。这种无定型碳存在于氧化膜的空隙处,能提高镁表面膜的致密度系数α,使α=1.03~1.15。带正电荷的无定型碳,还能强烈地抑制镁离子透过表面膜的扩散运动,故也能抑制镁的氧化。在纯净、干燥的CO2气氛中,700℃左右,镁熔体表面形成晶莹的、有金属色泽的薄膜,此膜具有一定的塑性。但随着温度的升高,表面膜渐渐变厚变硬,致密度逐渐降低,随后发生开裂,表面膜也就失去了防护作用,镁开始燃烧。
(5)镁与硫及SO2的反应
1)镁与硫的作用。硫与镁接触时,一方面受热蒸发(硫的沸点为444.6℃),形成SO2保护性气体,另一方面硫与镁熔体反应,在熔体表面形成较致密的MgS膜(致密度系数α=0.95),减缓了镁熔体的氧化。
2)镁与SO2的作用。反应方程式为
3Mg+SO2=2MgO+MgS (2-7)
4Mg+2SO2=4MgO+S2 (2-8)
生成的MgO+MgS复合表面膜近似严密,所以具有阻缓镁液氧化的作用,因此,SO2对镁熔体有一定的防护作用。当SO2从气氛中消失后,该表面膜就会破裂,镁熔体即发生燃烧。当温度高于750℃时,此膜也将破裂,不再起防护作用,SO2将与镁液发生剧烈反应而生成大量硫化夹杂物。
2.镁合金熔炼的熔剂保护
当镁合金在大气中熔炼时,为了防止镁液表面的氧化、燃烧,常使用熔剂保护,即在镁熔体表面撒上覆盖剂。覆盖剂应保持干燥,在使用前须在300℃的烘箱中烘烤2h以上。覆盖剂要求在保证镁液不发生燃烧、不氧化的条件下尽可能少加,以确保镁合金液质量以及降低生产成本。覆盖剂在进货后,应抽样进行小炉试验,确定质量合格后方可在生产线上使用。
(1)覆盖剂性能要求
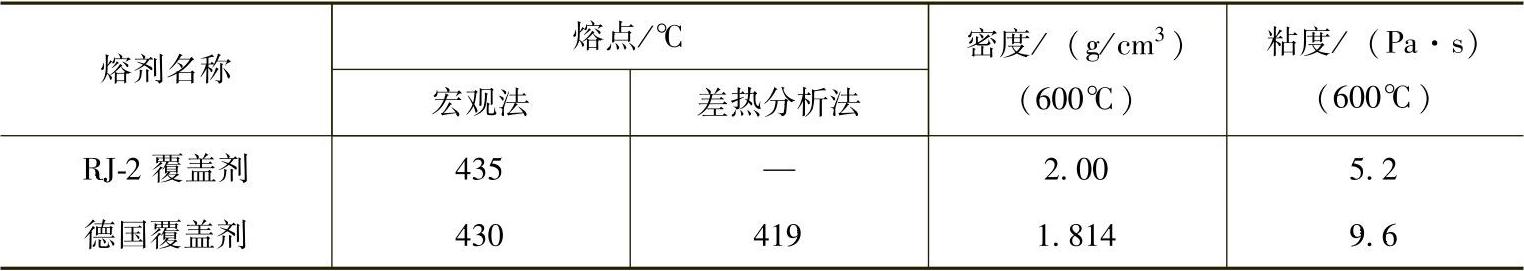
1)熔点。合适的熔点是对镁合金覆盖剂的基本要求。从使用角度看,覆盖剂的熔点应比精炼剂的熔点低一些。覆盖剂熔点的测定可采用两种方法进行:一是取200g覆盖剂在刚玉坩埚中熔化,并过热到600℃,然后停止加热,在覆盖剂液中插入直径为0.3mm的热电偶,并用温度记录仪记录其凝固曲线,取其温度平坦部分为其熔点;另一种方法是取2~3g覆盖剂放在铂金坩埚内,采用差热分析方法进行测定。国内常用的RJ-2覆盖剂以及一种德国覆盖剂的熔点见表2-8。
2)密度。镁合金的密度较小,覆盖剂的密度应尽可能接近或小于镁的密度。若覆盖剂的密度较大,则覆盖剂就容易下沉,对镁液的保护作用时间就短。几种覆盖剂的密度见表2-8。
3)粘度。覆盖剂的粘度与组成的盐类和其温度有关。对于镁合金覆盖剂,要求有一个合适的粘度。粘度低,覆盖剂的铺开性好,易和镁液分离,发泡剂易于分解;粘度高,覆盖剂铺开性差,和镁液分离困难。由于缺乏测定高温腐蚀介质粘度的专用仪器,参照熔模精密铸造中浆料的测定方法,用粘度杯漏完时间来评定覆盖剂的高温粘度。粘度杯由铸铁加工而成,壁厚为3mm,容积为100mL,小孔直径为6mm。测定前把漏斗放在箱式电炉中加热到700℃,测定时,取出漏斗放在架子上,把熔融的覆盖剂倒入杯中,测定其漏完的时间。几种覆盖剂的粘度值见表2-8。
表2-8 几种覆盖剂的熔点、密度及粘度(https://www.xing528.com)
4)铺开性和持续保护性。覆盖剂撒到镁液表面后很快熔化,在表面张力和“发泡”的作用下自动铺开形成连续的熔剂保护层。覆盖剂的铺开性越好,其对镁液的保护性能也越好,用量也减少。
持续保护性指在镁液表面加入一定量的覆盖剂后,形成的覆盖剂保护层不老化、不下沉,仍对镁液有保护作用的时间。
5)有害气体的排放量。镁合金覆盖剂由氯盐、氟盐所组成,使用中会有一定量的氯化氢、氟化氢、氯气及粉尘排出,尽可能减少排出的有害气体是衡量覆盖剂质量的关键之一。
(2)覆盖剂保护的缺点 使用保护熔剂熔炼通常会带来以下问题:①氯盐和氟盐在高温下易产生某些挥发性有毒气体,如HCl、Cl2等;②所用覆盖剂的密度一般较大,如RJ-2的密度在2.0g/cm3以上,大于镁合金的密度,因此,在熔炼过程中覆盖剂会下沉,需要不断添加,而且部分覆盖剂作为熔渣残留在合金液中形成夹杂物,降低合金的力学性能,这也是使用覆盖剂熔炼后镁合金铸件的常见缺陷;③覆盖剂挥发的气体如HCl有可能渗入合金液中,成为材料使用过程中的腐蚀源,加速材料的腐蚀,降低材料的使用寿命。
3.镁合金熔炼的气体保护
(1)SF6气体保护原理SF6是一种无色、无嗅、无毒、化学惰性很强的气体,相对分子质量为146.1,比空气重4倍。从分子结构看,一个硫原子被六个氟原子包围,具有化学惰性结构,在常温下极稳定。SF6气体是目前镁熔炼使用最广泛的保护气体。当合金液有表面搅拌或无搅拌时,保护纯镁及镁合金熔炼所需要的SF6最少用量见表2-9和表2-10。
表2-9 保护纯镁熔体所需SF6的最少用量(质量分数)[14]
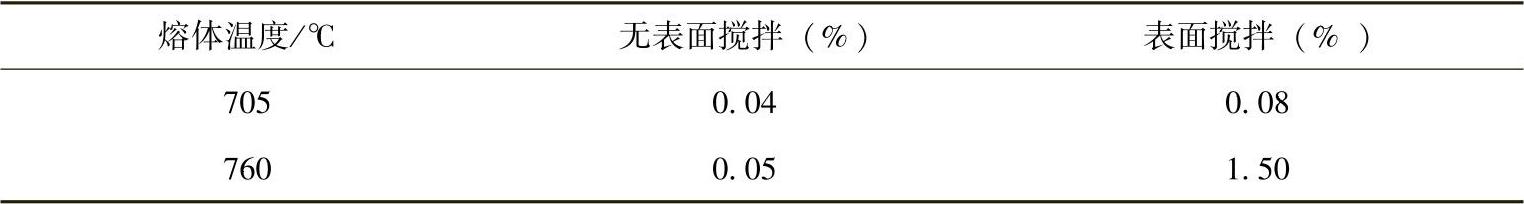
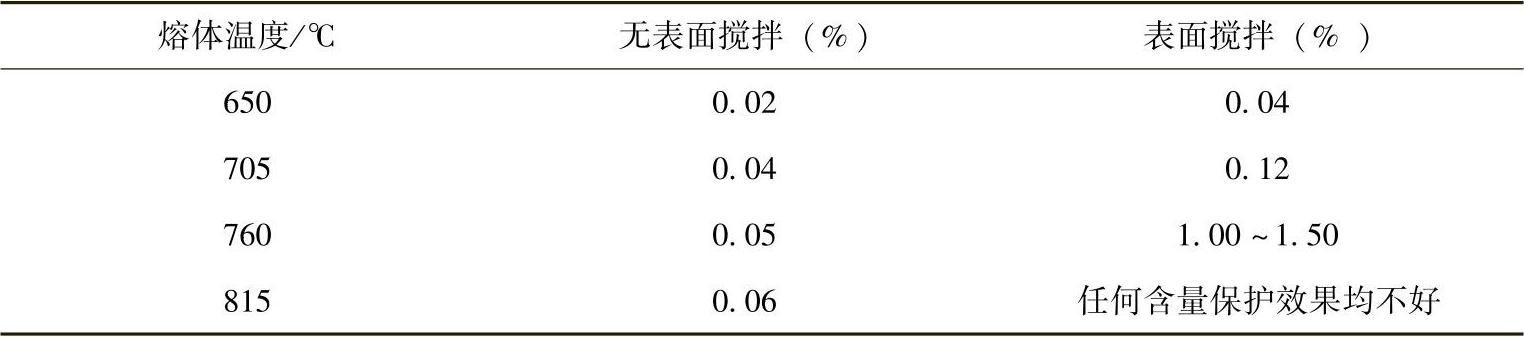
表2-10 保护AZ91B所需SF6的最少用量(质量分数)
与覆盖剂熔炼及采用Ar、CO2等气体保护熔炼相比,SF6气体保护熔炼具有如下特点:①SF6是一种无毒、无味的气体,对人体不会直接造成危害;②SF6气体用量较少,通常SF6与空气、CO2、Ar或SO2等气体混合使用,在SF6+空气或SF6+空气+CO2混合气体中,只要加入少量的SF6就能起到保护作用,因此成本低;③SF6不会对镁液产生污染。用SF6保护熔炼可以大大减少由于覆盖剂熔炼而带来的夹渣缺陷,有效降低镁合金铸件的腐蚀速率,提高耐蚀性。因此,SF6气体保护熔炼已经成为国外镁合金熔炼中广泛采用的生产技术。
通常将SF6气体加高压后变成液态,储存于专用的高压钢瓶中备用。在进行镁熔炼保护时,通过将少量SF6气体和CO2气体及干燥空气充分混合以后覆盖在镁熔体表面进行保护。SF6对镁合金液的保护主要是通过形成保护膜来实现的。其反应式为[15]
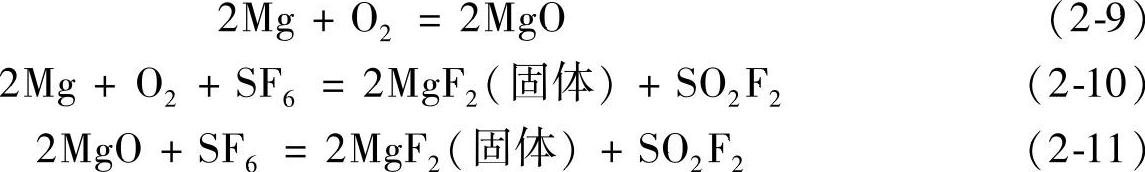
通过对表面膜分析[16],大多数物质为MgO(固体),也有少量的MgF2。MgF2是最稳定的一种化合物。通过XPS谱仪(X射线光电子能谱仪)分析,表面膜化学组成与保护气体中SF6量无关,也就是说,熔炼过程中只要维持少量的SF6,镁合金表面即能形成稳定的氧化薄膜。根据反应式(2-9)~式(2-11),氧化膜的形成过程可以描述为:首先在镁液表面,Mg与O反应生成MgO,Mg与SF6进一步反应生成MgF2,之后MgF2与MgO结合形成薄膜。这一层薄膜是有金属色泽的、致密的、连续的,以此来阻止镁合金液的进一步氧化而起到保护作用。但它只能维持几分钟,故混合气体要不间断地供应。
在镁合金的熔炼温度下,SF6会发生缓慢分解或与其他元素反应,形成SO2、HF、SF4等有毒气体。据报道,在815℃时还会产生0.1%剧毒的S2F10,但S2F10在300~350℃会分解为SF6和SF4。另外熔化镁合金的温度不会超过800℃,足以保护镁合金的SF6体积分数仅在0.4%以下,保护时混合气体的流量又极小,所产生的有毒气体可忽略不计或不存在,在实际生产应用中没有任何危险,可以认为是一种无毒、无腐蚀的保护方法。
(2)其他气体保护熔炼 SF6由于具有易用、无毒及无腐蚀的优越性能,在镁工业中得到了广泛的应用。但镁工业正面临着要求减少SF6使用的越来越大的压力,这主要出于两方面的原因:一是SF6正变得越来越昂贵,更主要的是SF6具有极高的温室效应。根据联合国政府间气候变化专门委员会(1PCC)的计算结果,SF6气体在100年之内的温室效应是CO2的23900倍,也就是说,1kgSF6的温室效应大约相当于24tCO2,而且,SF6在大气中的生存周期达到3200年,很难自然衰退。
鉴于以上原因,SF6已经受到环境保护人员严重的关注。在一份报告中,美国世界资源研究所敦促美国政府在温室气体目录中包含更多的氟化物,京都协议已经要求减少SF6气体的工业化使用。尽管镁工业消耗的SF6只占SF6年产量的10%左右,但是随着镁应用的迅速增长,SF6消耗也会大大增加。可以肯定地说,在不远的将来,SF6的大规模工业化应用将会被禁止,这就给整个镁工业提出了严峻的挑战。目前用于替代SF6的气体主要有SO2、HFC-134a及BF3等。
1)SO2保护熔炼。SO2是最早工业化使用的保护气体,但由于SO2具有毒性,并且在有水分存在的条件下会严重腐蚀钢制设备,自从20世纪70年代Fruehling[18]提出低含量的SF6具有很好的保护效果以来,SO2气体在很多工厂被禁止使用。但在人类对环境质量重新审视和全球正为减少温室效应而不懈努力的今天,SF6保护熔炼技术又受到了新的挑战,SO2气体由于没有温室效应又再次受到人们的重视。一些工厂及研究机构对SO2的保护作用做了深入的探索,应用结果表明,通过改进混气设备、增加安全装置并严格按工艺要求操作,SO2是可以用于镁熔体保护的。高压铸造工业应用结果表明,在井式工程设备中如果合理控制气体的混合和流速,SO2的体积分数在低于1%时也有好的效果,且符合环境和行业的要求。此外,在经济上也是可行的,1kgSO2的价格仅仅是SF6的10%~15%。因此大多数初级和再生厂商愿意用SO2或其他替代物代替SF6。
一般认为,SO2的保护机理是由于混合气体与镁熔体反应生成的多层复合保护膜具有保护性。可能的反应式如下:
Mg(液体)+O2(气体)+SO2(气体)=MgSO4(固体) (2-12)
MgSO4(固体)+4Mg(液体)=4MgO(固体)+MgS(固体) (2-13)
MgS(固体)+2O2(气体)=MgSO4(固体) (2-14)
2MgO(固体)+2SO2(气体)+O2(气体)=2MgSO4(固体) (2-15)
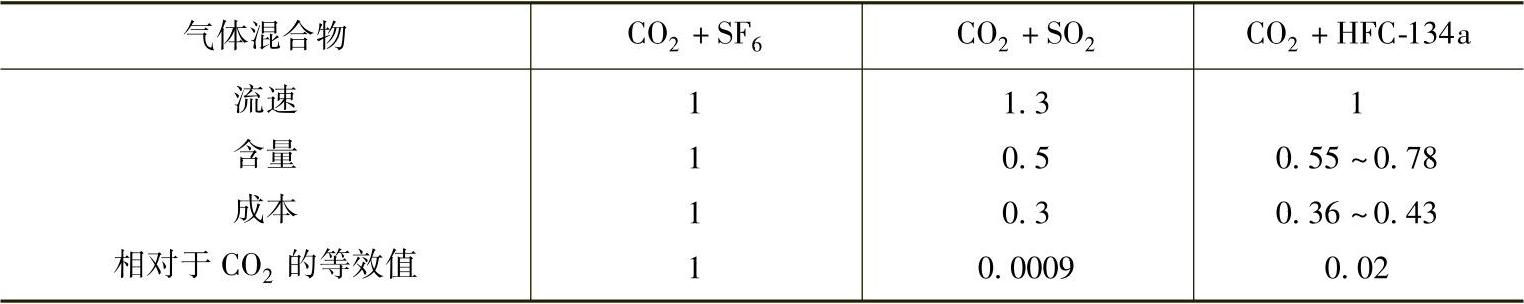
2)HFC-134a。澳大利亚的铸造合作研究中心(CAST)采用含氟材料作为SF6的替代物,并建议用HFC-134a(1,1,1,2—四氟乙烷)来代替SF6[17],认为采用HFC-134a具有以下优点:①它对一些镁合金和纯镁都有保护作用;②它的GWP值(全球变暖潜能值)是1300,而SF6为23900;③几乎没有臭氧破坏效应;④室温下安全、无毒、不燃;⑤在室温下无腐蚀性,但在金属熔融温度下由于形成HF而具有一定的腐蚀性;⑥它的价格是SF6的三分之一,且有充足的供应。CAST制造的最佳气体混合与分配系统已与澳大利亚镁业有限公司·(AMC)的3M NovecTM结合使用。Elektron镁协(UK)大规模的评估显示,CO2+HFC-134a比CO2+SF6、CO2+SO2更经济,更环保。在产品测试中用流速、含量来衡量三种替代物的价值比较,其结果见表2-11。可见,用HFC-134a代替SF6可使CO2的等值排放降低98%。与CO2+SO2的低价相比,HFC-134a的无毒更具优势。
表2-11 SF6、SO2及HFC-134a的成本及等值排放数据比较
3)BF3。Freuling[18]的研究发现BF3具有与SF6同样的保护效果,但由于成本高、反应活性及毒性而没有得到推广应用。在2000年5月,Hatch协会提出了一个新的利用BF3的系统。该系统利用KBF4在干燥空气流中分解而在线生成BF3气体。KBF4在加热的分解室中裂解为BF3和KF:
KBF4(固体)=BF3(气体)+KF(固体) (2-16)
KBF4在高于350℃发生分解,副产物KF依据反应温度的不同可呈玻璃体的固态或液态。气态的BF3由气流携带,再稀释到所需的浓度进入镁熔炼炉。该系统在680~750℃、0.3%~1.0%(体积分数)BF3的流量下,可对HPDC(高压铸造)合金熔体(AM60B)产生有效的保护。试验表明:在密封较好的情况下,工作环境及废气中的BF3的体积分数不超过0.00002%。Hatch协会为HPDC应用提出了一个BF3生产和应用的工业化系统。然而,由于工程方面的问题,以及对其高反应活性、腐蚀性及毒性的担心,而阻碍了它的进一步工业应用。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




