配位化合物(coordination compound)简称配合物,旧称络合物(complex),是一类组成复杂、种类繁多、应用广泛的化合物。早在18世纪初期人类就已制备出配合物:KCN·Fe(CN)2·Fe(CN)3。
人们在配合物的合成、性质、结构和应用方面做了大量的工作,使配合物的研究迅速发展,成为一门独立的学科——配位化学(coordination chemistry),并且广泛地渗透到分析化学、有机化学、催化化学、结构化学和生物化学等各个领域,已成为无机化学发展的主要方向。
1.配合物的定义
在1980年中国化学会公布的《无机化学命名原则》中,配位化合物的定义为:“配位化合物是由可以给出孤对电子或多个不定域电子的一定数目的离子或分子(称为配体)和具有接受孤对电子或多个不定域电子的空位的原子或离子(统称中心原子)按一定的组成和空间构型所形成的化合物。”
通常把由一定数目的配体(ligand)与形成体(formed body)所形成的复杂分子或离子称为配位个体(coordination unit)或配位单元。配位个体可以是配阳离子,如[Ag(NH3)2]+和[Cu(NH3)4]2+;配阴离子,如[PtCl6]2-;也可以是不带电荷的中性配位分子,如Ni(CO)4。配位分子本身就是配合物。配位个体与异号电荷的离子结合即形成配合物,如[Ag(NH3)2]Cl、K2[PtCl6]、[Cu(NH3)4]SO4、Ni(CO)4等均为配合物。

图3-26 配合物组成
2.配合物的组成
配合物由内界(inner sphere)和外界(outer sphere)两部分组成。内界就是配位个体,是配合物的核心部分,是由形成体(亦称中心离子或中心原子)和配位体(简称配体)通过配位键结合而成的一个相对稳定的整体,一般用方括号标明,如图3-26所示。配合物中与内界具有相反电荷的离子是外界,由于配合物是电中性的,因此,配位个体与外界离子所带电荷的数量相同、符号相反。Ni(CO)4、[PtCl6(NH3)2]等中性配位个体没有外界;在配合物[Pt(Py)4][PtCl4]中,可以认为[Pt(Py)4]2+和[PtCl4]2-均为内界,或者认为二者互为内外界。
组成配位个体的金属离子或原子统称为配合物的形成体,形成体位于配位个体的中心,是配位个体的核心部分。配合物的形成体多为过渡元素的离子或原子,如[Ag(NH3)2]+、[Cu(NH3)4]2+、K2[PtCl6]和Ni(CO)4中的Ag+、Cu2+、Pt4+和Ni均为配合物的形成体。
在配位个体中,提供孤电子对的离子或分子称为配体(ligand),如OH-、CN-、X-(卤离子)等离子以及H2O、NH3等分子。配体中提供孤电子对与形成体形成配位键的原子称为配位原子(coordination atom),常见的配位原子为电负性较大的非金属原子,如X(卤素)、O、S、C、N、P等。
按配体中所含配位原子数目的多少,可将配体分为单齿配体(monodentate ligand)和多齿配体(multidentate ligand)。只含有一个配位原子的配体称为单齿配体,如:H2O、NH3、CO(羰基)、CN-、X-、OH-、ONO-(亚硝酸根)、SCN-(硫氰酸根)、NCS-(异硫氰酸根)、Py(吡啶)等。
含有2个或2个以上配位原子的配体称为多齿配体,如:乙二胺(en)、草酸根(OX)、氨基乙酸。乙二胺四乙酸又称EDTA,是六齿配体。
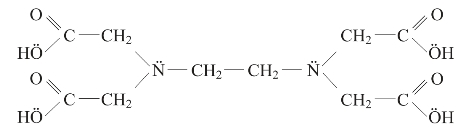
3.配位数
配位个体中直接与形成体相连的配位原子的数目称为配位数(coordination number),是形成体与配体形成配位键的数目。如[Ag(NH3)2]+中Ag+的配位数是2,[Cu(en)2]2+和[Cu(NH3)4]2+中Cu2+的配位数是4,K2[PtCl6]、[Fe(CN)6]4-中Pt4+、Fe2+的配位数是6。在配合物中,形成体的配位数可以从1到12。而最常见的配位数是4和6。
形成体的配位数=单齿配体个数=配位原子的个数(https://www.xing528.com)
形成体配位数的多少取决于形成体和配体的电荷、半径及核外电子的排布。一般来说,形成体所带正电荷越多,配位数越大;形成体半径越大,配位数也越大。与此相反,配体所带的负电荷越高,配位数越小;配体的半径越大,配位数也越小。此外,配体的浓度和反应温度对配位数也有影响,如增大配体的浓度,降低反应的温度,有利于生成高配位的配合物。
4.配位个体电荷
配位个体的电荷等于形成体的电荷与配体总电荷的代数和。例如[Ag(NH 3)2]+、[Cu(NH 3)4]2+中,由于配体是中性分子,所以配位个体的电荷就等于形成体的电荷,分别为+1和+2;而在[CoCl6]3-、[Fe(CN)6]4-中,由于形成体和配体都带电荷,所以配位个体的电荷分别为(+3)+(-1)×6=-3、(+2)+(-1)×6=-4。
如果配位个体带正电荷或负电荷,为了保证配合物的电中性,其外界必带与配位个体相反的等量电荷。因此,根据外界所带电荷数,也可判断配位个体的电荷数。如K2[PtCl6]中配位个体的电荷数为-2。
5.配合物命名
配合物的命名(nomenclature)原则与一般无机化合物的命名原则相同,不同之处在于配合物的内界。内界中,以“合”字将配体与形成体连接起来,并按如下格式命名:
配体数—配体名称—“合”—形成体名称(形成体氧化数)
其中配体数用一、二、三、四、……表示,氧化数用罗马数字Ⅰ、Ⅱ、Ⅲ、…表示,几种不同配体之间要用“·”隔开。
配体的命名次序为:先无机配体,后有机配体;先负离子,后中性分子;若配体均为负离子或均为中性分子,按配位原子元素符号的英文字母顺序排列。
命名实例如下:
[Co(NH3)6]Cl3 三氯化六氨合钴(Ⅲ)
[Fe(en)3]Br3 三溴化三(乙二胺)合铁(Ⅲ)
K[Ag(SCN)2] 二硫氰酸根合银(Ⅰ)酸钾
K[Pt(NH3)Cl3] 三氯·一氨合铂(Ⅱ)酸钾
H2[PtCl6] 六氯合铂(Ⅳ)酸
[Ag(NH3)2]OH 氢氧化二氨合银(Ⅰ)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




