【摘要】:基态的气态原子获得1个电子成为-1价气态阴离子时所需要的能量称为第一电子亲和能。电子亲和能的大小涉及核的吸引和核外电荷排斥两个因素。在周期表中,电子亲和能没有周期性的变化规律,且电子亲和能可正可负。图2-28列出了部分元素的电子亲和能数据。同一主族元素,自上而下,电子亲和能代数值总的趋势是逐渐增大,得到电子的能力降低。
基态的气态原子获得1个电子成为-1价气态阴离子时所需要的能量称为第一电子亲和能(electron affinity)。电子亲和能的大小涉及核的吸引和核外电荷排斥两个因素。原子半径减小,核的吸引力增大;但电子云密度也大,电子间排斥力增强。在周期表中,电子亲和能没有周期性的变化规律,且电子亲和能可正可负。
F(g)+e-→F-(g) E1=-328 kJ·mol-1
元素的第一电子亲和能除ⅡA族和零族元素外,一般都为负值;所有元素的第二电子亲和能都是正值。元素的第一电子亲和能越小,原子就越容易得到电子;反之,电子亲和能越大,其获得电子的能力就越小。图2-28列出了部分元素的电子亲和能数据。
 (https://www.xing528.com)
(https://www.xing528.com)
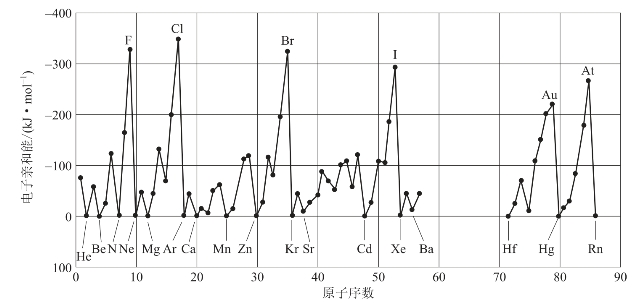
图2-28 元素的电子亲和能
同一周期从左到右,随着元素原子的有效核电荷数增大,原子半径逐渐减小,核对外层电子的吸引力增强,因此,元素原子的电子亲和能的代数值总的变化趋势是减小,原子得到电子的能力增大。当原子核外电子的排布处于全充满、半充满或全空的较稳定状态时,若要得到一个电子,则就要破坏这种稳定排布,因此,ⅡA、ⅤA族元素原子的第一电子亲和能大于其相邻元素原子的第一电子亲和能。若获得电子后,原子核外电子的排布达到半充满或全充满排布,则放出能量就多,电子亲和能代数值就小。
同一主族元素,自上而下,电子亲和能代数值总的趋势是逐渐增大,得到电子的能力降低。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




