(一)固定相
1.液—固吸附色谱 液—固吸附色谱是以固体吸附剂为固定相,如硅胶、氧化铝等。目前常用的是5~10μm的硅胶吸附剂。分配原理是组分在两相间经过反复多次的吸附与解吸分配平衡。实验室常用的吸附柱色谱装置如图8-13所示。
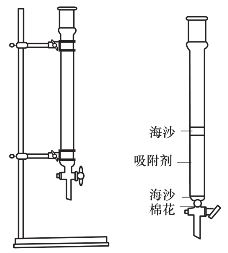
图8-13 吸附色谱柱
2.液—液分配色谱 分配色谱是利用混合物中各组分在互不相溶的流动相和固定相之间的溶解性差异而得到分离。
分配柱色谱有正相分配色谱和反相分配色谱两种。正相分配色谱常用于分离水溶性或极性较大的成分,如生物碱、苷类、有机酸等。正相分配色谱是以水或亲水相为固定相,如水、乙醇、缓冲溶液等;以与水互不相溶的弱极性有机溶剂为流动相,如氯仿、乙酸乙酯、丁醇等。反相分配色谱以亲脂性有机溶剂为固定相,以水或亲水性溶剂为流动相,可用于分离脂溶性或极性较小的成分,如高级脂肪酸、油脂等。
液体流动相涂浸在担体上。高效液相色谱早期使用的担体与气相色谱类似,是直径为100μm左右的全多孔型担体,如氧化硅、氧化铝、硅藻土等。其缺点是填料的不规则性和较宽的粒度范围导致填充不均匀,使色谱峰扩展而导致柱效降低。表层多孔型担体是表面附有厚度为1~2μm多孔硅胶的实心玻璃微珠,微珠直径为30~40μm。由于固定相仅是表面很薄一层,因此传质速度很快,同时装填容易,重现性好。缺点是比表面积较小,试样容量低,需要配用较高灵敏度的检测器。20世纪60年代后期发展了一种新型的固定相—化学键合固定相,即通过化学键把有机分子结合到担体表面。根据在硅胶表面(具有≡Si OH基团)的化学反应不同,键合固定相可分为:硅氧碳键型(≡Si
OH基团)的化学反应不同,键合固定相可分为:硅氧碳键型(≡Si O
O C);硅氧硅碳键型(≡Si
C);硅氧硅碳键型(≡Si O
O Si
Si C);硅碳键型(≡Si
C);硅碳键型(≡Si C)和硅氮键型(≡Si
C)和硅氮键型(≡Si N)。其中,使用最为广泛的是硅氧硅碳键型(≡Si
N)。其中,使用最为广泛的是硅氧硅碳键型(≡Si O
O Si
Si C)键合的固定相,因为它的化学键稳定,耐水、耐热、耐有机溶剂。
C)键合的固定相,因为它的化学键稳定,耐水、耐热、耐有机溶剂。
3.离子交换色谱和离子色谱 离子色谱用英文描述如下:
In ion-exchange chromatography(IEC),ionic components of the sample separated by selective exchange with counterions of the stationary phase.
(1)离子交换色谱(ion exchange chromatography)。离子交换色谱采用交换容量大的离子交换树脂作为固定相。流动相为无机酸或碱的水溶液,各种离子因其与树脂上离子交换基团的交换能力不同而得到分离。这种方法由于树脂的交换容量较大,试样中离子与树脂间的作用力较大,需要浓度较大的淋洗液才能洗脱,导致淋洗液的本底电导很大,采用电导检测器检测各种离子非常困难
最常见的离子交换树脂是聚苯乙烯型离子交换树脂,它是以苯乙烯为单体的球形网状结构中引入可被交换的活性基团而制成。在骨架中的苯环上,引入酸性基团得到阳离子交换树脂;引入胺基得到阴离子交换树脂。
阳离子交换树脂有强酸型的磺酸(—SO3H)阳离子交换树脂、中强酸型的磷酸(—PO3H2)阳离子交换树脂、弱酸型的羧酸(—COOH)交换树脂或酚性羟基(—OH)交换树脂。这些基团上的氢离子可被样品溶液中的阳离子交换,如NaCl与强酸型阳离子交换树脂的交换反应为:
![]()
阴离子交换树脂的交换基团为季胺、伯胺、仲胺、叔胺等碱性基团。
(2)离子色谱(ion chromatography)。离子色谱的特点如下。
①采用交换容量非常低的离子交换树脂(0.01~0.05mmol/g干树脂)作为固定相。(https://www.xing528.com)
②在分离流程中巧妙地引入了抑制柱,即在分离柱后,淋洗液携带被测离子首先进入一个填充有与分离柱性质相反的柱(即分离阳离子时,采用阳离子交换树脂作为分离柱填料,而将高交换容量的阴离子交换树脂作为抑制柱填料),抑制柱中的离子交换树脂(H+或OH-)与淋洗液(酸或碱)发生中和反应,转变成低电导水溶液,使之可以采用电导检测器方便、灵敏地进行检测。这样的离子色谱称为抑制柱型离子色谱,也称双柱抑制型离子色谱。
4.凝胶色谱(空间或体积排斥色谱) 排阻色谱用英文描述如下。
The use of exclusion packing as the stationary phase brings about a classification of molecules based largely on molecular geometry and size.Exclusion chromatography (EC)is referred to as gel permeation chromatography by polymer chemists and as gel filtration by biochemists.
凝胶渗透色谱的分离原理是当试样随流动相进入分离柱时,试样中的小分子扩散、渗透到孔穴内部,而大分子则被排阻在空穴之外。被排阻的大分子首先被流动相带出,其他不同大小的分子依次流出。
常用的固定相有葡聚糖凝胶、亲脂性葡聚糖凝胶、聚丙烯酰胺凝胶、琼脂糖凝胶。
凝胶色谱法可进行组分离和分级分离。组分离,又称脱盐,是把物质分为两组,把不能被凝胶保留而被洗脱掉的高分子物质与能扩散到凝胶中的低分子物质进行分离。分级分离是对一些分子量相差较小的,由大分子物质组成的比较复杂的混合物进行分离。凝胶色谱图如图8-14所示。
排阻色谱法的试样峰全部在溶剂的保留时间前出峰,它们在柱内停留时间短,峰较窄,利于检测。
排阻色谱可分离相对分子质量100~8×105的任何类型化合物,只要在流动相中可溶,即可进行分离。排阻色谱不能用来分离大小相似、相对分子质量接近的分子,如异构体等。
表8-6描述了如何根据被分离混合物的分子量大小来选择合适的液相色谱类型的方法。

图8-14 分子量分布图
表8-6 高效液相色谱分离类型

(二)流动相
液相色谱的流动相又称淋洗液、洗脱剂。在液—液色谱中,为避免固定液的流失,一般来说,对于亲水性固定液常用疏水性流动相,即流动相的极性小于固定相的极性,这种情况称为正相液—液色谱法。反之,若流动相的极性大于固定液的极性,称为反相液—液色谱。常用的溶剂极性由小到大排列顺序为:庚烷、己烷、环己烷、四氯化碳、甲苯、苯、氯仿、乙醚、乙酸乙酯、正丁醇、丁酮、四氢呋喃、二氧六环、丙酮、丙醇、乙醇、甲醇、乙腈、甲酰胺、水。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




