1.流动相载气
(1)载气类型。应根据检测器要求选择载气类型。热导池检测器选用导热系数较大的氢气有利于提高检测灵敏度。氢火焰离子检测器中,氮气是载气的首选目标。
(2)载气流速。载气流速是提高分离效率的重要参数。对一定的色谱柱和试样,最佳载气流速u与塔板高度H之间的计算式为:
![]()
H~u曲线如图8-8所示。在曲线的最低点,塔板高度H最小,柱效最高。该点所对应的流速即为最佳流速u最佳。u最佳和H最小可由式(8-6)微分求得:


图8-8 塔板高度与载气线速的关系
在实际工作中,为了缩短分析时间,往往使流速稍高于最佳流速。
根据式(8-10)、式(8-11)及图8-8,当流速较小时,分子扩散项(B项)是色谱峰扩散的主要因素,此时应采用相对分子质量较大的载气(N2、Ar),使组分在载气中有较小的扩散系数。当流速较大时,传质项(C项)为控制因素,宜采用相对分子质量较小的载气(H2、He)。
(3)气化温度。色谱仪进样口下端有一气化器。液体试样进样后,在气化室瞬间气化。气化温度一般较柱温高30~70℃,应防止气化温度太高造成试样分解。
2.色谱柱 色谱柱的英文描述如下。
The separation column is the heart of the chromatography.It provides versatility in the types of analysis that can be performed.This versatility, due to the wide choice of materials for the stationary and mobile phases, makes it possible to separate molecules that differ only slightly in their physical and chemical properties.Broadly speaking, the distribution of a solute between two phases results from the balance of forces between solute molecules and the molecules of each phase.
It reflects the relative attraction or repulsion that molecules or ions of the competing phases show for the solute and for themselves.These forces can be polar in nature, arising from permanent or induced dipole moments, or they can be due to dispersion forces.In ion-exchange chromatography, the forces on the solute molecules are substantially ionic in nature but include polar and nonpolar forces as well.The relative polarity of solvents is manifested in their dielectric constant.
(1)气—固色谱固定相。气—固色谱中,常用的固定相有非极性的活性炭、弱极性的氧化铝、强极性的硅胶等。常见的固定相吸附剂种类及其性能见表8-3。
表8-3 气—固色谱法常用的几种吸附剂及其性能
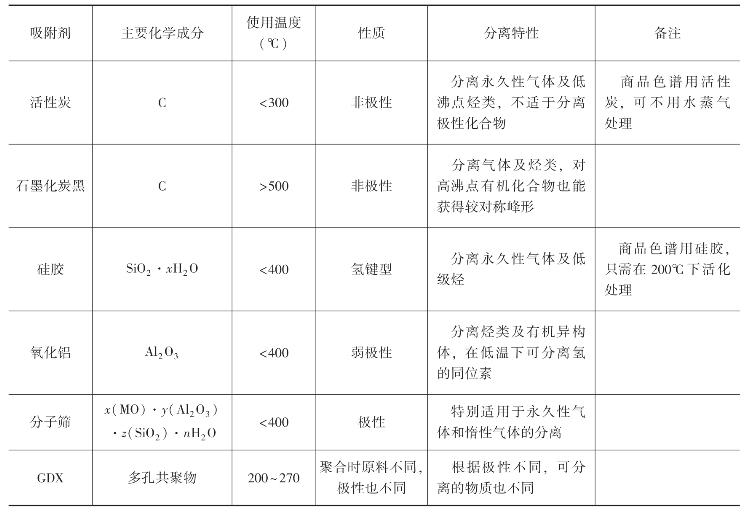
(2)气—液色谱固定相。气—液色谱中,对液态固定相的要求如下。
①挥发性小,在操作温度下有较低的蒸气压,以免流失。
②热稳定性好,在操作温度下呈液态,不发生分解。
③对试样各组分有适当的溶解能力,否则易被载气带走而起不到分配作用。
④具有高的选择性,即对沸点相同或相近的不同物质有尽可能高的分离能力。
固定液的选择一般应根据“相似相溶”原理进行。即固定液的性质和被测组分有某些相似性时,其溶解度就大。如果组分与固定液分子极性相似,固定液和被测组分两种分子间的作用力就强,被测组分在固定液中的溶解度就大。应用此原理的色谱流出规律如下。
①分离非极性物质,一般选用非极性固定液,这时试样中各组分按沸点次序先后流出色谱柱,沸点低的先出峰,沸点高的后出峰。(https://www.xing528.com)
②分离极性物质,选用极性固定液,这时试样中各组分按极性顺序分离,极性小的先流出,极性大的后流出。
③分离非极性和极性混合物,一般选用极性固定液,这时非极性组分先出峰,极性组分或易被极化的组分后出峰。
④对于能形成氢键的试样,如醇、酚、胺、水等的分离,一般选用极性或氢键型的固定液。这时试样中各组分按与固定液分子间形成氢键能力的大小先后流出,不易形成氢键的先流出,最易形成氢键的后流出。
⑤化学稳定性好,不与被测物质起化学反应。
常见的液态固定相有角鲨烷、甲基硅橡胶、苯基甲基聚硅氧烷、苯二甲酸二癸酯、聚乙二醇-20000、聚己二酸二乙二醇酯、聚丁二酸二乙二醇酯等。
气—液色谱中,液态固定相要涂浸在担体上。担体是一种具有化学惰性的多孔固体颗粒,其作用是提供一个大的惰性表面,用以承担固定液,使固定液以薄膜状态分布在其表面。担体应具有化学惰性、多孔性、热稳定性,且粒度均匀细小,一般选用40~100目。气—液色谱所用的担体可分为硅藻土型和非硅藻土型两类。硅藻土担体可分为红色担体和白色担体两种。它们都是天然硅藻土经煅烧而成,所不同的是白色担体在煅烧前于硅藻土原料中加入了少量助熔剂,如碳酸钠。红色担体表面空穴密集,孔径较小,平均孔径为1μm,比表面积大,为4.0m2/g,一般适用于分析非极性或弱极性物质。白色担体孔径较大(8~9μm),比表面积较小,只有1.0m2/g,一般用于分析极性物质。此外,硅藻土型担体表面含有相当数量的硅醇基团,分析极性试样时,会与活性中心相互作用,造成色谱峰的拖尾,因此须对担体进行钝化处理,以改进担体孔隙结构,屏蔽活性中心,提高柱效率。处理方法有酸洗、碱洗、硅烷化等。
非硅藻土型担体有氟担体、玻璃微球担体、高分子多孔微球等。
选择担体的原则如下。
①当固定液质量分数大于5%时,可选用硅藻土型(白色或红色)担体。
②当固定液质量分数小于5%时,应选用钝化处理过的担体。
③对于高沸点组分,可选用玻璃微球担体。
④对于强腐蚀性组分,可选用氟担体。
固定液在担体上的涂渍量称为配比,一般指固定液与担体的百分比,通常控制在5%~25%之间。配比越低,担体上所形成的液膜越薄,传质阻力越小,柱效越高,分析速度也越快,但允许的进样量也越小。
确定了固定液和配比后,称取一定量的担体(满足一次装柱需要),再根据担体量和配比称取固定液,将其用溶剂完全溶解后倒入担体中,缓慢使溶剂全部挥发即完成涂渍。
3.分离柱 分离柱有填充柱和毛细管柱两种。
毛细管柱和填充柱的比较见表8-4。前者的内径较小,后者较大。此外,由于毛细管柱的柱容量很小,用微量注射器很难准确地将小于0.01μL的液体试样直接送入,为此常采用分流进样方式。毛细管柱色谱和填充柱色谱的流路比较如图8-9所示。由图8-9可见,二者的主要不同是在毛细管柱色谱仪前增加了分流进样装置,柱后增加了尾吹气。
表8-4 毛细管柱和填充柱的比较
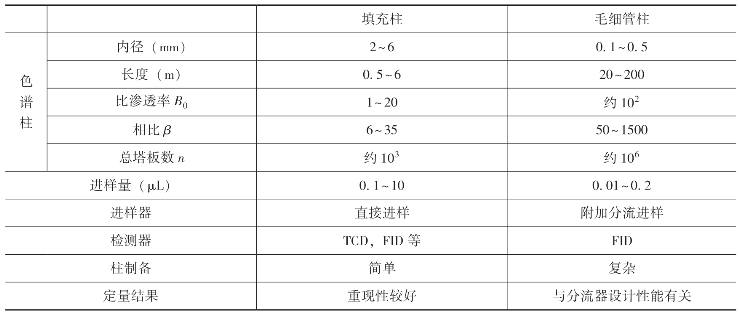
与填充柱色谱相比,毛细管柱色谱具有较高的分离效率。这是由于毛细管柱作为分离柱时,柱内不装填料,空心柱(管径0.2mm),长度可达百米,且载气气流以单路径通过柱子,消除了组分在柱中的涡流扩散现象。此外,可将固定液直接涂在毛细管的内管壁上,由于总的柱内面积较大,涂层可涂得很薄,则气相和液相传质阻力降低。这些因素使得毛细管柱的柱效比填充柱有了极大提高。
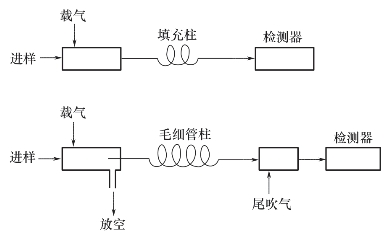
图8-9 毛细管柱色谱和填充柱色谱的流路比较
所谓分流进样,是将液体试样注入进样器使之气化,并与载气均匀混合,然后让少量试样进入色谱柱,大量试样放空。放空的试样量与进入毛细管柱的试样比称分流比,一般为50∶1~500∶1。分流后的试样能否代表原来的试样与分流器的设计有关。
柱温选择的原则是:在保证最难分离组分完全分离的前提下,尽可能采取较低的柱温,但以保留时间适宜、峰形不拖尾为度。
柱长的选用原则:在能满足分离目的的前提下,尽可能选用较短的分离柱,有利于缩短分离时间,提高工作效率。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




