差示扫描量热法和差热分析能较准确地测定和记录物质在加热过程中发生的失水、分解、相变、氧化还原、升华、熔融、晶格破坏和重建等一系列物理化学现象,以此推断物质的组成及反应的机理。
差热分析与差示扫描量热技术的主要应用领域如下。
1.玻璃化转变温度Tg 物质在玻璃化温度Tg前后的比热容变化往往使差示扫描量热或差热分析曲线呈现吸热方向的转折。试样玻璃化转变温度的读取方法如图4-8所示。

图4-8 玻璃化转变温度的测定
(1)中点玻璃化转变温度(Tmg)。前、后基线延长线距离的中点所在的水平线与玻璃化转变部分曲线的交点温度。
(2)外推玻璃化起始温度(Tig)。低温侧基线的延长线与通过玻璃化转变阶段曲线斜率最大点所引切线的交点温度。
(3)外推玻璃化终止温度(Teg)。高温侧基线的延长线与通过玻璃化转变阶段曲线斜率最大点所引切线的交点温度。
2.熔融和结晶温度 聚合物材料的结晶、熔融行为受两个主要因素的影响:外界条件
(主要是热历史)、内部分子结构。因此,在用差热扫描量热或差热分析技术测定结晶或熔融峰时往往需要消除材料的热历史。具体做法是将材料以一定的速率升至熔点以上几十度,如30~40℃甚至更高,聚合物熔体成为了均一的熔融态,大分子的有序结构得到消除,成为了完全无序的熔体(理论上完全消除)。具体温度视材料性质而定,但不能太高,以防止材料发生降解。然后,再对聚合物材料以一定速率冷却降温。最后,再升温,测定材料的熔融性质。测得的试样熔融和结晶温度等参数的读取方法分别如图4-9、图4-10所示。

图4-9 熔融温度的测定
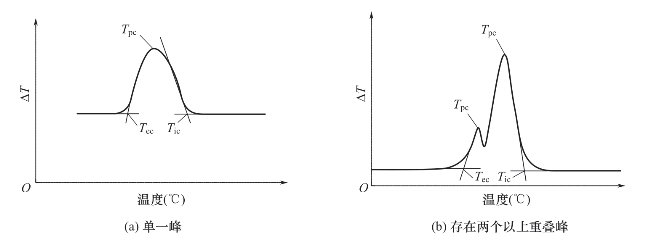
图4-10 结晶温度求法
3.水的状态确定 化合物中水的状态可分为吸附水、结晶水和结构水三种。不同状态的水的失水温度和差热曲线形状也不相同,从而可以依据差热曲线对水的状态进行分析。(https://www.xing528.com)
(1)吸附水。物质表面、颗粒周围或间隙所吸附的水称为吸附水。层间水、胶体水和潮解水等都属于吸附水。固体表面吸附的水通常加热到120℃(393K)左右即可完全失去,有些吸附力较强的吸附水需要加热到150℃(423K)左右才能完全去除。
(2)结构水。结构水是以H+、OH-、或H3O+等形式存在于矿物质晶格中的含量一定的水,是矿物中结构最牢固的水,又称化合水。结构水在加热过程中会溢出,使矿物晶格发生改变或破坏。多水高岭土的结构水失去温度为820~870℃,蒙脱石结构水失去的温度为923~973℃。
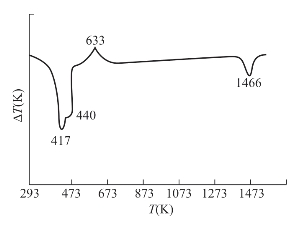
图4-11 二水石膏的差热曲线
(3)结晶水。结晶水是矿物水化作用的结果,水以水分子的形式占据矿物晶格中的一定位置,其含量固定不变。不同矿物中的结晶水结合强度不同,其失水温度也不同。石膏(CaSO4·2H2O)的差热曲线如图4-11所示。从图4-11中可见,二水石膏在140~150℃(413~423K)开始失去结晶水,变为半水石膏(CaSO4·1/2H2O),由于存在α和β两种晶型,在差热图中表现为一个毗连的双吸收峰,峰值温度为144℃(417K)、167℃(440K)。β型的半水石膏在300~400℃(573~673K)转变为六方晶系的石膏(CaSO4·εH2O,0.06<ε<0.11),产生一放热峰,峰值温度在360℃(633K)。继续加热至1193℃(1466K),生成无水的斜方晶系CaSO4。
4.同质多晶转变点的测定 同质多晶转变是指在加热或冷却过程中,成分相同的物质产生的多晶型转变。同质多晶点的测定与熔点的测定相同。
5.结晶度的测定 物质的结晶度由测试试样的结晶部分熔融所需的热量与100%结晶的同类试样的熔融热之比而求出,计算公式如下。
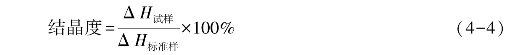
式中:ΔH试样——样品的熔融热,J/g;
ΔH标准样——相同化学结构100%结晶材料的熔融热,J/g。
例如,由差热曲线(升温速率5℃/min,氮气氛)得到的聚乙烯样品的熔融温度为131.6℃,熔融热为180J/g。而文献查得完全结晶的聚乙烯的熔融热为290J/g。则聚乙烯样品的结晶度为:

6.二元相图的绘制 差热分析法是一种绘制合金等二元相图的简易方法。图4-12(a)是根据图4-12(b)差示扫描量热法数据绘制的相图。图4-12(b)是调换了横纵坐标的差示扫描量热图,纵轴表示温度,自上而下增加。试样4的组成处于共晶点上,差示扫描量热图中显示为共晶熔融的尖锐的吸收峰。试样2、3、5的组成比介于纯试样A、B和共晶点之间。从差示扫描量热图中可知,试样在共晶熔融吸收峰之后,持续吸热,直到全部转变为液相才恢复为基线。

图4-12 存在共晶点的二元相图及其差示扫描量热曲线
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




