对气敏传感器来说,温度是它的一个非常重要的参数,所以在图2.1.3 中测试了三种采用纳米颗粒、纳米片和纳米花ZnO 粉末制成的气敏传感器在5×10-5 乙醇气体中的最佳工作温度,温度为200 ~500 ℃。这里,最佳工作温度指的是传感器在此温度下能获得对测试气体最高的灵敏度。纳米颗粒、纳米片和纳米花的最大灵敏度分别为30.8,38.9 和66.9,而它们所对应的最佳工作温度分别是400 ℃,350 ℃和350 ℃。从图2.1.3 中可以看出,在这三种传感器中,用ZnO 纳米花制成的气敏传感器几乎在所有的检测温度下都对乙醇气体具有最高的灵敏度,这就表明这种花状的形貌对提高气敏性能起到了很重要的作用。很明显,这种气敏性能的提高归因于这种独特的三维花状结构具有很高的比表面积,从而增加了对目标气体分子的吸附。

图2.1.3 用纳米颗粒、纳米片和纳米花制备的气敏传感器在不同温度下对5×10-5 乙醇气体的灵敏度
接着我们测试了这三种气敏传感器在350 ℃的工作温度下对5×10-5 乙醇气体的响应恢复时间,如图2.1.4 所示。根据对响应恢复时间的定义,我们测得ZnO 纳米颗粒的响应恢复时间为(7 s,15 s)、纳米片的响应恢复时间为(6 s,12 s)、纳米花的响应恢复时间为(6 s,8 s),因此在这三种传感器中,ZnO 纳米花对乙醇气体具有最短的响应恢复时间。这可能与ZnO 纳米花的结构有关,在这种结构的内部具有很多能够促进气体分子分散流通的通道,从而促进了气体分子的吸附和脱附。
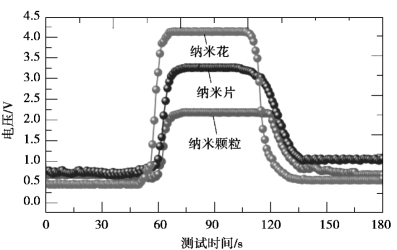
图2.1.4 用三种形貌的ZnO 制成的气敏传感器在350 ℃的工作温度下对5×10-5 乙醇气体的响应恢复时间
除了灵敏度,我们研究了ZnO 纳米花的选择性,探测了5 种有机气体,它们分别是C2H5OH,CH4,(CH3)2CO,NH3 和HCHO。图2.1.5 为ZnO 纳米花在350 ℃下对这5 种有机气体的灵敏度,其中每种气体的浓度都为5×10-5。我们发现该传感器对C2H5OH 气体具有最高的灵敏度,其次是(CH3)2CO 和CH4,而对NH3 和HCHO 几乎没有任何反应。ZnO 纳米花对C2H5OH 气体的灵敏度为73.3,而对其他气体的灵敏度不超过15。这就证明,ZnO 纳米花对C2H5OH 气体具有很好的选择性探测。

图2.1.5 用ZnO 纳米花制备的气敏传感器在350 ℃的工作温度下对不同有机气体的灵敏度
为了进一步测试ZnO 纳米花制备的传感器的重复性和稳定性。我们对该传感器进行了6 次循环测试,如图2.1.6 所示,它的响应恢复特征几乎可以重复,表明它具有很好的稳定性。图2.1.7 为用ZnO 纳米花制备的气敏传感器在350 ℃下对不同浓度的C2H5OH 气体的灵敏度,它的灵敏度在0 ~2×10-4 的浓度内增长很快,超过2×10-4 时,增长逐渐趋于缓慢,最终大约在1×10-3 达到饱和。另外,它在0 ~1×10-4 时,它的灵敏度几乎呈现直线增长,表明该传感器即使在较低的气体浓度下也有较好的气敏性能。
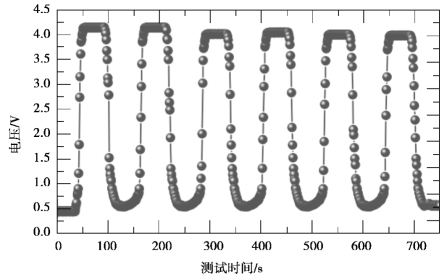
图2.1.6 用ZnO 纳米花制备的气敏传感器在350 ℃的工作温度下对5×10-5 C2H5OH 气体的6 次响应恢复特征
 (https://www.xing528.com)
(https://www.xing528.com)
图2.1.7 用ZnO 纳米花制备的气敏传感器在350 ℃的工作温度下对不同浓度C2H5OH 气体的灵敏度(插图中所示该传感器对较低浓度的C2H5OH 气体灵敏度)
ZnO 纳米花较好的气敏性能能够用表面电荷模型来解释,即气敏元件置于不同的气体环境中时它的电阻会发生改变。当气敏元件放置于空气中加热到100 ~200 ℃时,在空气中的氧分子就会吸附在ZnO 表面,并进一步产生带电的氧分子(式2.1.1)。随着温度升高到250 ~350 ℃,这些带电的氧分子通过从ZnO 的导带中获得电子进一步离解成负一和负二价的氧负离子(式2.1.2 和式2.1.3),从而使得气敏元件的电阻升高。一旦将气敏元件置于还原性气体C2H5OH 中,吸附在ZnO纳米花表面的氧负离子就会与乙醇气体分子发生反应,将电子归还于ZnO 的导带中,从而使ZnO 气敏元件的电阻降低。

分层、多孔的ZnO 纳米花的气敏性能的提高归因于该分层结构具有很多扩散通道,从而使得氧化锌能够更多地吸附空气中的氧气,则表面有更多的吸附氧。然而,对于制备的纳米颗粒,虽然它的颗粒尺寸很小,但是这些颗粒却由于范德华力的作用而团聚在一起。这种团聚使得材料内部的介孔变得非常微小甚至堵塞,不利于气体扩散而导致较长的响应恢复时间。相反,分层的花状结构则具有规整和均匀的孔和间隙,使气体分子能够顺畅地扩散,当元件置于还原性气氛中时,元件的导电态迅速发生转变。另外,这种由纳米片聚集的分层花状结构也具有较高的比表面积,进一步提高了它的气敏性能。
为了了解柠檬酸根离子对该纳米花状结构的作用,我们将不同浓度的柠檬酸钠添加到溶液中,保持其他实验条件不变,所得样品的高分辨的选区SEM 照片如图2.1.8 所示。


图2.1.8 不同浓度下的柠檬酸根离子对制备的ZnO 样品形貌的影响
当溶液中没有添加柠檬酸钠时,样品中没有任何形貌或者分层结构产生[图2.1.8(a)]。但是当柠檬酸钠添加到溶液中时,即使是很小的浓度(1 mM),ZnO 纳米片也产生了,表明柠檬酸钠对控制氧化锌的形貌有着重要作用。进一步增加柠檬酸钠的浓度到5 mM,开始出现ZnO 纳米花状结构的雏形。当增加到8 mM时,较为均匀的花状结构产生了,但是这些花状结构比较疏松。当柠檬酸钠的浓度增加到10 mM 时,均匀规整并且致密的ZnO 纳米花状结构便出现了。然而,当柠檬酸钠的浓度增加到超过15 mM 时,纳米花的堆积变得很混乱,产生了一种非常致密的球状结构,这表明只有在合适的浓度下,才能得到这种均匀、致密的分层花状结构。
根据以上分析,我们提出了该ZnO 纳米花的一种可能的生长机理,如图2.1.9所示。当溶液中没有添加柠檬酸根离子时,溶液中的锌与氢氧根离子结合,形成Zn(OH)2 前驱体和![]() 生长基元。ZnO 是一种极性晶体,它的极性+(0001)面易于吸附
生长基元。ZnO 是一种极性晶体,它的极性+(0001)面易于吸附![]() 生长基元,从而使ZnO 沿着极性方向生长。当少量的柠檬酸根离子加入时,这些柠檬酸根离子就倾向于吸附在该极性面上,从而抑制了ZnO 的极性生长,得到了片状结构。当柠檬酸根离子的量逐渐增多,柠檬酸根离子会组合成一种螯合环状物,这些螯合环状物在水热反应时可以作为一种软模板,吸附溶液中的锌离子和生长基元到其周围,使生长基元在此形核,从而使得纳米片均匀地聚集起来,生成了分层的花状结构。而当柠檬酸根离子添加量过多时,产生了大量的螯合环状物,这些环状物交错堆积,吸引生长基元在此形核,产生了致密的花状结构甚至球状结构。
生长基元,从而使ZnO 沿着极性方向生长。当少量的柠檬酸根离子加入时,这些柠檬酸根离子就倾向于吸附在该极性面上,从而抑制了ZnO 的极性生长,得到了片状结构。当柠檬酸根离子的量逐渐增多,柠檬酸根离子会组合成一种螯合环状物,这些螯合环状物在水热反应时可以作为一种软模板,吸附溶液中的锌离子和生长基元到其周围,使生长基元在此形核,从而使得纳米片均匀地聚集起来,生成了分层的花状结构。而当柠檬酸根离子添加量过多时,产生了大量的螯合环状物,这些环状物交错堆积,吸引生长基元在此形核,产生了致密的花状结构甚至球状结构。

图2.1.9 ZnO 形貌的演变机理[从(a)到(d)分别表示柠檬酸根离子浓度的升高]
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




