大多数实际液化系统都是利用膨胀阀,或称为焦耳-汤姆逊阀来获得低温。气体通过膨胀阀时,由于局部阻力,压力显著下降,这种现象叫做节流。因气体流经阀门时流速大,时间短,来不及与外界进行换热,可以近似看作绝热过程。若忽略动能和势能变化,根据能量守恒原则得到,h1=h2,即通过膨胀阀时焓不变。但在该阀中存在摩擦阻力损耗,所以它是个不可逆过程,节流后熵必定增加。
理想气体的焓仅是温度的函数,所以气体节流时,温度保持不变,而实际气体的焓是温度和压力的函数,节流后温度一般会发生变化,这一现象称为焦耳-汤姆逊效应。图30-6给出了实际气体的等焓膨胀T-p图。从图上可以看出,通过节流可以产生温升、温降及零效应。零效应的连线称为转化曲线,如图上虚线所示。焦耳-汤姆逊系数μJT反映的就是等焓下温度随压力改变的效应

焦耳-汤姆逊系数就是图30-6上等焓线的斜率。在转化曲线上,μJT=0;节流后温度升高,μJT<0;节流后温度降低,μJT>0。
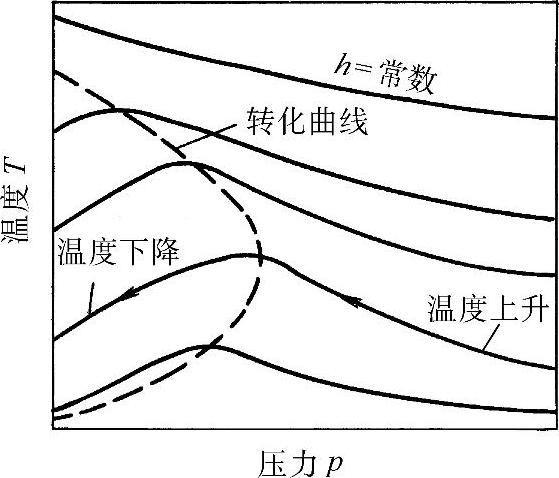
图30-6 实际气体的等焓膨胀T-p图
应用热力学基本关系式,可推出
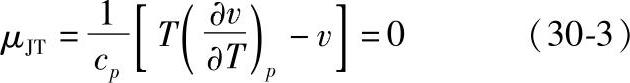
实际气体μJT表达式也可通过实验来建立,例如对于空气和氧,在p<15×103kPa时
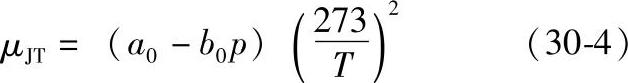
式中 a0、b0——实验常数,空气的a0=2.73×10-3,b0=0.085×10-6;氧的a0=3.19×10-3,b0=0.884×10-6。
由式(30-3)可知:(https://www.xing528.com)
当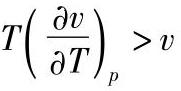 时,μJT>0,节流时温度降低;
时,μJT>0,节流时温度降低;
当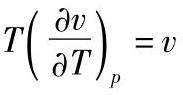 时,μJT=0,节流时温度不变;
时,μJT=0,节流时温度不变;
当 时,μJT<0,节流时温度升高。若真实气体符合范德瓦尔状态方程,则
时,μJT<0,节流时温度升高。若真实气体符合范德瓦尔状态方程,则
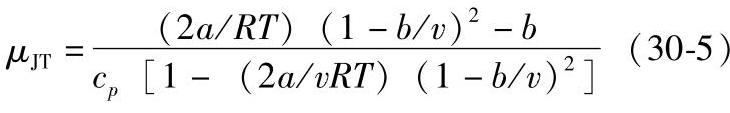
转化温度为
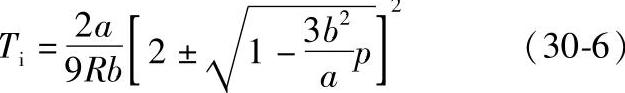
式(30-6)表示转化温度与压力之间的关系。它在T-p图上为一连续曲线,称为转化曲线。适合范德瓦尔气体的最高转化温度Ti,max为
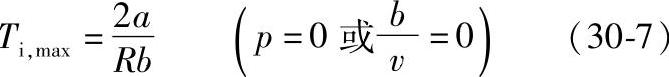
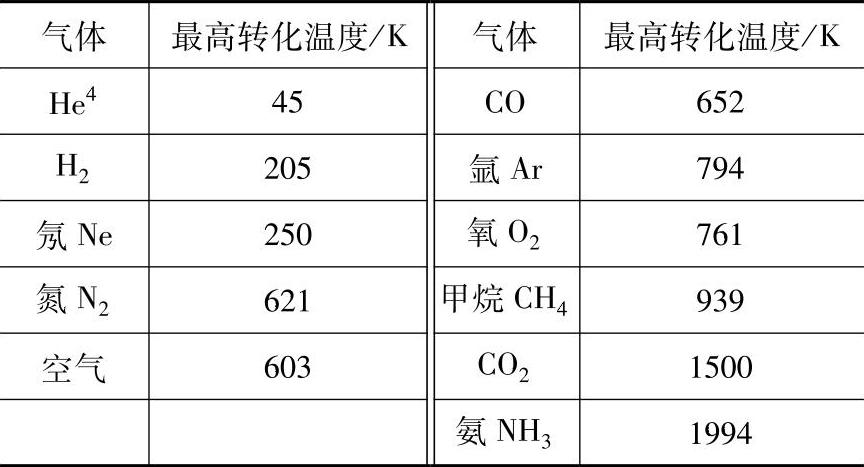
表30-7列出了一部分气体的最高转化温度。原则上可以分成两类:第一类是最高转化温度高于环境温度;第二类是最高转化温度低于环境温度,例如氦、氢、氖。第一类气体是可以单独用焦耳-汤姆逊效应来液化。第二类气体不能单独用焦耳-汤姆逊效应来液化,必须另外使用膨胀机或预冷来降低节流前的温度,这样才能得到液体产品。
表30-7 气体的最高转化温度
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




